- Beiträge: 1755
Sidebar
- Forum
- PH-Forum
- Forschung und Wissen
- Denervierung der Pulmonalarterie durch nichtinvasive stereotaktische Strahlenthe
Denervierung der Pulmonalarterie durch nichtinvasive stereotaktische Strahlenthe
24 Feb 2025 13:10 #2352
von danny
OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Denervierung der Pulmonalarterie durch nichtinvasive stereotaktische Strahlenthe wurde erstellt von danny
Denervierung der Pulmonalarterie durch nichtinvasive stereotaktische Strahlentherapie: eine Pilotstudie an Schweinemodellen zur pulmonalen Hypertonie
www.nature.com/articles/s41467-025-55933-8AbstraktDie katheterbasierte pulmonalarterielle Denervierung (PADN) hat vielversprechende Ergebnisse bei der Behandlung von pulmonaler Hypertonie (PH) erzielt. Wir präsentieren hier die stereotaktische Körperradiotherapie (SBRT) als neuen nichtinvasiven Ansatz für PADN. Eine einzelne Fraktion von 15 Gy, 20 Gy oder 25 Gy wurde für PADN in einem durch Thromboxan A2 (TxA2) induzierten Schweinemodell für akute PH verabreicht. Wir haben gezeigt, dass PADN durch 20-Gy-SBRT den mittleren pulmonalarteriellen Druck (PA) während der TxA2-Herausforderung senkte. Alle SBRT-Dosierungen führten im Vergleich zur Radiofrequenzablation (RFA) zu einem tieferen Denervierungsbereich und verringerten die sympathische neurale Noradrenalinsynthese in der Ablationszone. Mögliche strahlungsbedingte Nebenwirkungen wurden hauptsächlich bei Tieren festgestellt, die mit 25 Gy behandelt wurden. Bei Tieren mit nachfolgender, durch Monocrotalin induzierter chronischer PH führte PADN durch 20-Gy-SBRT zu einer signifikanteren Verbesserung der pulmonalen Hämodynamik und der PA-Umgestaltung im Vergleich zur RFA. Zusammenfassend deuten unsere Ergebnisse darauf hin, dass ein geeignetes SBRT-Schema die Wirksamkeit und Sicherheit bei PADN ausbalancieren könnte, was eine neuartige Strategie zur Behandlung von PH darstellen könnte.
EinführungPulmonale Hypertonie (PH) ist eine fortschreitende Erkrankung, die durch einen erhöhten pulmonalvaskulären Widerstand (PVR) und pulmonalarteriellen Druck gekennzeichnet ist und anschließend zu Rechtsherzversagen und letztendlich zum Tod führt. Trotz deutlicher Fortschritte in der medikamentösen Behandlung leiden PH-Patienten nach wie vor unter einer hohen Symptomlast und haben eine schlechte Langzeitprognose 1 , 2. Umfangreiche Forschungsarbeiten haben gezeigt, dass eine Überaktivierung des sympathischen Nervensystems und die anschließende Vasokonstriktion und Umgestaltung der PA eine entscheidende Rolle bei der Pathogenese von PH spielen 3 , 4. Die PA-Denervierung (PADN), eine innovative Therapie, bei der meist eine katheterbasierte Radiofrequenzablation (RFA) eingesetzt wird, um Barorezeptoren oder sympathische Nervenfasern im Bereich der Bifurkation der Haupt-PA zu zerstören, hat sich in Tierstudien und ersten Humanstudien allmählich als hilfreich bei der Verbesserung der pulmonalen Hämodynamik erwiesen 5 , 6 , 7 , 8 , 9 , 10 , 11 . In einer jüngsten Scheinkontrollstudie an mehreren Standorten und mit randomisierten Studien konnte durch PADN die körperliche Belastbarkeit und die klinischen Ergebnisse bei Patienten mit PH der WHO-Gruppe I während einer 6-monatigen Nachbeobachtung verbessert werden 12 .Beim Menschen werden die PAs vor allem durch sympathische Nerven innerviert, die im Fett- und Bindegewebe rund um den Hauptstamm und die Bifurkation der PA konzentriert sind, wobei > 40 % der Nerven in einer Tiefe von > 4 mm liegen 13 , 14. Daher ist die Wirksamkeit der transluminalen RFA-basierten PADN möglicherweise aufgrund der nicht erreichbaren Ablationstiefe begrenzt 15 , 16. Außerdem wurden in präklinischen Experimenten Lungenembolien und mit RFA assoziierte Verletzungen der PA-Wand festgestellt, darunter Dissektion, fokale Blutungen, verringerte mediale Dicke, Intimaruptur und Thrombose 7 , 16. Außerdem wurden bei der Anwendung in der realen Welt häufig verfahrensbedingte Brustschmerzen beobachtet 5 , 17 .Die stereotaktische Körperradiotherapie (SBRT) ist eine häufig eingesetzte nichtinvasive Technologie zur Behandlung solider Tumoren, bei der hochdosierte Strahlung präzise auf das Ziel gerichtet wird, während durch einen schnellen Dosisabfall die Verletzung des umliegenden Gewebes minimiert wird. Darüber hinaus wurde die SBRT erfolgreich zur Behandlung einer begrenzten Anzahl von Patienten mit Herzrhythmusstörungen eingesetzt, darunter ventrikuläre Tachykardie und Vorhofflimmern 18 , 19. Kürzlich konnte in Schweinemodellen gezeigt werden, dass die SBRT bei entsprechender Strahlendosis sicher und effektiv zur renalen Denervierung eingesetzt werden kann. Verglichen mit konventioneller Radiofrequenz bietet die SBRT die Vorteile eines nichtinvasiven Ansatzes und einer vollständigen, zirkulären Denervierung 20 , 21 .Bis heute ist der potenzielle Nutzen der nichtinvasiven SBRT für PADN unbekannt. Hier zeigen wir, dass die SBRT bei Anwendung des entsprechenden Schemas die sympathische Innervation der PAs nichtinvasiv beeinträchtigen kann, was zu einer anschließenden Verbesserung der Lungenhämodynamik sowohl bei Schweinemodellen von PH auf Basis akuter Vasokonstriktion als auch bei chronischer Monocrotalin-(MCT-)induzierter PH führt.ErgebnisseSBRT-VerfahrenAlle Tiere überlebten die erwartungsgemäße Lebensphase der Studie. Die SBRT wurde für PADN in den Behandlungsgruppen erfolgreich durchgeführt (Abb. 1 ) und während der perioperativen Phase wurden keine akuten Komplikationen beobachtet. Die Behandlungsparameter sind in der Zusatztabelle 1 aufgeführt . Strahlungsdosis und Volumenbeschränkung der gefährdeten Organe (OARs) führten zu einer Dosisverteilung, die bei einigen Tieren nicht perfekt mit dem Zielvolumen übereinstimmte. Ein typisches Dosis-Volumen-Histogramm ist in der Zusatzabbildung 1 dargestellt und zeigt, dass die angegebene Dosis präzise auf den Bifurkationsbereich der Haupt-PA zielte, mit einem schnellen Dosisabfall, um die Strahlung auf das umliegende Gewebe zu minimieren.Abb. 1: Verfahren der stereotaktischen Körperradiotherapie (SBRT) zur Denervierung der Lungenarterie.
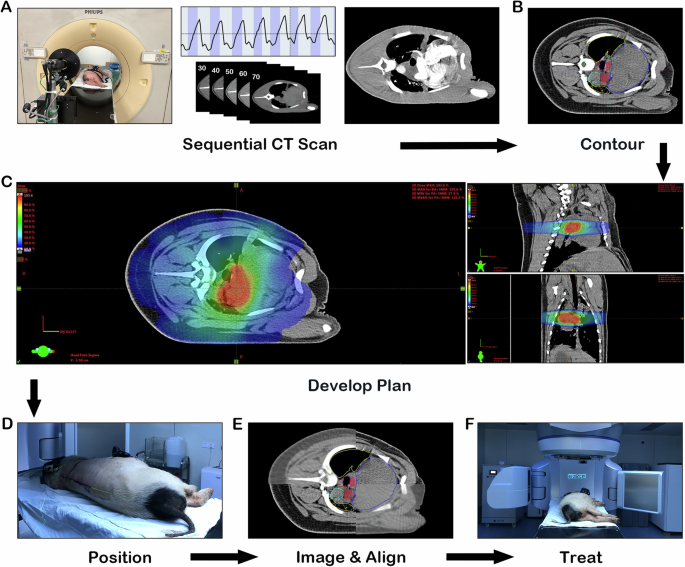 Ein Bama-Miniaturschwein wird einer sequentiellen Computertomographie (CT) des Brustbereichs unterzogen, darunter ein atmungsgesteuerter 4-dimensionaler CT-Scan unter Verwendung des Real-time Position Management Respiratory Gating Systems und ein kontrastmittelverstärktes CT. B Das Zielvolumen, das den Bereich der Lungenarteriengabelung zeigt, ist in fünf Atmungsphasen (30 – 70 %) der 4-dimensionalen CT rot dargestellt, und das interne Zielvolumen wird dann zur Bewegungskompensation auf dem phasengemittelten CT-Bild erstellt. Zu den Konturen der gefährdeten Organe zählen Herz (blau), Lunge (gelb), Luftröhre (violett), Speiseröhre (braun), Aorta (cyan) und Rückenmark (grün). C In diesem Behandlungsplan wird das geplante Zielvolumen (orangefarbene Grenze), eine 5 mm große Erweiterung des internen Zielvolumens (rote Grenze), mit einer Dosis von 20 Gy verabreicht. Die Farbskala zeigt, dass die verschriebene Dosis das Ziel umfasst und gleichzeitig die Strahlung des umliegenden Gewebes bei einem schnellen Dosisabfall minimiert. D Zum Zeitpunkt der Behandlung wird das Schwein mithilfe von Lasern und Hautmarkierungen positioniert. E Vor der Bestrahlung wird eine Cone-Beam-CT zur Bildausrichtung mit der Planungs-CT durchgeführt. F Anschließend wird eine atmungsgesteuerte SBRT mithilfe eines bildgesteuerten Linearbeschleunigers durchgeführt.
Hämodynamische LeistungZu Beginn entwickelten sowohl PADN- als auch Kontrolltiere PH, wie durch einen maximalen mittleren PA-Druck (PAP) von über 40 mmHg gezeigt wurde, und die hämodynamische Reaktion auf die Infusion eines Thromboxan-A2-Agonisten (TxA2) war bei beiden Gruppen ähnlich. In der 4-Monats-Nachuntersuchung reduzierte PADN durch RFA und 20-Gy-SBRT den mittleren und systolischen PAP während der TxA2-Exposition ( P < 0,05), während in den 15-Gy- und 25-Gy-Gruppen im Vergleich zu den Kontrolltieren keine signifikanten Unterschiede festgestellt wurden. Zudem zeigte der diastolische PAP nach PADN als Reaktion auf die TxA2-Infusion eine ähnliche Tendenz wie der mittlere und systolische PAP, erreichte aber im Vergleich zu den unbehandelten Tieren keine statistische Signifikanz (Abb.
2
). Es wurden keine signifikanten Auswirkungen auf die Herzfrequenz oder den systemischen Blutdruck beobachtet (Ergänzende Abb.
2
).Abb. 2: Pulmonale Hämodynamik.
Ein Bama-Miniaturschwein wird einer sequentiellen Computertomographie (CT) des Brustbereichs unterzogen, darunter ein atmungsgesteuerter 4-dimensionaler CT-Scan unter Verwendung des Real-time Position Management Respiratory Gating Systems und ein kontrastmittelverstärktes CT. B Das Zielvolumen, das den Bereich der Lungenarteriengabelung zeigt, ist in fünf Atmungsphasen (30 – 70 %) der 4-dimensionalen CT rot dargestellt, und das interne Zielvolumen wird dann zur Bewegungskompensation auf dem phasengemittelten CT-Bild erstellt. Zu den Konturen der gefährdeten Organe zählen Herz (blau), Lunge (gelb), Luftröhre (violett), Speiseröhre (braun), Aorta (cyan) und Rückenmark (grün). C In diesem Behandlungsplan wird das geplante Zielvolumen (orangefarbene Grenze), eine 5 mm große Erweiterung des internen Zielvolumens (rote Grenze), mit einer Dosis von 20 Gy verabreicht. Die Farbskala zeigt, dass die verschriebene Dosis das Ziel umfasst und gleichzeitig die Strahlung des umliegenden Gewebes bei einem schnellen Dosisabfall minimiert. D Zum Zeitpunkt der Behandlung wird das Schwein mithilfe von Lasern und Hautmarkierungen positioniert. E Vor der Bestrahlung wird eine Cone-Beam-CT zur Bildausrichtung mit der Planungs-CT durchgeführt. F Anschließend wird eine atmungsgesteuerte SBRT mithilfe eines bildgesteuerten Linearbeschleunigers durchgeführt.
Hämodynamische LeistungZu Beginn entwickelten sowohl PADN- als auch Kontrolltiere PH, wie durch einen maximalen mittleren PA-Druck (PAP) von über 40 mmHg gezeigt wurde, und die hämodynamische Reaktion auf die Infusion eines Thromboxan-A2-Agonisten (TxA2) war bei beiden Gruppen ähnlich. In der 4-Monats-Nachuntersuchung reduzierte PADN durch RFA und 20-Gy-SBRT den mittleren und systolischen PAP während der TxA2-Exposition ( P < 0,05), während in den 15-Gy- und 25-Gy-Gruppen im Vergleich zu den Kontrolltieren keine signifikanten Unterschiede festgestellt wurden. Zudem zeigte der diastolische PAP nach PADN als Reaktion auf die TxA2-Infusion eine ähnliche Tendenz wie der mittlere und systolische PAP, erreichte aber im Vergleich zu den unbehandelten Tieren keine statistische Signifikanz (Abb.
2
). Es wurden keine signifikanten Auswirkungen auf die Herzfrequenz oder den systemischen Blutdruck beobachtet (Ergänzende Abb.
2
).Abb. 2: Pulmonale Hämodynamik.
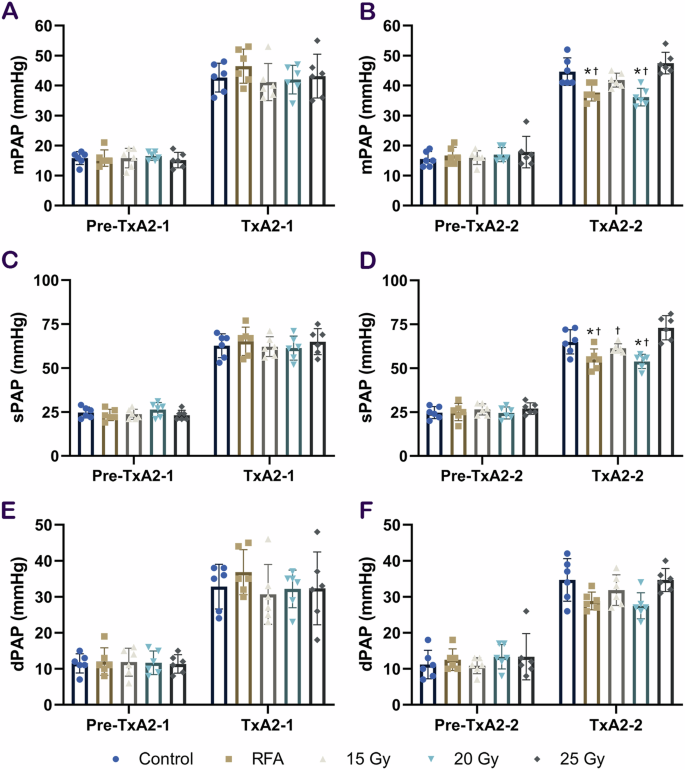 A , B Mittlerer pulmonalarterieller Druck (mPAP), C , D systolischer pulmonalarterieller Druck (sPAP) und E , F diastolischer pulmonalarterieller Druck (dPAP) zu Beginn und maximaler Thromboxan-A2-Agonist (TxA2) vor (TxA2-1) und 4 Monate nach (TxA2-2) Verfahren zur pulmonalarteriellen Denervierung in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. Der zweiseitige P-Wert wurde aus einer einfaktoriellen ANOVA mit Bonferroni-Post-hoc-Analyse berechnet. * P < 0,05 vs. Kontrolle. † P < 0,05 vs. 25-Gy-Gruppe. RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Quantifizierung von Plasma-Noradrenalin (NE) und Renin-Angiotensin-Aldosteron-System (RAAS)Es gab keine signifikanten Unterschiede in den absoluten Konzentrationen von NE, Renin, Angiotensin II und Aldosteron im Plasma oder in der Veränderungsrate zwischen den Kontroll- und Behandlungsgruppen zu Studienbeginn und bei der 4-Monats-Nachuntersuchung (alle P > 0,05, Zusatztabelle
2
).Auswirkungen der SBRT in der AblationszoneAbgesehen von einer leichten Gewebeanhaftung, die gelegentlich in der 25-Gy-Gruppe festgestellt wurde, wurden bei der makroskopischen anatomischen Untersuchung keine eindeutigen Läsionen entlang der behandelten PAs beobachtet (Ergänzende Abbildung
3
).Ähnlich wie bei Nervenverletzungen durch intravaskuläre Radiofrequenz- oder Ultraschallablation kann die SBRT die PA-Nerven wirksam zerstören und sich als degenerative oder nekrotische endoneurale Veränderungen äußern, darunter Vakuolisierung, Kernpyknose, Bildung von Verdauungskammern und Koagulationsnekrose sowie leichte bis mittelschwere perineurale Fibrose und Kollagenablagerung (Abb.
3A
). Die Gesamtwerte der Nervenverletzungen waren in den RFA-, 20-Gy- und 25-Gy-Gruppen signifikant höher (2,5 ± 0,2, 2,5 ± 0,4, 2,7 ± 0,2 vs. 1,2 ± 0,5, P < 0,01), aber nicht in der 15-Gy-Gruppe (1,9 ± 0,5 vs. 1,2 ± 0,5, P > 0,05) als in den Kontrollgruppen. Darüber hinaus führte eine Dosierung von 25 Gy zu stärkeren Nervenschäden als 15 Gy ( p < 0,05, Abb.
3B
). Ebenso führte PADN mit 20 Gy und 25 Gy zu erheblichen Nervenverletzungen in beiden Regionen innerhalb und jenseits von 5 mm vom Lumen ( p < 0,05), während in der 15-Gy-Gruppe keine statistischen Unterschiede im Vergleich zu den Kontrollgruppen festgestellt wurden ( p > 0,05). PADN durch RFA verursachte jedoch keine signifikanten Nervenschäden jenseits von 5 mm vom Lumen ( p > 0,05), trotz offensichtlicher Verletzungen der Nerven innerhalb von 5 mm ( p < 0,01, Abb.
3C, D
).Abb. 3: Beurteilung pathologischer Nervenverletzungen.
A , B Mittlerer pulmonalarterieller Druck (mPAP), C , D systolischer pulmonalarterieller Druck (sPAP) und E , F diastolischer pulmonalarterieller Druck (dPAP) zu Beginn und maximaler Thromboxan-A2-Agonist (TxA2) vor (TxA2-1) und 4 Monate nach (TxA2-2) Verfahren zur pulmonalarteriellen Denervierung in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. Der zweiseitige P-Wert wurde aus einer einfaktoriellen ANOVA mit Bonferroni-Post-hoc-Analyse berechnet. * P < 0,05 vs. Kontrolle. † P < 0,05 vs. 25-Gy-Gruppe. RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Quantifizierung von Plasma-Noradrenalin (NE) und Renin-Angiotensin-Aldosteron-System (RAAS)Es gab keine signifikanten Unterschiede in den absoluten Konzentrationen von NE, Renin, Angiotensin II und Aldosteron im Plasma oder in der Veränderungsrate zwischen den Kontroll- und Behandlungsgruppen zu Studienbeginn und bei der 4-Monats-Nachuntersuchung (alle P > 0,05, Zusatztabelle
2
).Auswirkungen der SBRT in der AblationszoneAbgesehen von einer leichten Gewebeanhaftung, die gelegentlich in der 25-Gy-Gruppe festgestellt wurde, wurden bei der makroskopischen anatomischen Untersuchung keine eindeutigen Läsionen entlang der behandelten PAs beobachtet (Ergänzende Abbildung
3
).Ähnlich wie bei Nervenverletzungen durch intravaskuläre Radiofrequenz- oder Ultraschallablation kann die SBRT die PA-Nerven wirksam zerstören und sich als degenerative oder nekrotische endoneurale Veränderungen äußern, darunter Vakuolisierung, Kernpyknose, Bildung von Verdauungskammern und Koagulationsnekrose sowie leichte bis mittelschwere perineurale Fibrose und Kollagenablagerung (Abb.
3A
). Die Gesamtwerte der Nervenverletzungen waren in den RFA-, 20-Gy- und 25-Gy-Gruppen signifikant höher (2,5 ± 0,2, 2,5 ± 0,4, 2,7 ± 0,2 vs. 1,2 ± 0,5, P < 0,01), aber nicht in der 15-Gy-Gruppe (1,9 ± 0,5 vs. 1,2 ± 0,5, P > 0,05) als in den Kontrollgruppen. Darüber hinaus führte eine Dosierung von 25 Gy zu stärkeren Nervenschäden als 15 Gy ( p < 0,05, Abb.
3B
). Ebenso führte PADN mit 20 Gy und 25 Gy zu erheblichen Nervenverletzungen in beiden Regionen innerhalb und jenseits von 5 mm vom Lumen ( p < 0,05), während in der 15-Gy-Gruppe keine statistischen Unterschiede im Vergleich zu den Kontrollgruppen festgestellt wurden ( p > 0,05). PADN durch RFA verursachte jedoch keine signifikanten Nervenschäden jenseits von 5 mm vom Lumen ( p > 0,05), trotz offensichtlicher Verletzungen der Nerven innerhalb von 5 mm ( p < 0,01, Abb.
3C, D
).Abb. 3: Beurteilung pathologischer Nervenverletzungen.
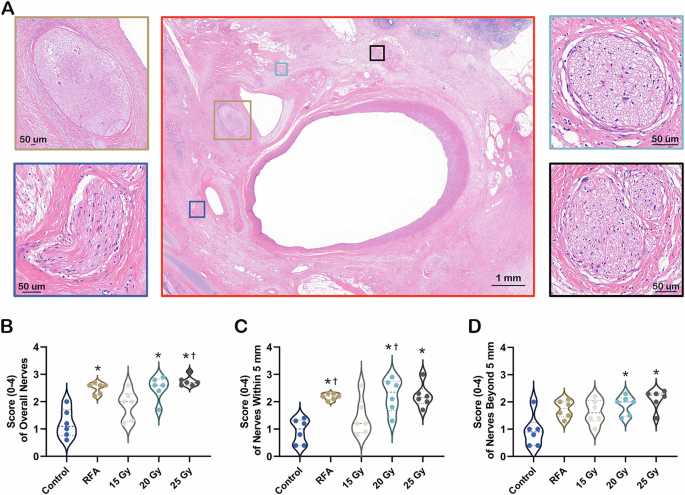 Ein repräsentatives Bild der Pulmonalarterie (rotes Quadrat), gefärbt mit Hämatoxylin und Eosin nach stereotaktischer Radioablation. Vergrößerte Mikrofotografien, auf denen strahleninduzierte degenerative oder nekrotische endoneurale Veränderungen einschließlich Vakuolisierung, Kernpyknose (cyanfarbenes Quadrat), Bildung von Verdauungskammern (schwarzes Quadrat) und Koagulationsnekrose (dunkelgelbes Quadrat) sowie leichte bis mittelschwere perineurale Fibrose und Kollagenablagerung gezeigt werden. Gleichzeitig wird auch der relativ normale Nerv (blaues Quadrat) angezeigt. Semiquantitativer Gesamtwert der Nervenverletzung B und Werte in Regionen innerhalb von C und jenseits von 5 mm D vom Arterienlumen in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. Der zweiseitige P-Wert wurde aus dem Kruskal-Wallis-Test berechnet, gefolgt von allen paarweisen Mehrfachvergleichen. * P < 0,05 vs. Kontrolle. † P < 0,05 vs. 15-Gy-Gruppe. RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Alle radioablativen Läsionen, die in der Tiefe von der Intima bis zur tiefsten Stelle der Gewebeverletzung dargestellt wurden, waren > 10 mm, und SBRT führte im Vergleich zur RFA zu einem tieferen Denervierungsbereich ( P < 0,05). Das Endothel der anvisierten PAs blieb bei allen Versuchspersonen intakt, und bei den mit 20 Gy und 25 Gy ablatierten Tieren wurde gelegentlich eine minimale Neointima beobachtet, die sich auf der inneren elastischen Lamina bildete. Die mediale PA-Verletzung, die sich durch minimalen bis mäßigen Verlust glatter Muskelzellen bei Proteoglykan-Ersatz zeigt, nahm dosisabhängig zu, ohne statistische Signifikanz zu erreichen ( P > 0,05). Die durch minimale bis leichte perivaskuläre Entzündung und Verlust glatter Muskelzellen gekennzeichnete nutritive Arteriolenschädigung war in der 15-Gy-Gruppe geringer als in der RFA- und 25-Gy-Gruppe ( P < 0,05). Darüber hinaus nahm die Schwere der Weichteilverletzungen, die durch denaturiertes Kollagen, Entzündungen, Fettnekrose und Fibrose gekennzeichnet waren, mit zunehmender SBRT-Dosis allmählich zu, und RFA verursachte schwerwiegendere Weichteilverletzungen als SBRT mit 15 Gy und 20 Gy. Die spezifischen Daten und repräsentativen Bilder sind in der Zusatztabelle
3
und Abb.
4
dargestellt .Abb. 4: Repräsentative Bilder des Ablationsbereichs.
Ein repräsentatives Bild der Pulmonalarterie (rotes Quadrat), gefärbt mit Hämatoxylin und Eosin nach stereotaktischer Radioablation. Vergrößerte Mikrofotografien, auf denen strahleninduzierte degenerative oder nekrotische endoneurale Veränderungen einschließlich Vakuolisierung, Kernpyknose (cyanfarbenes Quadrat), Bildung von Verdauungskammern (schwarzes Quadrat) und Koagulationsnekrose (dunkelgelbes Quadrat) sowie leichte bis mittelschwere perineurale Fibrose und Kollagenablagerung gezeigt werden. Gleichzeitig wird auch der relativ normale Nerv (blaues Quadrat) angezeigt. Semiquantitativer Gesamtwert der Nervenverletzung B und Werte in Regionen innerhalb von C und jenseits von 5 mm D vom Arterienlumen in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. Der zweiseitige P-Wert wurde aus dem Kruskal-Wallis-Test berechnet, gefolgt von allen paarweisen Mehrfachvergleichen. * P < 0,05 vs. Kontrolle. † P < 0,05 vs. 15-Gy-Gruppe. RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Alle radioablativen Läsionen, die in der Tiefe von der Intima bis zur tiefsten Stelle der Gewebeverletzung dargestellt wurden, waren > 10 mm, und SBRT führte im Vergleich zur RFA zu einem tieferen Denervierungsbereich ( P < 0,05). Das Endothel der anvisierten PAs blieb bei allen Versuchspersonen intakt, und bei den mit 20 Gy und 25 Gy ablatierten Tieren wurde gelegentlich eine minimale Neointima beobachtet, die sich auf der inneren elastischen Lamina bildete. Die mediale PA-Verletzung, die sich durch minimalen bis mäßigen Verlust glatter Muskelzellen bei Proteoglykan-Ersatz zeigt, nahm dosisabhängig zu, ohne statistische Signifikanz zu erreichen ( P > 0,05). Die durch minimale bis leichte perivaskuläre Entzündung und Verlust glatter Muskelzellen gekennzeichnete nutritive Arteriolenschädigung war in der 15-Gy-Gruppe geringer als in der RFA- und 25-Gy-Gruppe ( P < 0,05). Darüber hinaus nahm die Schwere der Weichteilverletzungen, die durch denaturiertes Kollagen, Entzündungen, Fettnekrose und Fibrose gekennzeichnet waren, mit zunehmender SBRT-Dosis allmählich zu, und RFA verursachte schwerwiegendere Weichteilverletzungen als SBRT mit 15 Gy und 20 Gy. Die spezifischen Daten und repräsentativen Bilder sind in der Zusatztabelle
3
und Abb.
4
dargestellt .Abb. 4: Repräsentative Bilder des Ablationsbereichs.
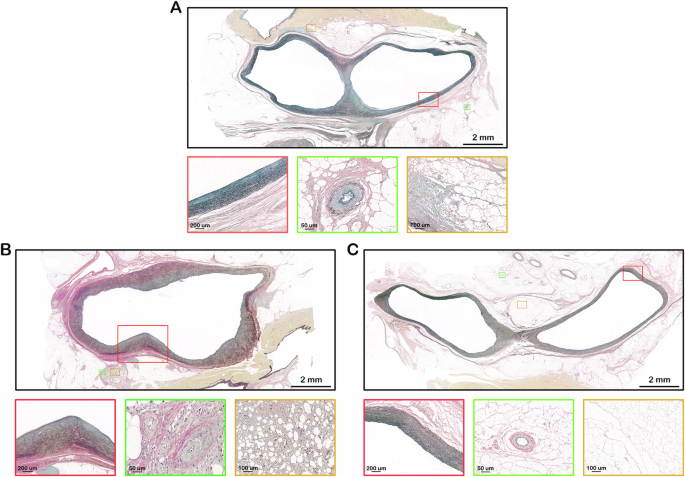 A Das obere Feld zeigt einen mit Movat-Pentachrom gefärbten Bereich einer Lungenarteriengabelung nach stereotaktischer Radioablation mit 20 Gy. Das untere Feld zeigt vergrößerte Mikrofotografien. Dargestellt ist eine mediale Lungenarterienverletzung, die sich durch leichten Verlust glatter Muskelzellen mit Proteoglykan-Ersatz zeigt, der sich grün färbt (rotes Quadrat). Es sind umgebende Nährstoffarteriolenschäden zu beobachten, die durch leichte perivaskuläre Entzündung und Verlust glatter Muskelzellen gekennzeichnet sind (grünes Quadrat). Eine Weichteilverletzung, die durch leichte Entzündung und Fibrose gekennzeichnet ist, ist in einem orangefarbenen Quadrat dargestellt. B Das obere Feld zeigt einen mit Movat-Pentachrom gefärbten Bereich einer Lungenarteriengabelung nach Radiofrequenzablation. Das untere Feld zeigt vergrößerte Mikrofotografien der entsprechenden Verletzungen der Lungenarterie (rotes Quadrat), der Arteriolen (grünes Quadrat) und des Weichteilgewebes (orangefarbenes Quadrat). C Mit Movat-Pentachrom gefärbte Lungenarteriengabelung (schwarzes Quadrat) und vergrößerte Mikrofotografien der Lungenarterie (rotes Quadrat), der Arteriolen (grünes Quadrat) und des Weichgewebes (oranges Quadrat) in der Kontrollgruppe. Jedes Experiment wurde unabhängig voneinander dreimal mit ähnlichen Ergebnissen wiederholt.
Denervierungseffizienz durch immunhistochemischen Test beurteiltDie Tyrosinhydroxylase (TH)-Färbungswerte für Nerven innerhalb der Ablationszone waren in den PADN-Gruppen signifikant niedriger als in den unbehandelten Kontrollgruppen (1,2 ± 0,3 für RFA, 1,4 ± 0,3 für 15 Gy, 1,2 ± 0,3 für 20 Gy, 1,1 ± 0,3 für 25 Gy vs. 2,3 ± 0,4, P < 0,05). Im Gegensatz dazu gab es keine signifikanten Unterschiede zwischen den Behandlungsgruppen ( P > 0,05, Abb. 5A). Es war eine Tendenz zu niedrigeren TH-Werten proximal der 20-Gy- und 25-Gy-Ablationszone erkennbar ( P > 0,05, Abb. 5B). PADN mit 20 Gy und 25 Gy führte zu einer signifikant schwächeren TH-Expression in PA-Abschnitten distal der Zielstelle ( P < 0,05). Im Gegensatz dazu war die Färbeintensität der RFA- und 15-Gy-Gruppe mit den Kontrollgruppen vergleichbar ( P > 0,05, Abb.
5C
). Repräsentative Bilder funktionell beeinträchtigter Nerven nach Immunfärbung sind in Abb.
5D
dargestellt .Abb. 5: Immunhistochemische Analyse der Denervierung.
A Das obere Feld zeigt einen mit Movat-Pentachrom gefärbten Bereich einer Lungenarteriengabelung nach stereotaktischer Radioablation mit 20 Gy. Das untere Feld zeigt vergrößerte Mikrofotografien. Dargestellt ist eine mediale Lungenarterienverletzung, die sich durch leichten Verlust glatter Muskelzellen mit Proteoglykan-Ersatz zeigt, der sich grün färbt (rotes Quadrat). Es sind umgebende Nährstoffarteriolenschäden zu beobachten, die durch leichte perivaskuläre Entzündung und Verlust glatter Muskelzellen gekennzeichnet sind (grünes Quadrat). Eine Weichteilverletzung, die durch leichte Entzündung und Fibrose gekennzeichnet ist, ist in einem orangefarbenen Quadrat dargestellt. B Das obere Feld zeigt einen mit Movat-Pentachrom gefärbten Bereich einer Lungenarteriengabelung nach Radiofrequenzablation. Das untere Feld zeigt vergrößerte Mikrofotografien der entsprechenden Verletzungen der Lungenarterie (rotes Quadrat), der Arteriolen (grünes Quadrat) und des Weichteilgewebes (orangefarbenes Quadrat). C Mit Movat-Pentachrom gefärbte Lungenarteriengabelung (schwarzes Quadrat) und vergrößerte Mikrofotografien der Lungenarterie (rotes Quadrat), der Arteriolen (grünes Quadrat) und des Weichgewebes (oranges Quadrat) in der Kontrollgruppe. Jedes Experiment wurde unabhängig voneinander dreimal mit ähnlichen Ergebnissen wiederholt.
Denervierungseffizienz durch immunhistochemischen Test beurteiltDie Tyrosinhydroxylase (TH)-Färbungswerte für Nerven innerhalb der Ablationszone waren in den PADN-Gruppen signifikant niedriger als in den unbehandelten Kontrollgruppen (1,2 ± 0,3 für RFA, 1,4 ± 0,3 für 15 Gy, 1,2 ± 0,3 für 20 Gy, 1,1 ± 0,3 für 25 Gy vs. 2,3 ± 0,4, P < 0,05). Im Gegensatz dazu gab es keine signifikanten Unterschiede zwischen den Behandlungsgruppen ( P > 0,05, Abb. 5A). Es war eine Tendenz zu niedrigeren TH-Werten proximal der 20-Gy- und 25-Gy-Ablationszone erkennbar ( P > 0,05, Abb. 5B). PADN mit 20 Gy und 25 Gy führte zu einer signifikant schwächeren TH-Expression in PA-Abschnitten distal der Zielstelle ( P < 0,05). Im Gegensatz dazu war die Färbeintensität der RFA- und 15-Gy-Gruppe mit den Kontrollgruppen vergleichbar ( P > 0,05, Abb.
5C
). Repräsentative Bilder funktionell beeinträchtigter Nerven nach Immunfärbung sind in Abb.
5D
dargestellt .Abb. 5: Immunhistochemische Analyse der Denervierung.
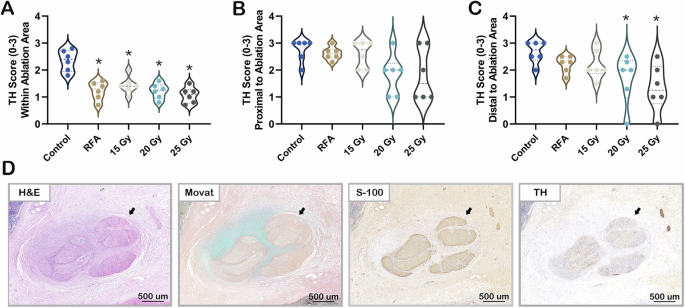 Semiquantitative Bewertungen der Tyrosinhydroxylase (TH)-Färbungsintensität innerhalb A , proximal B und distal C des Ablationsbereichs in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. Der zweiseitige P-Wert wurde aus dem Kruskal-Wallis-Test berechnet, gefolgt von allen paarweisen Mehrfachvergleichen. * P < 0,05 vs. Kontrolle. D Repräsentative Bilder verletzter Nerven (durchgezogener Pfeil) mit Hämatoxylin und Eosin (H&E), Movat-Pentachrom-Färbungen und immunhistochemischen Färbungen gegen S-100 und TH. Eine starke positive Reaktion auf S-100 bestätigt das Vorhandensein von Nervenbündeln, während eine schwache Reaktion auf TH eine funktionelle Nervenschädigung anzeigt. RFA, Radiofrequenzablation. Jedes Experiment wurde unabhängig dreimal mit ähnlichen Ergebnissen wiederholt. Quelldaten werden als Quelldatendatei bereitgestellt.
Auswirkungen der SBRT auf die PA-Umgestaltung und die RAAS-Aktivität im LungengewebeWie in Abb.
6
gezeigt , schienen in kleinen (<100 μm) und mittelgroßen (100 – 300 μm) Lungengefäßen die Verhältnisse von Gefäßwanddicke und -fläche in den RFA-, 15-Gy- und 20-Gy-Gruppen niedriger zu sein, und in der 25-Gy-Gruppe war eine Tendenz zu dickeren Gefäßwänden und größerer Wandfläche zu beobachten. Es gab jedoch keine signifikanten Unterschiede zwischen den Gruppen ( P > 0,05). Obwohl sich außerdem eine ähnliche Tendenz bei den Fluoreszenzdichten und Proteinexpressionen des Angiotensin-II-Typ-1-Rezeptors (AT1R) und des Mineralokortikoid-Rezeptors (MR) im Lungengewebe nahe dem Ablationsbereich zeigte, zeigten die PADN-Gruppen vergleichbare RAAS-Aktivitäten wie die unbehandelten Tiere ( P > 0,05, Abb.
7
).Abb. 6: Auswirkungen der stereotaktischen radioablativen PADN auf die PA-Umgestaltung.
Semiquantitative Bewertungen der Tyrosinhydroxylase (TH)-Färbungsintensität innerhalb A , proximal B und distal C des Ablationsbereichs in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. Der zweiseitige P-Wert wurde aus dem Kruskal-Wallis-Test berechnet, gefolgt von allen paarweisen Mehrfachvergleichen. * P < 0,05 vs. Kontrolle. D Repräsentative Bilder verletzter Nerven (durchgezogener Pfeil) mit Hämatoxylin und Eosin (H&E), Movat-Pentachrom-Färbungen und immunhistochemischen Färbungen gegen S-100 und TH. Eine starke positive Reaktion auf S-100 bestätigt das Vorhandensein von Nervenbündeln, während eine schwache Reaktion auf TH eine funktionelle Nervenschädigung anzeigt. RFA, Radiofrequenzablation. Jedes Experiment wurde unabhängig dreimal mit ähnlichen Ergebnissen wiederholt. Quelldaten werden als Quelldatendatei bereitgestellt.
Auswirkungen der SBRT auf die PA-Umgestaltung und die RAAS-Aktivität im LungengewebeWie in Abb.
6
gezeigt , schienen in kleinen (<100 μm) und mittelgroßen (100 – 300 μm) Lungengefäßen die Verhältnisse von Gefäßwanddicke und -fläche in den RFA-, 15-Gy- und 20-Gy-Gruppen niedriger zu sein, und in der 25-Gy-Gruppe war eine Tendenz zu dickeren Gefäßwänden und größerer Wandfläche zu beobachten. Es gab jedoch keine signifikanten Unterschiede zwischen den Gruppen ( P > 0,05). Obwohl sich außerdem eine ähnliche Tendenz bei den Fluoreszenzdichten und Proteinexpressionen des Angiotensin-II-Typ-1-Rezeptors (AT1R) und des Mineralokortikoid-Rezeptors (MR) im Lungengewebe nahe dem Ablationsbereich zeigte, zeigten die PADN-Gruppen vergleichbare RAAS-Aktivitäten wie die unbehandelten Tiere ( P > 0,05, Abb.
7
).Abb. 6: Auswirkungen der stereotaktischen radioablativen PADN auf die PA-Umgestaltung.
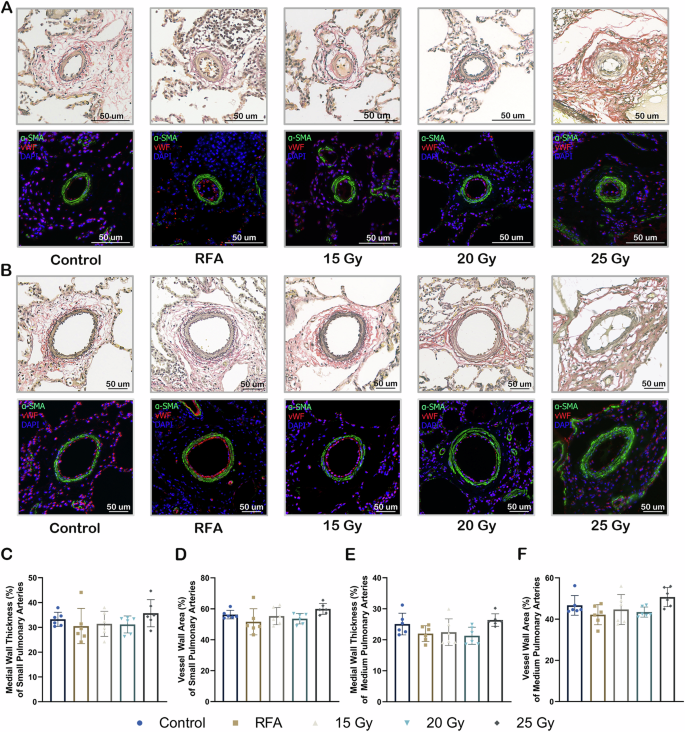 Repräsentative Bilder der Elastic-Van Gieson-Färbung, Immunfluoreszenz-Doppelfärbung gegen von-Willebrand-Faktor (vWF) und α-Glattmuskelaktin (α-SMA) von kleinen (<100 μm) A- und mittleren (100–300 μm) B- PAs. Quantitative Analyse der Gefäßwanddicke und -fläche für kleine C- , D- und mittlere E- , F- PAs in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. PA, Lungenarterie; PADN, Lungenarterien-Denervation; RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Abb. 7: Auswirkungen der stereotaktischen radioablativen PADN auf die RAAS-Aktivität des Lungengewebes.
Repräsentative Bilder der Elastic-Van Gieson-Färbung, Immunfluoreszenz-Doppelfärbung gegen von-Willebrand-Faktor (vWF) und α-Glattmuskelaktin (α-SMA) von kleinen (<100 μm) A- und mittleren (100–300 μm) B- PAs. Quantitative Analyse der Gefäßwanddicke und -fläche für kleine C- , D- und mittlere E- , F- PAs in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. PA, Lungenarterie; PADN, Lungenarterien-Denervation; RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Abb. 7: Auswirkungen der stereotaktischen radioablativen PADN auf die RAAS-Aktivität des Lungengewebes.
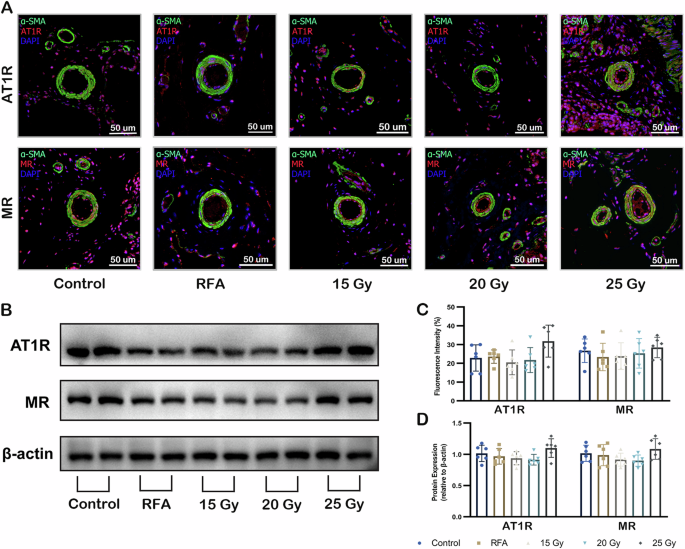 Repräsentative Bilder der Immunfluoreszenz A und des Western Blot B von AT1R und MR im Lungengewebe neben dem Ablationsbereich. Analyse der mittleren relativen Fluoreszenzintensität C und des Proteinausdrucks D von AT1R und MR in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. α-SMA, α-Glattmuskelaktin; AT1R, Angiotensin-II-Typ-1-Rezeptor; MR, Mineralokortikoidrezeptor; PADN, Denervierung der Pulmonalarterie; RAAS, Renin-Angiotensin-Aldosteron-System. RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Behandlungsbedingte NebenwirkungenObwohl an den umliegenden Organen wie Herz, Lunge, Luftröhre, Speiseröhre und Aorta offensichtliche morphologische Verletzungen fehlten, wurden auf Computertomographien (CT) gelegentlich strahlenbedingte Nebenwirkungen beobachtet. Im Vergleich zur Kontrollgruppe waren die PA-Durchmesser des gezielten distalen Bifurkationsbereichs bei den Tieren, die 25 Gy erhielten, kleiner ( P < 0,05), während in den anderen Ablationsgruppen kein signifikanter Unterschied festgestellt wurde ( P > 0,05, Zusatztabelle
4
). Darüber hinaus wurde bei 4 mit 25 Gy behandelten Tieren eine Strahlenpneumonie beobachtet (Abb.
8
). Bis zu 4 Monate nach der SBRT waren keine erkennbaren Schäden an den Koronararterien und den anderen OARs zu sehen.Abb. 8: Terminale Computertomographie (CT)-Auswertung.
Repräsentative Bilder der Immunfluoreszenz A und des Western Blot B von AT1R und MR im Lungengewebe neben dem Ablationsbereich. Analyse der mittleren relativen Fluoreszenzintensität C und des Proteinausdrucks D von AT1R und MR in Kontroll- und Behandlungsgruppen. Werte werden als Mittelwert ± SD ausgedrückt, n = 6 für jede Gruppe. α-SMA, α-Glattmuskelaktin; AT1R, Angiotensin-II-Typ-1-Rezeptor; MR, Mineralokortikoidrezeptor; PADN, Denervierung der Pulmonalarterie; RAAS, Renin-Angiotensin-Aldosteron-System. RFA, Radiofrequenzablation. Quelldaten werden als Quelldatendatei bereitgestellt.
Behandlungsbedingte NebenwirkungenObwohl an den umliegenden Organen wie Herz, Lunge, Luftröhre, Speiseröhre und Aorta offensichtliche morphologische Verletzungen fehlten, wurden auf Computertomographien (CT) gelegentlich strahlenbedingte Nebenwirkungen beobachtet. Im Vergleich zur Kontrollgruppe waren die PA-Durchmesser des gezielten distalen Bifurkationsbereichs bei den Tieren, die 25 Gy erhielten, kleiner ( P < 0,05), während in den anderen Ablationsgruppen kein signifikanter Unterschied festgestellt wurde ( P > 0,05, Zusatztabelle
4
). Darüber hinaus wurde bei 4 mit 25 Gy behandelten Tieren eine Strahlenpneumonie beobachtet (Abb.
8
). Bis zu 4 Monate nach der SBRT waren keine erkennbaren Schäden an den Koronararterien und den anderen OARs zu sehen.Abb. 8: Terminale Computertomographie (CT)-Auswertung.
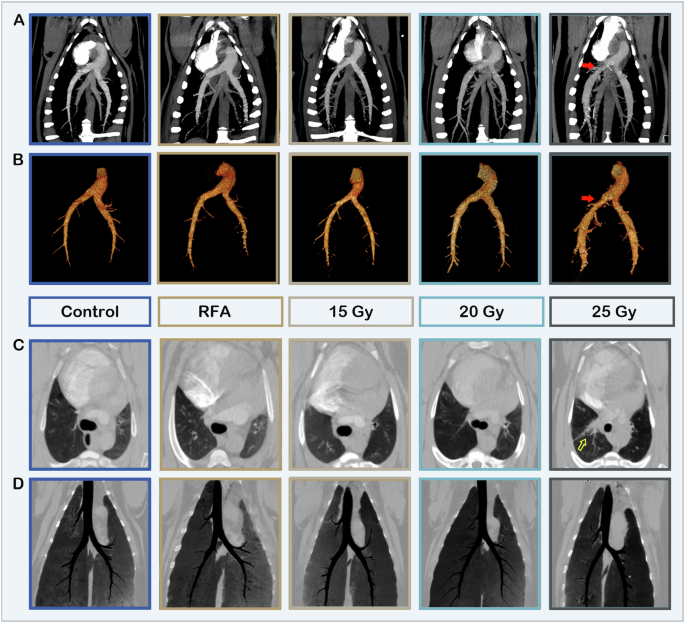 Repräsentative multiplanare Reformation A und Volumenrendering-Bilder B der Lungenarterie, axiale C und multiplanare Reformation D von Lungenbildern am Endpunkt von 4 Monaten in Kontroll- und Behandlungsgruppen. Es werden eine Lungenarterienstenose (durchgezogener Pfeil) in der 25-Gy-Ablationszone und eine Strahlenpneumonie (durchsichtiger Pfeil) gezeigt, während in den anderen Ablationsgruppen kein offensichtlicher Kollateralschaden festgestellt werden kann. RFA, Radiofrequenzablation.
In Übereinstimmung mit den CT-Befunden wurden histopathologische Manifestationen von wahrscheinlich strahlenbedingten Lungenverletzungen, einschließlich verschiedener Grade chronischer Entzündungen, Hyperplasie des interalveolären Lymph- und Bindegewebes, vor allem bei Tieren beobachtet, die mit 25 Gy behandelt wurden (Ergänzende Abbildung
4
). Bei einem Tier, das 25 Gy erhalten hatte, wurde neben dem Ablationsbereich eine fokale Degeneration und Verkalkung des Myokards festgestellt. Es wurden keine offensichtlichen mikroskopischen Hinweise auf Verletzungen der Speiseröhre, der Luftröhre oder der Aorta gefunden (Ergänzende Abbildung
5
).Wirksamkeit von SBRT-basiertem PADN in einem MCT-induzierten chronischen PH-ModellDie hämodynamischen Daten zu drei Zeitpunkten (Woche 0, Woche 6 und Woche 12) der vier Gruppen sind in Tabelle
1
aufgeführt . Die hämodynamischen Basisvariablen waren ähnlich. In der 6. Woche wurde in den PH-Gruppen im Vergleich zur Kontrollgruppe ein Anstieg des mittleren PAP ( P < 0,05) sowie ein Anstieg des systolischen PAP, diastolischen PAP und PVR beobachtet, was zeigte, dass das PH-Modell erfolgreich etabliert wurde. PADN war mit signifikanten Reduktionen des mittleren PAP, des systolischen PAP und diastolischen PAP verbunden, was zu einer signifikanten Reduktion von PVR im Vergleich zur PH-Kontrollgruppe führte ( P < 0,05). Zudem führte SBRT im Vergleich zur RFA zu einer deutlicheren Verbesserung des mittleren PAP, des systolischen PAP und des PVR ( P < 0,05).Tabelle 1 Hämodynamische Veränderungen im chronischen PH-Modell
Obwohl MCT eine starke PA-Umgestaltung induzierte, was sich in dem höheren Prozentsatz medialer Wanddicke und dem niedrigeren Prozentsatz keiner Muskularisierung widerspiegelte, führte PADN zu einer signifikanten Abnahme der vollständigen Muskularisierung und der gesamten medialen Wanddicke im Vergleich zur PH-Kontrollgruppe ( P < 0,05). Darüber hinaus führte PADN durch 20-Gy-SBRT zu einer signifikanteren Verringerung der medialen Wanddicke ( P < 0,05) und zeigte eine Tendenz zu einer niedrigeren Rate vollständiger Muskularisierung als RFA (Abb.
9
).Abb. 9: Chronische PA-Umgestaltung.
Repräsentative multiplanare Reformation A und Volumenrendering-Bilder B der Lungenarterie, axiale C und multiplanare Reformation D von Lungenbildern am Endpunkt von 4 Monaten in Kontroll- und Behandlungsgruppen. Es werden eine Lungenarterienstenose (durchgezogener Pfeil) in der 25-Gy-Ablationszone und eine Strahlenpneumonie (durchsichtiger Pfeil) gezeigt, während in den anderen Ablationsgruppen kein offensichtlicher Kollateralschaden festgestellt werden kann. RFA, Radiofrequenzablation.
In Übereinstimmung mit den CT-Befunden wurden histopathologische Manifestationen von wahrscheinlich strahlenbedingten Lungenverletzungen, einschließlich verschiedener Grade chronischer Entzündungen, Hyperplasie des interalveolären Lymph- und Bindegewebes, vor allem bei Tieren beobachtet, die mit 25 Gy behandelt wurden (Ergänzende Abbildung
4
). Bei einem Tier, das 25 Gy erhalten hatte, wurde neben dem Ablationsbereich eine fokale Degeneration und Verkalkung des Myokards festgestellt. Es wurden keine offensichtlichen mikroskopischen Hinweise auf Verletzungen der Speiseröhre, der Luftröhre oder der Aorta gefunden (Ergänzende Abbildung
5
).Wirksamkeit von SBRT-basiertem PADN in einem MCT-induzierten chronischen PH-ModellDie hämodynamischen Daten zu drei Zeitpunkten (Woche 0, Woche 6 und Woche 12) der vier Gruppen sind in Tabelle
1
aufgeführt . Die hämodynamischen Basisvariablen waren ähnlich. In der 6. Woche wurde in den PH-Gruppen im Vergleich zur Kontrollgruppe ein Anstieg des mittleren PAP ( P < 0,05) sowie ein Anstieg des systolischen PAP, diastolischen PAP und PVR beobachtet, was zeigte, dass das PH-Modell erfolgreich etabliert wurde. PADN war mit signifikanten Reduktionen des mittleren PAP, des systolischen PAP und diastolischen PAP verbunden, was zu einer signifikanten Reduktion von PVR im Vergleich zur PH-Kontrollgruppe führte ( P < 0,05). Zudem führte SBRT im Vergleich zur RFA zu einer deutlicheren Verbesserung des mittleren PAP, des systolischen PAP und des PVR ( P < 0,05).Tabelle 1 Hämodynamische Veränderungen im chronischen PH-Modell
Obwohl MCT eine starke PA-Umgestaltung induzierte, was sich in dem höheren Prozentsatz medialer Wanddicke und dem niedrigeren Prozentsatz keiner Muskularisierung widerspiegelte, führte PADN zu einer signifikanten Abnahme der vollständigen Muskularisierung und der gesamten medialen Wanddicke im Vergleich zur PH-Kontrollgruppe ( P < 0,05). Darüber hinaus führte PADN durch 20-Gy-SBRT zu einer signifikanteren Verringerung der medialen Wanddicke ( P < 0,05) und zeigte eine Tendenz zu einer niedrigeren Rate vollständiger Muskularisierung als RFA (Abb.
9
).Abb. 9: Chronische PA-Umgestaltung.
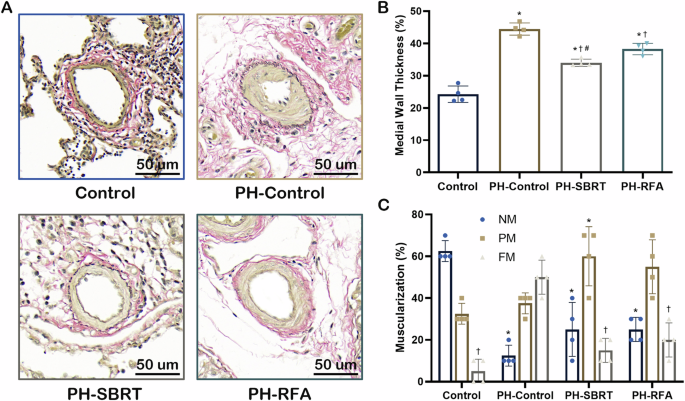 A Repräsentative Bilder der PA-Muskularisierung durch Elastic-Van-Gieson-Färbung. B Quantitative Analyse der Gefäßwanddicke und C Prozentsatz der PA-Muskularisierung. Werte werden als Mittelwert ± SD ausgedrückt, n = 4 für jede Gruppe. Zweiseitiger P-Wert wurde aus einfaktorieller ANOVA mit Bonferroni-Post-hoc-Analyse berechnet. * P < 0,05 vs. Kontrollgruppe. † P < 0,05 vs. PH-Kontrollgruppe. # P < 0,05 vs. PH-RFA-Gruppe. FM vollständige Muskularisierung, NM keine Muskularisierung, PA Lungenarterie, PH Lungenhypertonie, PM partielle Muskularisierung, RFA Radiofrequenzablation, SBRT stereotaktische Körperbestrahlung. Quelldaten werden als Quelldatendatei bereitgestellt.
DiskussionPADN durch intravaskuläre Radiofrequenz oder Ultraschall hat sich nach und nach als neue Intervention zur Behandlung der pulmonalen arteriellen Hypertonie und anderer PH-Subtypen etabliert
5
,
8
,
9
,
17
,
22
,
23
,
24
,
25.
Nach bestem Wissen und Gewissen ist dies die erste systemische Studie zur Bewertung der funktionellen, anatomischen und histopathologischen Leistung einer externen Photostrahltherapie bei PADN. Die wichtigsten Erkenntnisse sind: (1) PADN durch SBRT unter Anwendung einer geeigneten Strahlendosis und eines entsprechenden Behandlungsplans konnte ein Gleichgewicht zwischen Wirksamkeit und Sicherheit zur Zerstörung der PA-Nerven und Unterdrückung der sympathischen Aktivität herstellen und so den Anstieg des mittleren PAP in einem akuten Schweine-PH-Modell verhindern; (2) Im MCT-induzierten Modell der chronischen PH führte PADN durch 20-Gy-SBRT im Vergleich zur RFA zu einer stärkeren Verbesserung der pulmonalen Hämodynamik und der PA-Umgestaltung.Das Lungengefäßsystem ist stark innerviert und setzt > 40 % der zirkulierenden Katecholamine frei und verstoffwechselt
26.
In den letzten Jahrzehnten haben zahlreiche Belege gezeigt, dass eine sympathische Überaktivierung und ihre direkten Auswirkungen auf die PA-Vasokonstriktion eine entscheidende Rolle bei der Pathogenese von PH spielen
3
,
4.
Barorezeptorstrukturen wurden in oder in der Nähe der Hauptbifurkation des PA beschrieben, und der efferente Ast des vasokonstriktiven Barorezeptorreflexes wird vorwiegend durch den sympathischen Tonus vermittelt
27.
Die vorliegende Studie hat bestätigt, dass PADN durch nichtinvasive SBRT mit 20 Gy, die auf die Bifurkation des Hauptstamms des PA abzielt, die Lungenhämodynamik verbessern kann, wie eine Verringerung des maximalen mittleren PAP durch TxA2 und eine Abnahme des mittleren PAP und PVR bei Tieren mit chronischer PH gezeigt hat. Die Wirksamkeit dieser Technik wurde auch durch offensichtliche histologische Nervenschäden und eine deutliche Verringerung der TH-Färbung bestätigt. Wie bereits in der Literatur über Strahlenschäden an peripheren Nerven nach intraoperativer Strahlentherapie berichtet, nahm die Häufigkeit von Neuropathie mit steigender Dosis ab 15 Gy zu
28.
Obwohl 15 Gy in unserer Studie relativ leichte morphologische Veränderungen verursachten, beeinträchtigten sie die NE-Synthese der Nerven in der Ablationszone. Trotzdem blieben die zirkulierenden NE-Konzentrationen im Plasma nach PADN durch Verabreichung vorab festgelegter Strahlendosen unverändert. Dies lässt sich möglicherweise dadurch erklären, dass Plasmakatecholamine von der neuronalen Freisetzung, Wiederaufnahme, dem Stoffwechsel und der Clearance beeinflusst werden und daher unempfindliche Marker für den sympathischen Nervenausfluss sind
29
.Bisher zeigten begrenzte Daten, dass die menschlichen PAs vorwiegend durch sympathische Nerven innerviert werden, die sich auf die Bifurkation konzentrieren, wobei > 40 % der Nerven in einer Tiefe von > 4 mm liegen und dem arteriellen Verlauf distal folgen
13
,
14.
Aufgrund der durchschnittlichen Eindringtiefe von 3–4 mm
30
verursachte transluminale Radiofrequenzenergie begrenzte histologische Schäden an Nerven um dickwandigere PAs und erzeugte unvollständige PADN
15
,
16.
Die vorliegende Studie zeigt eine radioablative Läsionstiefe von bis zu über 10 mm und deckt damit die große Mehrheit der Nerven ab. Darüber hinaus deuten bemerkenswerte Nervenverletzungen in den Regionen innerhalb und jenseits der 5-mm-Isodoselinie des Planungszielvolumens durch eine Strahlung von ≥ 20 Gy auf eine ausreichende Denervierung hin.Die chronische Aktivierung des RAAS bei PH-Patienten ist gut beschrieben. Eine sympathische Überaktivierung kann durch Modulation der RAAS-Aktivität eine abnorme Vasokonstriktion, Zellproliferation und -migration sowie Fibrose fördern, was zu einer Umgestaltung der Lungengefäße führt
31.
In Studien zu chronischer PH wurde gezeigt, dass PADN die lokale und systemische RAAS-Aktivität herunterreguliert und dann die PA-Umgestaltung abschwächt
13
,
32.
Allerdings wurde PH im TxA2-Modell durch eine akute Vasokonstriktion und nicht durch fortschreitende Umgestaltung der Lungengefäße induziert, deren Parameter wie Plasma-RAAS-Spiegel, Expression von lokalem AT1R und MR und Grad der PA-Muskularisierung nach PADN von 15 Gy oder 20 Gy konstant blieben. Im Modell der chronischen PH kehrte PADN die PA-Umgestaltung um, und SBRT-basiertes PADN induzierte weniger Gefäßmuskularisierung als RFA, was mit einer stärkeren Verbesserung der Lungenhämodynamik übereinstimmt. Dies lässt sich möglicherweise dadurch erklären, dass die SBRT zu einem tieferen Denervierungsbereich führte und damit die überwiegende Mehrheit der Nerven erreichte. Eine weitere mögliche Erklärung hierfür ist, dass eine niedrig dosierte Strahlentherapie die proliferierenden Zellen verringern und nachteilige Umbauprozesse abschwächen kann
33
.Trotz einer effizienteren Denervierung durch höhere Dosen muss beachtet werden, dass eine übermäßige Bestrahlung der Lunge zu einer Umgestaltung der Lungengefäße mit anschließender PH führen kann. Dies ist von zahlreichen Variablen abhängig, einschließlich Bestrahlungsvolumen, Dosis, Dosisleistung und jeweiliger Bestrahlungstechnik
34.
Obwohl es für SBRT nicht gut dokumentiert ist, wurden vaskuläre Komplikationen nach kranialer Radiochirurgie bereits bei so geringen Dosen wie 25 Gy dokumentiert
35
, und die Gefäßumgestaltung war trotz niedrigerer Strahlungsdosen mit zunehmendem Bestrahlungsvolumen ausgeprägter
34.
In Übereinstimmung mit der Literatur fand diese Studie heraus, dass die direkten Effekte der Bestrahlung bei 25 Gy durch Aufhebung des Nutzens der PADN eine Tendenz zur Hochregulierung der Expression von AT1R und MR sowie zur PA-Umgestaltung in den Lungen neben der Ablationszone zeigten, was eine mögliche Erklärung für die neutrale Wirkung auf die Lungenhämodynamik während der TxA2-Exposition nach PADN mit 25 Gy liefert.Bislang gibt es kaum Daten zur Toxizität von hochdosierter Strahlung im begrenzten Bereich der PA. Tierexperimente zur intraoperativen Strahlentherapie zeigen, dass die großen Gefäße bis zu 30 Gy ohne erkennbare Komplikationen wie Thrombose, fibrotische Okklusion und Aneurysmabildung vertragen
28
. In dieser Untersuchung wurden jedoch dosisabhängige Intimahyperplasie der PA, Verletzungen der Mittelwand und insbesondere verringerte Durchmesser der Ziel-PAs in der 25-Gy-Gruppe beobachtet, was darauf hindeutet, dass die Toleranzgrenze für die PA niedriger zu sein scheint als erwartet. Eine mögliche Erklärung dafür könnte sein, dass die PA aufgrund ihrer dünneren Wand als die Aorta relativ anfällig für hypofraktionierte hohe Dosen ist. Trotzdem weist das größere Kaliber der menschlichen PA im Vergleich zu dem des Schweins wahrscheinlich eine etwas höhere Toleranz gegenüber schweren Komplikationen auf.Strahlenpneumonie ist ein in aktuellen Forschungsarbeiten beobachteter häufiger Kollateralschaden und ist bei der Durchführung einer SBRT bei PADN besonders besorgniserregend. Frühere Arbeiten über die Verträglichkeit von Thoraxgewebe gegenüber einer intraoperativen Einzelfraktion-Hochdosis-Strahlentherapie haben gezeigt, dass Dosen bis zu 20 Gy gut vertragen werden, während 30 Gy oder mehr zu erheblichen Schäden führten
36.
Die erhöhte Inzidenz von Strahlenpneumonie bei den in dieser Studie mit 25 Gy behandelten Tieren bestätigt diese früheren Ergebnisse. Anhand der Dosis und des Gesamtvolumens kritischer normaler Strukturen, die Strahlung erhalten, lässt sich die potenzielle Wahrscheinlichkeit einer Toxizität vorhersagen. In dieser Studie lagen die Maximaldosis und das Volumen der Ziel-PA und der umgebenden Organe in den 15-Gy- und 20-Gy-Gruppen alle unterhalb der Toleranzgrenzen für SBRT
37
, und das Sicherheitsprofil wurde durch CT-Scan, Autopsie und histologische Untersuchung bestätigt. Zudem ist in einer gepoolten Analyse von 88 klinischen Studien die Gesamtrate strahleninduzierter Lungentoxizität nach thorakaler SBRT relativ niedrig
38
. Daher könnte man die Hypothese aufstellen, dass die Sicherheit mit 15 bis 20 Gy hätte erreicht werden können, ohne die Wirksamkeit der Denervierung zu beeinträchtigen, da der prozentuale Volumenanteil bilateraler Lungen, die 20 Gy erhalten, der als wichtiger Parameter zur Vorhersage schwerer Strahlenpneumonie und frühen Todes bei SBRT zur Behandlung von Thoraxtumoren gilt
39
, mit dieser neuen Technik für PADN beim Menschen auf ein sicheres Niveau begrenzt werden kann. Zudem ist es wahrscheinlich, dass durch ungenaues Zielen Kollateralverletzungen entstehen. Daher sollte Verfahrensdetails wie Zielabgrenzung, Bewegungskompensation durch Atemgating oder Verfolgung und Ausrichtung mehr Aufmerksamkeit gewidmet werden, um Genauigkeit zu gewährleisten. Ungeachtet des akzeptablen Nutzen-Risiko-Verhältnisses ist die mediastinale, zentrale und ultrazentrale Lungen-SBRT einer der Bereiche mit dem höchsten Risiko für eine Strahlenbehandlung. Bevor man vorsichtig mit der klinischen Anwendung fortfahren kann, müssen weitere Daten erhoben werden.PH ist eine tödliche Erkrankung mit schlechter Prognose und hoher Mortalität. Zur Behandlung von PH werden kontinuierlich verschiedene invasive Strategien zur Modulation des autonomen Nervensystems untersucht. Es wurde berichtet, dass eine versehentliche niedrig dosierte Bestrahlung der Hauptstämme der PA den erhöhten pulmonalarteriellen Widerstand eines idiopathischen PH-Patienten umkehrte, bei dem zunächst fälschlicherweise Lungenkrebs oder Lymphom diagnostiziert worden war. Daher kann die Hypothese aufgestellt werden, dass die Verringerung sympathischer efferenter Signale durch niedrig dosierte Strahlung zur Verringerung des PVR beigetragen haben könnte
40.
Mit der Verbesserung der Strahlentherapietechniken kann die nichtinvasive SBRT in Zukunft eine genaue und effiziente PADN ermöglichen und stellt somit eine vielversprechende Behandlungsoption für PH-Patienten dar. Angesichts der Möglichkeit einer sekundären Malignität sollte die Anwendung dieser Strategie bei jungen PH-Patienten jedoch sorgfältig gegen Nutzen und potenzielle Schäden abgewogen werden.Unsere Studie hat mehrere Einschränkungen. Erstens sollte diese Pilotstudie die Durchführbarkeit von SBRT als neuartige Strategie für PADN untersuchen. Die in den Schweinemodellen nachgewiesene verbesserte Hämodynamik kann nicht direkt auf den Menschen übertragen werden. Zweitens wurden die hämodynamischen Messungen unter Narkose durchgeführt, was den sympathischen Tonus verändern könnte. Drittens sind Anatomie und Position der OARs um die Ablationszone herum unterschiedlich, obwohl Schweine ein ähnliches Herz-Kreislauf-System wie Menschen haben. Gleichzeitig ist es möglich, dass pathologische PAs und Nerven bei PH-Patienten anders auf die Radioablation reagieren. Schließlich wurden die langfristigen Auswirkungen der Bestrahlung auf das Zielgewebe und das umliegende Gewebe nicht untersucht.Zusammenfassend zeigt unsere Machbarkeitsstudie, dass SBRT bei Anwendung eines geeigneten Schemas die sympathische Innervation der PAs nichtinvasiv beeinträchtigen kann, was zu einer anschließenden Verbesserung der pulmonalen Hämodynamik sowohl bei akuter Vasokonstriktion als auch bei chronischer MCT-induzierter PH bei Schweinen führt. Zielausrichtung (d. h. das erforderliche Volumen, das zum gewünschten Effekt führt, Bewegungskompensation), optimale Dosierung sowie langfristige Wirksamkeit und Sicherheit müssen vor der klinischen Umsetzung weiter untersucht werden.
A Repräsentative Bilder der PA-Muskularisierung durch Elastic-Van-Gieson-Färbung. B Quantitative Analyse der Gefäßwanddicke und C Prozentsatz der PA-Muskularisierung. Werte werden als Mittelwert ± SD ausgedrückt, n = 4 für jede Gruppe. Zweiseitiger P-Wert wurde aus einfaktorieller ANOVA mit Bonferroni-Post-hoc-Analyse berechnet. * P < 0,05 vs. Kontrollgruppe. † P < 0,05 vs. PH-Kontrollgruppe. # P < 0,05 vs. PH-RFA-Gruppe. FM vollständige Muskularisierung, NM keine Muskularisierung, PA Lungenarterie, PH Lungenhypertonie, PM partielle Muskularisierung, RFA Radiofrequenzablation, SBRT stereotaktische Körperbestrahlung. Quelldaten werden als Quelldatendatei bereitgestellt.
DiskussionPADN durch intravaskuläre Radiofrequenz oder Ultraschall hat sich nach und nach als neue Intervention zur Behandlung der pulmonalen arteriellen Hypertonie und anderer PH-Subtypen etabliert
5
,
8
,
9
,
17
,
22
,
23
,
24
,
25.
Nach bestem Wissen und Gewissen ist dies die erste systemische Studie zur Bewertung der funktionellen, anatomischen und histopathologischen Leistung einer externen Photostrahltherapie bei PADN. Die wichtigsten Erkenntnisse sind: (1) PADN durch SBRT unter Anwendung einer geeigneten Strahlendosis und eines entsprechenden Behandlungsplans konnte ein Gleichgewicht zwischen Wirksamkeit und Sicherheit zur Zerstörung der PA-Nerven und Unterdrückung der sympathischen Aktivität herstellen und so den Anstieg des mittleren PAP in einem akuten Schweine-PH-Modell verhindern; (2) Im MCT-induzierten Modell der chronischen PH führte PADN durch 20-Gy-SBRT im Vergleich zur RFA zu einer stärkeren Verbesserung der pulmonalen Hämodynamik und der PA-Umgestaltung.Das Lungengefäßsystem ist stark innerviert und setzt > 40 % der zirkulierenden Katecholamine frei und verstoffwechselt
26.
In den letzten Jahrzehnten haben zahlreiche Belege gezeigt, dass eine sympathische Überaktivierung und ihre direkten Auswirkungen auf die PA-Vasokonstriktion eine entscheidende Rolle bei der Pathogenese von PH spielen
3
,
4.
Barorezeptorstrukturen wurden in oder in der Nähe der Hauptbifurkation des PA beschrieben, und der efferente Ast des vasokonstriktiven Barorezeptorreflexes wird vorwiegend durch den sympathischen Tonus vermittelt
27.
Die vorliegende Studie hat bestätigt, dass PADN durch nichtinvasive SBRT mit 20 Gy, die auf die Bifurkation des Hauptstamms des PA abzielt, die Lungenhämodynamik verbessern kann, wie eine Verringerung des maximalen mittleren PAP durch TxA2 und eine Abnahme des mittleren PAP und PVR bei Tieren mit chronischer PH gezeigt hat. Die Wirksamkeit dieser Technik wurde auch durch offensichtliche histologische Nervenschäden und eine deutliche Verringerung der TH-Färbung bestätigt. Wie bereits in der Literatur über Strahlenschäden an peripheren Nerven nach intraoperativer Strahlentherapie berichtet, nahm die Häufigkeit von Neuropathie mit steigender Dosis ab 15 Gy zu
28.
Obwohl 15 Gy in unserer Studie relativ leichte morphologische Veränderungen verursachten, beeinträchtigten sie die NE-Synthese der Nerven in der Ablationszone. Trotzdem blieben die zirkulierenden NE-Konzentrationen im Plasma nach PADN durch Verabreichung vorab festgelegter Strahlendosen unverändert. Dies lässt sich möglicherweise dadurch erklären, dass Plasmakatecholamine von der neuronalen Freisetzung, Wiederaufnahme, dem Stoffwechsel und der Clearance beeinflusst werden und daher unempfindliche Marker für den sympathischen Nervenausfluss sind
29
.Bisher zeigten begrenzte Daten, dass die menschlichen PAs vorwiegend durch sympathische Nerven innerviert werden, die sich auf die Bifurkation konzentrieren, wobei > 40 % der Nerven in einer Tiefe von > 4 mm liegen und dem arteriellen Verlauf distal folgen
13
,
14.
Aufgrund der durchschnittlichen Eindringtiefe von 3–4 mm
30
verursachte transluminale Radiofrequenzenergie begrenzte histologische Schäden an Nerven um dickwandigere PAs und erzeugte unvollständige PADN
15
,
16.
Die vorliegende Studie zeigt eine radioablative Läsionstiefe von bis zu über 10 mm und deckt damit die große Mehrheit der Nerven ab. Darüber hinaus deuten bemerkenswerte Nervenverletzungen in den Regionen innerhalb und jenseits der 5-mm-Isodoselinie des Planungszielvolumens durch eine Strahlung von ≥ 20 Gy auf eine ausreichende Denervierung hin.Die chronische Aktivierung des RAAS bei PH-Patienten ist gut beschrieben. Eine sympathische Überaktivierung kann durch Modulation der RAAS-Aktivität eine abnorme Vasokonstriktion, Zellproliferation und -migration sowie Fibrose fördern, was zu einer Umgestaltung der Lungengefäße führt
31.
In Studien zu chronischer PH wurde gezeigt, dass PADN die lokale und systemische RAAS-Aktivität herunterreguliert und dann die PA-Umgestaltung abschwächt
13
,
32.
Allerdings wurde PH im TxA2-Modell durch eine akute Vasokonstriktion und nicht durch fortschreitende Umgestaltung der Lungengefäße induziert, deren Parameter wie Plasma-RAAS-Spiegel, Expression von lokalem AT1R und MR und Grad der PA-Muskularisierung nach PADN von 15 Gy oder 20 Gy konstant blieben. Im Modell der chronischen PH kehrte PADN die PA-Umgestaltung um, und SBRT-basiertes PADN induzierte weniger Gefäßmuskularisierung als RFA, was mit einer stärkeren Verbesserung der Lungenhämodynamik übereinstimmt. Dies lässt sich möglicherweise dadurch erklären, dass die SBRT zu einem tieferen Denervierungsbereich führte und damit die überwiegende Mehrheit der Nerven erreichte. Eine weitere mögliche Erklärung hierfür ist, dass eine niedrig dosierte Strahlentherapie die proliferierenden Zellen verringern und nachteilige Umbauprozesse abschwächen kann
33
.Trotz einer effizienteren Denervierung durch höhere Dosen muss beachtet werden, dass eine übermäßige Bestrahlung der Lunge zu einer Umgestaltung der Lungengefäße mit anschließender PH führen kann. Dies ist von zahlreichen Variablen abhängig, einschließlich Bestrahlungsvolumen, Dosis, Dosisleistung und jeweiliger Bestrahlungstechnik
34.
Obwohl es für SBRT nicht gut dokumentiert ist, wurden vaskuläre Komplikationen nach kranialer Radiochirurgie bereits bei so geringen Dosen wie 25 Gy dokumentiert
35
, und die Gefäßumgestaltung war trotz niedrigerer Strahlungsdosen mit zunehmendem Bestrahlungsvolumen ausgeprägter
34.
In Übereinstimmung mit der Literatur fand diese Studie heraus, dass die direkten Effekte der Bestrahlung bei 25 Gy durch Aufhebung des Nutzens der PADN eine Tendenz zur Hochregulierung der Expression von AT1R und MR sowie zur PA-Umgestaltung in den Lungen neben der Ablationszone zeigten, was eine mögliche Erklärung für die neutrale Wirkung auf die Lungenhämodynamik während der TxA2-Exposition nach PADN mit 25 Gy liefert.Bislang gibt es kaum Daten zur Toxizität von hochdosierter Strahlung im begrenzten Bereich der PA. Tierexperimente zur intraoperativen Strahlentherapie zeigen, dass die großen Gefäße bis zu 30 Gy ohne erkennbare Komplikationen wie Thrombose, fibrotische Okklusion und Aneurysmabildung vertragen
28
. In dieser Untersuchung wurden jedoch dosisabhängige Intimahyperplasie der PA, Verletzungen der Mittelwand und insbesondere verringerte Durchmesser der Ziel-PAs in der 25-Gy-Gruppe beobachtet, was darauf hindeutet, dass die Toleranzgrenze für die PA niedriger zu sein scheint als erwartet. Eine mögliche Erklärung dafür könnte sein, dass die PA aufgrund ihrer dünneren Wand als die Aorta relativ anfällig für hypofraktionierte hohe Dosen ist. Trotzdem weist das größere Kaliber der menschlichen PA im Vergleich zu dem des Schweins wahrscheinlich eine etwas höhere Toleranz gegenüber schweren Komplikationen auf.Strahlenpneumonie ist ein in aktuellen Forschungsarbeiten beobachteter häufiger Kollateralschaden und ist bei der Durchführung einer SBRT bei PADN besonders besorgniserregend. Frühere Arbeiten über die Verträglichkeit von Thoraxgewebe gegenüber einer intraoperativen Einzelfraktion-Hochdosis-Strahlentherapie haben gezeigt, dass Dosen bis zu 20 Gy gut vertragen werden, während 30 Gy oder mehr zu erheblichen Schäden führten
36.
Die erhöhte Inzidenz von Strahlenpneumonie bei den in dieser Studie mit 25 Gy behandelten Tieren bestätigt diese früheren Ergebnisse. Anhand der Dosis und des Gesamtvolumens kritischer normaler Strukturen, die Strahlung erhalten, lässt sich die potenzielle Wahrscheinlichkeit einer Toxizität vorhersagen. In dieser Studie lagen die Maximaldosis und das Volumen der Ziel-PA und der umgebenden Organe in den 15-Gy- und 20-Gy-Gruppen alle unterhalb der Toleranzgrenzen für SBRT
37
, und das Sicherheitsprofil wurde durch CT-Scan, Autopsie und histologische Untersuchung bestätigt. Zudem ist in einer gepoolten Analyse von 88 klinischen Studien die Gesamtrate strahleninduzierter Lungentoxizität nach thorakaler SBRT relativ niedrig
38
. Daher könnte man die Hypothese aufstellen, dass die Sicherheit mit 15 bis 20 Gy hätte erreicht werden können, ohne die Wirksamkeit der Denervierung zu beeinträchtigen, da der prozentuale Volumenanteil bilateraler Lungen, die 20 Gy erhalten, der als wichtiger Parameter zur Vorhersage schwerer Strahlenpneumonie und frühen Todes bei SBRT zur Behandlung von Thoraxtumoren gilt
39
, mit dieser neuen Technik für PADN beim Menschen auf ein sicheres Niveau begrenzt werden kann. Zudem ist es wahrscheinlich, dass durch ungenaues Zielen Kollateralverletzungen entstehen. Daher sollte Verfahrensdetails wie Zielabgrenzung, Bewegungskompensation durch Atemgating oder Verfolgung und Ausrichtung mehr Aufmerksamkeit gewidmet werden, um Genauigkeit zu gewährleisten. Ungeachtet des akzeptablen Nutzen-Risiko-Verhältnisses ist die mediastinale, zentrale und ultrazentrale Lungen-SBRT einer der Bereiche mit dem höchsten Risiko für eine Strahlenbehandlung. Bevor man vorsichtig mit der klinischen Anwendung fortfahren kann, müssen weitere Daten erhoben werden.PH ist eine tödliche Erkrankung mit schlechter Prognose und hoher Mortalität. Zur Behandlung von PH werden kontinuierlich verschiedene invasive Strategien zur Modulation des autonomen Nervensystems untersucht. Es wurde berichtet, dass eine versehentliche niedrig dosierte Bestrahlung der Hauptstämme der PA den erhöhten pulmonalarteriellen Widerstand eines idiopathischen PH-Patienten umkehrte, bei dem zunächst fälschlicherweise Lungenkrebs oder Lymphom diagnostiziert worden war. Daher kann die Hypothese aufgestellt werden, dass die Verringerung sympathischer efferenter Signale durch niedrig dosierte Strahlung zur Verringerung des PVR beigetragen haben könnte
40.
Mit der Verbesserung der Strahlentherapietechniken kann die nichtinvasive SBRT in Zukunft eine genaue und effiziente PADN ermöglichen und stellt somit eine vielversprechende Behandlungsoption für PH-Patienten dar. Angesichts der Möglichkeit einer sekundären Malignität sollte die Anwendung dieser Strategie bei jungen PH-Patienten jedoch sorgfältig gegen Nutzen und potenzielle Schäden abgewogen werden.Unsere Studie hat mehrere Einschränkungen. Erstens sollte diese Pilotstudie die Durchführbarkeit von SBRT als neuartige Strategie für PADN untersuchen. Die in den Schweinemodellen nachgewiesene verbesserte Hämodynamik kann nicht direkt auf den Menschen übertragen werden. Zweitens wurden die hämodynamischen Messungen unter Narkose durchgeführt, was den sympathischen Tonus verändern könnte. Drittens sind Anatomie und Position der OARs um die Ablationszone herum unterschiedlich, obwohl Schweine ein ähnliches Herz-Kreislauf-System wie Menschen haben. Gleichzeitig ist es möglich, dass pathologische PAs und Nerven bei PH-Patienten anders auf die Radioablation reagieren. Schließlich wurden die langfristigen Auswirkungen der Bestrahlung auf das Zielgewebe und das umliegende Gewebe nicht untersucht.Zusammenfassend zeigt unsere Machbarkeitsstudie, dass SBRT bei Anwendung eines geeigneten Schemas die sympathische Innervation der PAs nichtinvasiv beeinträchtigen kann, was zu einer anschließenden Verbesserung der pulmonalen Hämodynamik sowohl bei akuter Vasokonstriktion als auch bei chronischer MCT-induzierter PH bei Schweinen führt. Zielausrichtung (d. h. das erforderliche Volumen, das zum gewünschten Effekt führt, Bewegungskompensation), optimale Dosierung sowie langfristige Wirksamkeit und Sicherheit müssen vor der klinischen Umsetzung weiter untersucht werden.
www.nature.com/articles/s41467-025-55933-8AbstraktDie katheterbasierte pulmonalarterielle Denervierung (PADN) hat vielversprechende Ergebnisse bei der Behandlung von pulmonaler Hypertonie (PH) erzielt. Wir präsentieren hier die stereotaktische Körperradiotherapie (SBRT) als neuen nichtinvasiven Ansatz für PADN. Eine einzelne Fraktion von 15 Gy, 20 Gy oder 25 Gy wurde für PADN in einem durch Thromboxan A2 (TxA2) induzierten Schweinemodell für akute PH verabreicht. Wir haben gezeigt, dass PADN durch 20-Gy-SBRT den mittleren pulmonalarteriellen Druck (PA) während der TxA2-Herausforderung senkte. Alle SBRT-Dosierungen führten im Vergleich zur Radiofrequenzablation (RFA) zu einem tieferen Denervierungsbereich und verringerten die sympathische neurale Noradrenalinsynthese in der Ablationszone. Mögliche strahlungsbedingte Nebenwirkungen wurden hauptsächlich bei Tieren festgestellt, die mit 25 Gy behandelt wurden. Bei Tieren mit nachfolgender, durch Monocrotalin induzierter chronischer PH führte PADN durch 20-Gy-SBRT zu einer signifikanteren Verbesserung der pulmonalen Hämodynamik und der PA-Umgestaltung im Vergleich zur RFA. Zusammenfassend deuten unsere Ergebnisse darauf hin, dass ein geeignetes SBRT-Schema die Wirksamkeit und Sicherheit bei PADN ausbalancieren könnte, was eine neuartige Strategie zur Behandlung von PH darstellen könnte.
EinführungPulmonale Hypertonie (PH) ist eine fortschreitende Erkrankung, die durch einen erhöhten pulmonalvaskulären Widerstand (PVR) und pulmonalarteriellen Druck gekennzeichnet ist und anschließend zu Rechtsherzversagen und letztendlich zum Tod führt. Trotz deutlicher Fortschritte in der medikamentösen Behandlung leiden PH-Patienten nach wie vor unter einer hohen Symptomlast und haben eine schlechte Langzeitprognose 1 , 2. Umfangreiche Forschungsarbeiten haben gezeigt, dass eine Überaktivierung des sympathischen Nervensystems und die anschließende Vasokonstriktion und Umgestaltung der PA eine entscheidende Rolle bei der Pathogenese von PH spielen 3 , 4. Die PA-Denervierung (PADN), eine innovative Therapie, bei der meist eine katheterbasierte Radiofrequenzablation (RFA) eingesetzt wird, um Barorezeptoren oder sympathische Nervenfasern im Bereich der Bifurkation der Haupt-PA zu zerstören, hat sich in Tierstudien und ersten Humanstudien allmählich als hilfreich bei der Verbesserung der pulmonalen Hämodynamik erwiesen 5 , 6 , 7 , 8 , 9 , 10 , 11 . In einer jüngsten Scheinkontrollstudie an mehreren Standorten und mit randomisierten Studien konnte durch PADN die körperliche Belastbarkeit und die klinischen Ergebnisse bei Patienten mit PH der WHO-Gruppe I während einer 6-monatigen Nachbeobachtung verbessert werden 12 .Beim Menschen werden die PAs vor allem durch sympathische Nerven innerviert, die im Fett- und Bindegewebe rund um den Hauptstamm und die Bifurkation der PA konzentriert sind, wobei > 40 % der Nerven in einer Tiefe von > 4 mm liegen 13 , 14. Daher ist die Wirksamkeit der transluminalen RFA-basierten PADN möglicherweise aufgrund der nicht erreichbaren Ablationstiefe begrenzt 15 , 16. Außerdem wurden in präklinischen Experimenten Lungenembolien und mit RFA assoziierte Verletzungen der PA-Wand festgestellt, darunter Dissektion, fokale Blutungen, verringerte mediale Dicke, Intimaruptur und Thrombose 7 , 16. Außerdem wurden bei der Anwendung in der realen Welt häufig verfahrensbedingte Brustschmerzen beobachtet 5 , 17 .Die stereotaktische Körperradiotherapie (SBRT) ist eine häufig eingesetzte nichtinvasive Technologie zur Behandlung solider Tumoren, bei der hochdosierte Strahlung präzise auf das Ziel gerichtet wird, während durch einen schnellen Dosisabfall die Verletzung des umliegenden Gewebes minimiert wird. Darüber hinaus wurde die SBRT erfolgreich zur Behandlung einer begrenzten Anzahl von Patienten mit Herzrhythmusstörungen eingesetzt, darunter ventrikuläre Tachykardie und Vorhofflimmern 18 , 19. Kürzlich konnte in Schweinemodellen gezeigt werden, dass die SBRT bei entsprechender Strahlendosis sicher und effektiv zur renalen Denervierung eingesetzt werden kann. Verglichen mit konventioneller Radiofrequenz bietet die SBRT die Vorteile eines nichtinvasiven Ansatzes und einer vollständigen, zirkulären Denervierung 20 , 21 .Bis heute ist der potenzielle Nutzen der nichtinvasiven SBRT für PADN unbekannt. Hier zeigen wir, dass die SBRT bei Anwendung des entsprechenden Schemas die sympathische Innervation der PAs nichtinvasiv beeinträchtigen kann, was zu einer anschließenden Verbesserung der Lungenhämodynamik sowohl bei Schweinemodellen von PH auf Basis akuter Vasokonstriktion als auch bei chronischer Monocrotalin-(MCT-)induzierter PH führt.ErgebnisseSBRT-VerfahrenAlle Tiere überlebten die erwartungsgemäße Lebensphase der Studie. Die SBRT wurde für PADN in den Behandlungsgruppen erfolgreich durchgeführt (Abb. 1 ) und während der perioperativen Phase wurden keine akuten Komplikationen beobachtet. Die Behandlungsparameter sind in der Zusatztabelle 1 aufgeführt . Strahlungsdosis und Volumenbeschränkung der gefährdeten Organe (OARs) führten zu einer Dosisverteilung, die bei einigen Tieren nicht perfekt mit dem Zielvolumen übereinstimmte. Ein typisches Dosis-Volumen-Histogramm ist in der Zusatzabbildung 1 dargestellt und zeigt, dass die angegebene Dosis präzise auf den Bifurkationsbereich der Haupt-PA zielte, mit einem schnellen Dosisabfall, um die Strahlung auf das umliegende Gewebe zu minimieren.Abb. 1: Verfahren der stereotaktischen Körperradiotherapie (SBRT) zur Denervierung der Lungenarterie.









OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Bitte Anmelden oder Registrieren um der Konversation beizutreten.
