- Beiträge: 1755
Sidebar
PH, Schwangerschaft
13 Aug 2024 13:10 #2177
von danny
OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
PH, Schwangerschaft wurde erstellt von danny
www.frontiersin.org/journals/cardiovascu...29057/fullBehandlung schwangerer Patientinnen mit pulmonaler arterieller Hypertonie
 Xiao Zhang
1,2,3
Xiao Zhang
1,2,3
 Zhao Huangfu
4 *
Zhao Huangfu
4 *
 Tabelle 1. Aktualisierte Klassifizierung aus den ESC/ERS-Richtlinien 2022. PräkonzeptionsmanagementVerhütungsmittelDie ESC/ERS-Leitlinien von 2022 empfehlen, alle Patienten mit PAH nach einem strengen Verhütungsschema zu behandeln (
9
). Obwohl bei einigen PAH-Patienten mit gut kontrollierter Erkrankung, geringem Risikoprofil und normaler oder nahezu normaler Ruhehämodynamik eine Schwangerschaft möglich sein kann, ist bei Frauen mit schlecht kontrollierter Erkrankung oder Frauen ohne Fruchtbarkeitsanforderungen eine wirksame Empfängnisverhütung angesichts der möglichen Schäden durch Versagen der Empfängnisverhütung unerlässlich (
12
). Die Anwendung von oralen Kontrazeptiva mit reinem Gestagen, Kondomen, Intrauterinpessaren oder einer postkoitalen Notfallverhütung nach dem Geschlechtsverkehr ist bei PAH-Patienten wirksam (
9
,
13
). Allerdings wurde angesichts von Arzneimittelwechselwirkungen, möglichen Kontraindikationen für hormonelle Eingriffe (z. B. Thromboembolien) und der Unzuverlässigkeit von Verhütungsmitteln in mehreren Berichten die Kombination von zwei oder mehr Verhütungsmethoden vorgeschlagen, insbesondere bei PAH-Patienten, die mit Endothelin-Rezeptorantagonisten behandelt werden (
14
–
16
). Eine Tubenligatur ist ebenfalls eine effektive Methode zur dauerhaften Empfängnisverhütung, doch da es sich um einen invasiven Eingriff handelt, gehen die Patientinnen damit auch ein gewisses Risiko von Narkoseunfällen und Komplikationen ein. Daher kann die Tubenligatur gleichzeitig mit einem anderen chirurgischen Eingriff, wie z. B. einem Kaiserschnitt, durchgeführt werden, wodurch das Risiko mehrerer Operationen verringert wird. Darüber hinaus ist die hysteroskopische Sterilisation mittels Mikroinsertion eine der effektivsten Verhütungsmethoden für PAH-Patienten, da das Operationsrisiko offenbar geringer ist (
17
,
18
).Beratung vor der EmpfängnisAufgrund des hohen Risikos unerwünschter Schwangerschaftsausgänge und vererbter Herzfehler (
19
,
20
) wurde in den ESC/ERS-Leitlinien von 2022 empfohlen, dass Frauen mit PAH, die eine Schwangerschaft erwägen oder bereits schwanger waren, eine genetische Beratung und gemeinsame Entscheidungsfindung in erfahrenen medizinischen Zentren erhalten sollten (
9
). Bei schwangeren Frauen mit bekannten PAH-assoziierten genetischen Mutationen sollten auch fetale genetische Tests durchgeführt werden (
21
). Auch wenn keine genetischen Tests durchgeführt werden, sollten Familienmitglieder auf frühe Anzeichen und Symptome aufmerksam gemacht werden, um sicherzustellen, dass rechtzeitig eine angemessene Diagnose gestellt wird (
22
). Tatsächlich sollten Patientinnen mit hohem Risiko neben der Beratung über die mit der Müttersterblichkeit verbundenen Risiken auch über die Möglichkeit einer Schwangerschaftsvermeidung und eines therapeutischen Schwangerschaftsabbruchs informiert werden. In solchen Fällen können auch Alternativen wie Adoption und Leihmutterschaft (sofern legal) geprüft werden (
9
).BehandlungObwohl PAH-Patientinnen eine strenge Verhütungsmethode anwenden müssen, gibt es immer noch Patientinnen, die diese nicht anwenden, weil PAH vor der Schwangerschaft nicht diagnostiziert wurde, oder die auf einer Schwangerschaft bestehen, obwohl sie sich des höheren Schwangerschaftsrisikos bewusst sind (
23
). Eine frühzeitige medikamentöse Intervention, eine umfassende multidisziplinäre Beurteilung und ein gemeinsames Management könnten daher zu Schlüsselfaktoren für die Verbesserung der Gesundheit von Mutter und Fötus werden (
13
,
16
,
24 ). Die Behandlungsprinzipien für schwangere Frauen mit PAH sind die Linderung der klinischen Symptome, die Erhöhung der Belastungsbelastbarkeit und die Verbesserung der Hämodynamik des Lungenkreislaufs. In
den Tabellen 2
und
3
finden Sie eine Zusammenfassung der Arzneimittelkategorien der Food and Drug Administration in der Schwangerschaft sowie der relevanten PAH-assoziierten Therapeutika . TBELLE 2
Tabelle 1. Aktualisierte Klassifizierung aus den ESC/ERS-Richtlinien 2022. PräkonzeptionsmanagementVerhütungsmittelDie ESC/ERS-Leitlinien von 2022 empfehlen, alle Patienten mit PAH nach einem strengen Verhütungsschema zu behandeln (
9
). Obwohl bei einigen PAH-Patienten mit gut kontrollierter Erkrankung, geringem Risikoprofil und normaler oder nahezu normaler Ruhehämodynamik eine Schwangerschaft möglich sein kann, ist bei Frauen mit schlecht kontrollierter Erkrankung oder Frauen ohne Fruchtbarkeitsanforderungen eine wirksame Empfängnisverhütung angesichts der möglichen Schäden durch Versagen der Empfängnisverhütung unerlässlich (
12
). Die Anwendung von oralen Kontrazeptiva mit reinem Gestagen, Kondomen, Intrauterinpessaren oder einer postkoitalen Notfallverhütung nach dem Geschlechtsverkehr ist bei PAH-Patienten wirksam (
9
,
13
). Allerdings wurde angesichts von Arzneimittelwechselwirkungen, möglichen Kontraindikationen für hormonelle Eingriffe (z. B. Thromboembolien) und der Unzuverlässigkeit von Verhütungsmitteln in mehreren Berichten die Kombination von zwei oder mehr Verhütungsmethoden vorgeschlagen, insbesondere bei PAH-Patienten, die mit Endothelin-Rezeptorantagonisten behandelt werden (
14
–
16
). Eine Tubenligatur ist ebenfalls eine effektive Methode zur dauerhaften Empfängnisverhütung, doch da es sich um einen invasiven Eingriff handelt, gehen die Patientinnen damit auch ein gewisses Risiko von Narkoseunfällen und Komplikationen ein. Daher kann die Tubenligatur gleichzeitig mit einem anderen chirurgischen Eingriff, wie z. B. einem Kaiserschnitt, durchgeführt werden, wodurch das Risiko mehrerer Operationen verringert wird. Darüber hinaus ist die hysteroskopische Sterilisation mittels Mikroinsertion eine der effektivsten Verhütungsmethoden für PAH-Patienten, da das Operationsrisiko offenbar geringer ist (
17
,
18
).Beratung vor der EmpfängnisAufgrund des hohen Risikos unerwünschter Schwangerschaftsausgänge und vererbter Herzfehler (
19
,
20
) wurde in den ESC/ERS-Leitlinien von 2022 empfohlen, dass Frauen mit PAH, die eine Schwangerschaft erwägen oder bereits schwanger waren, eine genetische Beratung und gemeinsame Entscheidungsfindung in erfahrenen medizinischen Zentren erhalten sollten (
9
). Bei schwangeren Frauen mit bekannten PAH-assoziierten genetischen Mutationen sollten auch fetale genetische Tests durchgeführt werden (
21
). Auch wenn keine genetischen Tests durchgeführt werden, sollten Familienmitglieder auf frühe Anzeichen und Symptome aufmerksam gemacht werden, um sicherzustellen, dass rechtzeitig eine angemessene Diagnose gestellt wird (
22
). Tatsächlich sollten Patientinnen mit hohem Risiko neben der Beratung über die mit der Müttersterblichkeit verbundenen Risiken auch über die Möglichkeit einer Schwangerschaftsvermeidung und eines therapeutischen Schwangerschaftsabbruchs informiert werden. In solchen Fällen können auch Alternativen wie Adoption und Leihmutterschaft (sofern legal) geprüft werden (
9
).BehandlungObwohl PAH-Patientinnen eine strenge Verhütungsmethode anwenden müssen, gibt es immer noch Patientinnen, die diese nicht anwenden, weil PAH vor der Schwangerschaft nicht diagnostiziert wurde, oder die auf einer Schwangerschaft bestehen, obwohl sie sich des höheren Schwangerschaftsrisikos bewusst sind (
23
). Eine frühzeitige medikamentöse Intervention, eine umfassende multidisziplinäre Beurteilung und ein gemeinsames Management könnten daher zu Schlüsselfaktoren für die Verbesserung der Gesundheit von Mutter und Fötus werden (
13
,
16
,
24 ). Die Behandlungsprinzipien für schwangere Frauen mit PAH sind die Linderung der klinischen Symptome, die Erhöhung der Belastungsbelastbarkeit und die Verbesserung der Hämodynamik des Lungenkreislaufs. In
den Tabellen 2
und
3
finden Sie eine Zusammenfassung der Arzneimittelkategorien der Food and Drug Administration in der Schwangerschaft sowie der relevanten PAH-assoziierten Therapeutika . TBELLE 2
 Tabelle 2. Arzneimittelkategorien der US-amerikanischen Food and Drug Administration (FDA) in der Schwangerschaft. TBELLE 3
Tabelle 2. Arzneimittelkategorien der US-amerikanischen Food and Drug Administration (FDA) in der Schwangerschaft. TBELLE 3
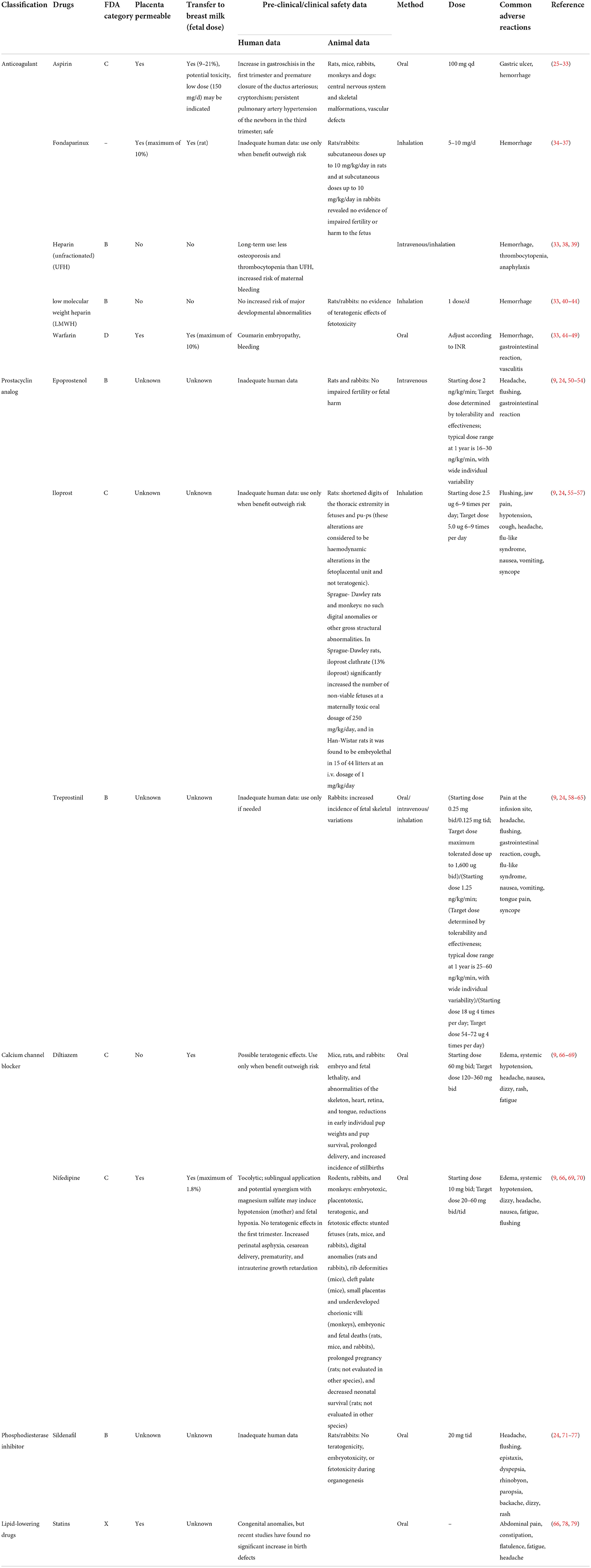 Tabelle 3. Arzneimittel und Sicherheitsdaten. GeschäftsführungSchwangere Frauen mit PAH sollten übermäßige Aktivitäten vermeiden, aber dennoch ermutigt werden, im Rahmen der Symptomgrenzen aktiv zu sein (
16
,
80
). Wann immer möglich, sollte immer eine Seitenlage eingenommen werden, um die Kompression der unteren Hohlvene im dritten Trimester zu minimieren. Beim Gehen können auch elastische Stützstrümpfe getragen werden, um drastische Veränderungen des Blutvolumens zu vermeiden. Darüber hinaus sollte eine entsprechende Ergänzung von Eisen und Folsäure gefördert werden, um einer Anämie vorzubeugen, während zur Stärkung der Immunität eine Impfung zumindest gegen Influenza, Streptococcus pneumoniae und SARS-CoV-2 vor der Schwangerschaft empfohlen wird (
9
,
81
,
82
).Für Patientinnen mit PAH, die sich für eine Fortsetzung der Schwangerschaft entscheiden, sollte ein standardisierter, individualisierter und realistischer Diagnose- und Behandlungsplan erstellt werden. Während der Schwangerschaft sollten sie regelmäßig und streng von Ärzten mit unterschiedlichem disziplinären Hintergrund beurteilt und untersucht werden (
83
). Vor der 20. Schwangerschaftswoche sollten alle 2 Wochen und nach der 20. Schwangerschaftswoche einmal wöchentlich vorgeburtliche Kontrolluntersuchungen durchgeführt werden. Neben der routinemäßigen geburtshilflichen Untersuchung sollte auch auf die Klassifizierung der primären Erkrankung, die die PAH verursacht, die primären Symptome der PAH, die Herzfunktion, Echokardiographie, den 6-Minuten-Gehtest und biochemische Indikatoren wie Thrombozytenzahl, Hämoglobin, Werte des natriuretischen Peptids des Gehirns und arterielle Blutgasanalyse geachtet werden (
23
). Da Feten schwangerer Frauen mit PAH typischerweise unterschiedliche Grade von Wachstumsstörungen aufweisen, sollte bei jeder geburtshilflichen Untersuchung Ultraschall durchgeführt werden, um den Status des fetalen Wachstums zu überprüfen (
7
,
13
,
23
). Bei einer Verschlechterung des Zustands wäre ein Krankenhausaufenthalt erforderlich. Bei schwangeren Frauen mit mittelschwerer bis schwerer PAH (mWHO II-IV) ist die Behandlung durch ein multidisziplinäres Team erforderlich. Dieses Expertenteam sollte mindestens einen Kardiologen, einen Ophthalmologen und einen Anästhesisten mit Fachkenntnissen in der Behandlung von Hochrisikoschwangeren mit Herzerkrankungen umfassen. Darüber hinaus sollten, entsprechend der individuellen Situation jeder Patientin, weitere Spezialisten einbezogen werden, darunter solche mit umfassenden Kenntnissen in Pharmazie, Herz-Thorax-Chirurgie, Fetalmedizin, Neonatologie, Hämatologie, Krankenpflege und Pneumologie (
1
,
84
). Angesichts der hohen Prävalenz von Symptomen wie Depression, Angst und Anpassungsstörungen bei Patientinnen mit PAH ist eine empathische und hoffnungsvolle Kommunikation für Ärzte, die schwangere Frauen mit PAH betreuen, ebenfalls von entscheidender Bedeutung (
9
).Unterstützende TherapieSauerstofftherapieDie Inhalation von Sauerstoff wird empfohlen, wenn die periphere Sauerstoffsättigung < 90 % oder der arterielle Sauerstoffpartialdruck < 60 mmHg beträgt. Die Aufrechterhaltung des arteriellen Sauerstoffpartialdrucks bei > 70 mmHg und der Sauerstoffsättigung bei > 92 % kann den pulmonalvaskulären Widerstand, den Rechts-Links-Shunt und die Häufigkeit von Neugeborenen mit untergewichtigem Geburtsgewicht verringern (
85
). Bei schlafbezogener Entsättigung sollte eine nächtliche Sauerstofftherapie in Betracht gezogen werden (
86
). Die Sauerstoffinhalation sollte auch in Betracht gezogen werden, wenn schwangere Patientinnen mit PAH mit dem Flugzeug reisen, insbesondere wenn sie an einer PAH der Klasse III-IV der New York Heart Association (NYHA) leiden oder einen arteriellen Sauerstoffpartialdruck von < 8 kPa haben (
87
,
88
). Obwohl die Sauerstoffgabe den pulmonalvaskulären Widerstand senkt und die Belastungstoleranz bei Patienten mit PAH verbessert, gibt es keine Daten, die darauf hindeuten, dass eine langfristige Sauerstofftherapie einen nachhaltigen Nutzen für den Krankheitsverlauf hat (
9
).Diuretika, Kardiotonika und AntiarrhythmikaDiuretika können die Symptome einer Dekompensation nach Rechtsherzinsuffizienz lindern. Torasemid oder Furosemid sind Optionen für Schleifendiuretika während der Schwangerschaft. Spironolacton sollte jedoch während des ersten Trimesters aufgrund seiner antiandrogenen Wirkung vermieden werden (
13
,
66
,
89
,
90
). Während der Anwendung von Diuretika ist eine regelmäßige Überwachung der Nierenfunktion und der Serumelektrolyte erforderlich, um einen intravaskulären Volumenmangel und einen weiteren Abfall des Herzzeitvolumens und des systemischen Blutdrucks zu vermeiden.Kardiologische Mittel wie Digoxin oder Milrinon können das Herzzeitvolumen bei Patienten mit PAH verbessern, obwohl ihre langfristige Wirksamkeit unklar bleibt. Außerdem ist die Aufrechterhaltung des Sinusrhythmus wichtig, da Vorhofflimmern und supraventrikuläre Tachykardie mit dem Auftreten von Rechtsherzversagen und anschließender Mortalität verbunden sind (
91
). Intravenöses Adenosin ist die bevorzugte Behandlungsmethode bei akuten Episoden einer paroxysmalen supraventrikulären Tachykardie (PSVT). Im Gegensatz dazu sind β-adrenerge Rezeptorblocker, mit Ausnahme von Atenolol, Medikamente der ersten Wahl zur Vorbeugung von PSVT. Eine elektrische Kardioversion wird auch empfohlen, wenn Patienten mit Vorhofflimmern hämodynamisch instabil werden oder wenn bei ihnen ein hohes Mortalitätsrisiko besteht (
92
). Ibutilid- oder Flecainid-Injektionen können in Betracht gezogen werden, um Vorhofflattern und Vorhofflimmern bei PAH-Patienten mit strukturell normalen Herzen zu beseitigen (
93
). Da Patienten mit angeborenen Herzfehlern Vorhofflattern im Allgemeinen nicht gut tolerieren, sollte eine elektrische Kardioversion durchgeführt werden, um den Sinusrhythmus wiederherzustellen (
94
). Die idiopathische Tachykardie des rechtsventrikulären Ausflusstrakts ist die häufigste Art von ventrikulärer Tachykardie, die β-Rezeptorblocker, Verapamil oder andere antiarrhythmische Prophylaxemittel erfordert. Bei Versagen der medikamentösen Behandlung ist eine Katheterablation erforderlich. Wenn möglich, sollte die Katheterablation bis zum zweiten Trimester verschoben und in einem gut ausgerüsteten medizinischen Zentrum mit Experten mit umfassender Erfahrung durchgeführt werden (
95
,
96
). Außerdem kann eine gelegentliche Sinusbradykardie mit dem hypotensiven Syndrom in Rückenlage verbunden sein. Eine symptomatische Bradykardie sollte mit Veränderungen der mütterlichen Lage behandelt werden. Falls die klinischen Symptome anhalten, sollte anschließend ein temporärer Schrittmacher eingesetzt werden (
97
,
98
). Bei hämodynamisch stabilen Patienten sind temporäre Herzschrittmacher in der Regel nicht erforderlich. Sie werden jedoch während der Wehen bei Frauen mit Bradykardierisiko oder bei Frauen mit einer Synkopenanamnese empfohlen (
97
). Bei Patientinnen mit hohem Risiko für einen plötzlichen Herztod sollten implantierbare Kardioverter-Defibrillatoren auch vor einer Schwangerschaft in Betracht gezogen werden (
80
,
99
).AntikoagulanzientherapieSchwangere Frauen weisen häufig eine Hyperkoagulabilität auf, die das Thromboserisiko erhöhen kann. Wenn bei einer schwangeren Person mit PAH eine kardiopulmonale Dysfunktion festgestellt wurde, werden Antikoagulanzien zur Verringerung des Thromboserisikos empfohlen. Die Auswahl der gerinnungshemmenden Medikamente sollte umfassend unter Berücksichtigung der betroffenen Person, des Stadiums der Schwangerschaft, des mütterlichen Blutungsrisikos und teratogener Wirkungen abgewogen werden (
15
,
100
). Da niedermolekulares Heparin (NMH) geringere Auswirkungen auf den Fötus sowie ein geringeres Osteoporoserisiko aufweist, gilt es als bevorzugtes Medikament zur Vorbeugung und Behandlung venöser Thromboembolien während der Schwangerschaft und im Wochenbett. Der vorbeugende Effekt von NMH gegen Klappenthrombosen ist jedoch schwach (
38
). Wenn NMH oder unfraktioniertes Heparin (UFH) während der Schwangerschaft angewendet werden, wird empfohlen, die Anfangsdosis nach dem Gewicht der Mutter im ersten Trimenon (8.–10. Schwangerschaftswoche) zu berechnen. Die Dosis sollte anschließend durch wöchentliche Überwachung der Anti-Faktor-Xa-Spiegel oder der partiellen Thromboplastinzeit angepasst werden, bis die maximalen Anti-Xa-Spiegel nach 4 bis 6 Stunden 0,6–1,2 IU/ml erreicht haben (
1
,
101
). Fondaparinux kann sogar für PAH-Patienten in Betracht gezogen werden, wenn diese gegen NMH allergisch sind. Warfarin kann die Plazenta passieren und dosisabhängig teratogene Wirkungen haben, die zum „fetalen Warfarin-Syndrom“ führen können (
102
). Daher sollte Warfarin im ersten Trimester nur in begrenzten Dosen verwendet oder durch NMH ersetzt werden. Die Warfarin-Dosierung muss auf < 5 mg/Tag begrenzt und die International Normalized Ratio (INR) im zweiten und dritten Trimester auf 1,5–2,0 angepasst werden. Das Sicherheitsprofil von Warfarin bei Schwangeren ist jedoch nach wie vor umstritten, und daher sollte es während der Schwangerschaft wenn möglich vermieden werden
(
40
,
45
,
103–106
)
. Darüber hinaus fehlen weiterhin hochwertige Belege für die Sicherheit und Wirksamkeit neuer oraler Antikoagulanzien wie Dabigatran, Rivaroxaban und Apixaban bei schwangeren Frauen, was deren Anwendungsempfehlung verhindert (
107
,
108
). Eine Metaanalyse von 339 schwangeren Frauen, die neue direkte orale Antikoagulanzien einnahmen, ergab, dass 22,2 % Fehlgeburten erlitten und 3,6 % Föten mit Skelett- und Gesichtsdeformationen hatten (
109
). Insbesondere mussten alle Patientinnen die orale Antikoagulation während der ersten beiden Schwangerschaftsmonate absetzen, was darauf hindeutet, dass die während der Schwangerschaft angewendeten neuen oralen Antikoagulationsschemata möglicherweise mit einem höheren Risiko von Fehlgeburten und Geburtsfehlern verbunden sind (
110
).Orale Antikoagulanzien sollten 3–5 Tage vor der Entbindung durch LMWH oder UFH ersetzt werden, was die Durchführung eines Kaiserschnitts sicherer macht. LMWH sollte jedoch 12–24 Stunden vor der Entbindung abgesetzt werden, während UFH > 4–7 Tage vor der Entbindung abgesetzt werden sollte. Protaminantagonisten können vorsichtig bei Schwangeren eingesetzt werden, bei denen ein Schwangerschaftsabbruch notwendig ist, die Heparinbehandlung jedoch nicht abgebrochen wurde. Warfarin hingegen kann durch Vitamin-K1-Antagonisten antagonisiert werden (
15
,
111–113
)
.
Wenn 24 Stunden nach der Entbindung keine offensichtliche Blutung auftritt, kann die Antikoagulationstherapie wieder aufgenommen werden. Es ist jedoch zu beachten, dass Patientinnen, die zuvor mit Warfarin behandelt wurden, stattdessen LMWH erhalten und der INR-Wert mehrere Tage nach der Entbindung überwacht werden sollte. LMWH kann dann abgesetzt werden, wenn Warfarin zu wirken beginnt.PAH-spezifische TherapieDie derzeit verfügbaren Medikamente, die auf die pathologischen Bahnen abzielen, die der PAH zugrunde liegen, führten zwar nicht zu einer vollständigen Umkehrung der Erkrankung, senkten aber nachweislich den pulmonalarteriellen Druck und linderten die klinischen Symptome. Bei Patienten mit stabiler Hämodynamik wird die routinemäßige Anwendung von Vasodilatatoren und anderen Medikamenten, die die Hämodynamik beeinträchtigen können, nicht empfohlen. Bei Patienten mit instabiler Hämodynamik kann jedoch die kumulative Gabe von pulmonalen Vasodilatatoren zu den bestehenden allgemeinen Behandlungsschemata das Risiko der Müttersterblichkeit und von ungünstigen Schwangerschaftsausgängen deutlich senken (
14
,
114
). Zu diesen Vasodilatatoren zählen Kalziumkanalblocker (CCB) (
4
,
6
,
115
), Prostaglandine und assoziierte Analoga (
7
,
50
,
51
,
55
,
116
) sowie Phosphodiesterasehemmer (PDE-I) (
117
), jedoch keine Endothelin-Rezeptorantagonisten aufgrund des teratogenen Potenzials (
118
,
119
). Pieper et al. schlugen vor, mit der medikamentösen Behandlung der PAH mindestens drei Monate vor der Entbindung zu beginnen, da die optimale Wirkung erst drei Monate später eintrat (
14
). Da jedoch die Anwendung pulmonaler Vasodilatatoren bei Schwangeren die Sicherheit des Fötus gefährden kann, muss ihre Anwendung mit ihren Standardformulierungen und -anwendungen evaluiert werden, was zusätzliche Unterstützung durch hochwertige, evidenzbasierte Forschung erfordert.Prostaglandine und AnalogaProstacyclin kann die Proliferation glatter Muskeln hemmen, die Gefäßumgestaltung umkehren, den pulmonalen und systemischen Kreislauf erweitern, die Funktion des rechten Ventrikels verbessern und eine thrombozytenaggregationshemmende Wirkung haben (
120
). Allerdings können Thrombozytopenie und blutungsbedingte Komplikationen auftreten, wenn die Patienten gleichzeitig mit Antikoagulanzien und Prostacyclin behandelt werden. Daher sollten die Blutwerte und die Gerinnungsparameter engmaschig überwacht werden (
45
)
. Indikationen für den Beginn der Anwendung von Prostaglandinen sind typischerweise Patienten mit PAH der WHO-FC-Klasse III-IV oder eingeschränkter Funktion des rechten Ventrikels ( 88
,
121-123
)
.Derzeit ist Epoprostenol das am häufigsten verwendete zielgerichtete Medikament bei schwangeren Frauen mit PAH (62 %) und das Medikament der ersten Wahl zur Behandlung von Schwangerschaften mit PAH oder Eisenmenger-Syndrom ( 52
,
124–126
)
. Epoprostenol kann die körperliche Belastbarkeit, Lebensqualität und Überlebensrate verbessern (
120
). Aufgrund des langsamen Wirkungseintritts und der kurzen Halbwertszeit wird empfohlen, die Behandlung mit diesem Medikament mindestens 8 Wochen vor der Entbindung über einen zentralen Venenkatheter zu beginnen (
120
). Es kann auch postpartal zur Vorbeugung einer pulmonalarteriellen Hypertoniekrise und einer Rechtsherzinsuffizienz verwendet werden (
127
,
128 ). Zur Sicherheit dieses Medikaments für den Fötus liegen keine Daten und Erfahrungen
vor
, aber mehrere Studien haben gezeigt, dass es im dritten Trimenon keine fetalen Missbildungen oder intrauterine Wachstumsstörungen verursacht hat (
55
,
116
). Zu den Nebenwirkungen, die mit der Langzeitanwendung von Epoprostenol verbunden sind, können Gesichtsrötung, Kopfschmerzen, Durchfall, Bauchschmerzen, Gebärmutterkontraktionen und postpartale Blutungen gehören. Eine Dosisreduktion ist jedoch nur erforderlich, wenn die Nebenwirkungen schwerwiegend werden.Iloprost ist ein inhaliertes Prostacyclin-Analogon, das häufig zur Linderung von Dyspnoe während chirurgischer Eingriffe eingesetzt wird. Der Wirkungseintritt beträgt im Allgemeinen 15–20 Minuten, und die Wirkungsdauer beträgt 1–2 Stunden (
125
,
127
,
129
). Im Vergleich zur intravenösen Verabreichung neigt die kurzfristige Anwendung von Iloprost-Aerosol-Inhalationen dazu, den pulmonalarteriellen Druck wirksamer zu senken (
6
,
7
,
55
). Derzeit gibt es keine Hinweise darauf, dass inhaliertes Iloprost Müttersterblichkeit oder angeborene fetale Anomalien verursachen kann. Es gibt jedoch Hinweise darauf, dass die Inhalation von Iloprost innerhalb von 24 Schwangerschaftswochen und in der perinatalen Periode das Risiko fetaler Missbildungen und Mortalität signifikant senken kann (
55
,
114
,
130
). Es ist zu beachten, dass intravenöses Epoprostenol verabreicht werden sollte, wenn sich die Krankheit nach Inhalation von Iloprost verschlimmert (
52
,
114
). Inhalative Prostaglandine werden im Allgemeinen bei Patienten mit weniger schweren PAH-Symptomen eingesetzt, da die intermittierende Verabreichung mittels Vernebelung eine kurze Halbwertszeit hat und es zu einem erneuten Anstieg des pulmonalarteriellen Drucks kommen kann (
13
,
55
). Es ist jedoch ein Zeichen für einen ernsten Zustand, wenn Patienten mit PAH Iloprost vor der Empfängnis einnehmen.Treprostinil kann auf verschiedene Weise verabreicht werden, einschließlich subkutaner Infusion, intravenöser und oraler Verabreichung (
131
). Dieses Medikament kann bei Patienten mit Herzfunktionsklasse II-IV der WHO oder PAH der NYHA-Klasse III-IV eingesetzt werden. Es wurde berichtet, dass es die 6-Minuten-Gehstrecke, die periphere Blutsauerstoffsättigung und die Herzfunktion signifikant verbessert (
132
). Einige Patienten (etwa 8 %) lehnten die Einnahme dieses Medikaments jedoch aufgrund der Schmerzen an der Infusionsstelle ab (
133
).CCBsEinige schwangere Frauen mit PAH können von CCBs profitieren. CCBs werden jedoch normalerweise nur bei Patienten angewendet, deren Testergebnisse für akute pulmonale Vasodilatation positiv sind (
4
,
6
,
85
,
115
). Diltiazem ist das CCB der ersten Wahl für Patienten mit schnellem Herzrhythmus, während Nifedipin für Patienten mit langsamem Herzrhythmus verwendet wird. Zunächst sollte die Mindestdosis verwendet und die Dosis schrittweise entsprechend Blutdruck, Herzrhythmus, Herzfrequenz, EKG-Ergebnissen und klinischen Symptomen erhöht werden, bis die maximal verträgliche Dosis erreicht ist. Wenn die Struktur und Funktion des rechten Herzens auf physiologischem Niveau bleiben und der pulmonalarterielle Druck nach der CCB-Therapie normal oder annähernd normal ist (mittlerer pulmonalarterieller Druck ≤ 30 mmHg und pulmonaler Gefäßwiderstand < 4 WU), kann davon ausgegangen werden, dass der Patient kontinuierlich auf CCBs empfindlich reagiert, was bedeutet, dass die CCBs chronisch angewendet werden können. Wenn keine zufriedenstellende Reaktion eintritt, sollte eine zusätzliche PAH-Therapie eingeleitet werden. Verschiedene Studien haben jedoch gezeigt, dass CCBs keine langfristigen vasodilatatorischen Effekte bei Patienten mit PAH hervorrufen können. Eine Exposition gegenüber CCBs im dritten Trimester kann das Risiko für Krampfanfälle bei Neugeborenen erhöhen (Odd Ratio = 3,6) (
134
,
135
). Daher muss eine schrittweise Umstellung von CCBs auf Prostaglandine oder Analoga oder PDE-I in Betracht gezogen werden, wenn die Herzfunktion und der pulmonalarterielle Druck nicht auf einem normalen Niveau gehalten werden können (
127
).PDE-IPDE-5-Hemmer sind das bevorzugte Medikament für Frauen mit PAH der WHO-Herzfunktionsklasse I-II oder normaler rechtsventrikulärer Funktion (
5
,
71
,
136
). Die Expressionsgrade von PDE-5 im rechtsventrikulären Myokard sind bei Patientinnen mit PAH häufig erhöht. PDE-5-Hemmer können diese Veränderung umkehren, indem sie die Gefäßglattmuskulatur entspannen und den pulmonalarteriellen Druck senken (
6
). Darüber hinaus verändert die Verwendung von PDE-5-Hemmern weder den Laktatspiegel noch den pH-Wert des Fötus. Sildenafil ist der am häufigsten angewendete PDE-5-Hemmer. Es wurde bereits festgestellt, dass Sildenafil die klinischen Symptome, die Herzfunktion, die hämodynamischen Indizes und den Schwangerschaftsverlauf signifikant verbessern kann (
111
). Es kann auch die Rate erfolgreicher vaginaler Entbindungen erhöhen und die Häufigkeit von Frühgeburten oder Säuglingen mit geringem Geburtsgewicht verringern (
130
,
136
,
137
). Wenn sich die Herzfunktion weiter verschlechtert und der pulmonalvaskuläre Widerstand nach oraler Sildenafil-Behandlung steigt, kann die Inhalation von Iloprost zur Linderung der Symptome in Betracht gezogen werden (
136
,
137
). Darüber hinaus zeigte eine frühere Studie, dass fünf schwangere Frauen mit PAH, die PDE-5-Hemmer und Prostacyclin intravenös erhielten, bei der Langzeitnachbeobachtung in der Stillzeit keine signifikanten Komplikationen bei Mutter und Kind aufwiesen (
84
).Obwohl Sildenafil weit verbreitet ist, muss seine Sicherheit während der Schwangerschaft noch weiter untersucht werden. Eine Studie aus dem Jahr 2021 mit 77 Säuglingen von Frauen, die während der Schwangerschaft mit PDE-5-Hemmern behandelt wurden, ergab, dass neun Säuglinge Frühgeborene waren, sechs für ihr Gestationsalter zu klein waren, fünf bei ihren 5-Minuten-Tests für Aussehen, Puls, Grimasse, Aktivität und Atmung einen Wert von < 8 erreichten, 18 auf die Neugeborenen-Intensivstation eingeliefert wurden und bei acht Säuglingen Atemwegs- und Herz-Kreislauf-Erkrankungen diagnostiziert wurden (
138
). Darüber hinaus gibt es derzeit keine klinischen Belege für die Wirksamkeit von Vardenafil und Tadalafil bei schwangeren Frauen mit PAH.StatineNeben hypolipidämischen Effekten wurden von Statinen auch entzündungshemmende, antiproliferative und apoptotische Wirkungen berichtet. Zahlreiche klinische und experimentelle Studien haben gezeigt, dass Statine den pulmonalarteriellen Druck senken und die pulmonale vaskuläre Umgestaltung verbessern können, indem sie die Apoptose fördern, die Zellproliferation hemmen, entzündungshemmende Wirkungen haben, die Rho-Kinase-Signalgebung und die Endothelin-1-Freisetzung hemmen (
139
–
142
). Obwohl Statine auch die Rate an Geburtsfehlern oder die Rate an fetaler Teratogenität nicht erhöhten, war die Stichprobengröße relativ klein (
78
). Obwohl Statine derzeit im Allgemeinen während der Schwangerschaft und Stillzeit nicht empfohlen werden, können sie zur Langzeitbehandlung von postpartaler PAH nach der Stillzeit verwendet werden (
66
,
79
).ECMOECMO ist eine fortschrittliche Technologie zur Atmungs- und Kreislaufunterstützung, die für Patienten mit akutem, reversiblem Atemversagen vorgeschlagen wurde (
143
). ECMO kann den Sauerstoffsättigungsstatus von Patienten mit PAH aufrechterhalten, wenn die Herzfunktion dekompensiert ist (
144
,
145
). Verschiedene Fallberichte deuteten darauf hin, dass die ECMO-Behandlung bei der Mehrzahl der schwangeren Frauen mit PAH zu günstigen Schwangerschaftsergebnissen führte (
146
–
148
). Es wurde jedoch auch von Patienten mit PAH berichtet, die ECMO erhielten, die aufgrund einer schweren Rechtsherzinsuffizienz drei Monate nach der Entbindung nicht überlebten (
149
). Außerdem erfordert der kontinuierliche Betrieb von ECMO eine systemische Antikoagulation, wobei das kontinuierliche Nässen aus dem Operationsschnitt zu schweren Gerinnungsstörungen führen kann (
150
,
151
). Aufgrund der bisher berichteten geringen Stichprobengröße sind weitere Studien mit größeren Stichproben erforderlich.Operative TherapieEine PAH als Folge einer bekannten kardiopulmonalen Erkrankung erfordert eine aggressive Behandlung der Primärerkrankung mit Verfahren wie biventrikulärer Stimulation und Herzoperationen (
85
). Eine Herzoperation mit kardiopulmonalem Bypass kann bei Patientinnen erwogen werden, die auf eine medikamentöse Therapie angesprochen haben, bei denen aber die Möglichkeit einer Operation besteht. Die Operation sollte zwischen der 13. und 28. Schwangerschaftswoche durchgeführt werden. Liegt die Schwangerschaftswoche über 26 Wochen, kann vor der Durchführung der kardiopulmonalen Bypass-Operation ein Kaiserschnitt zur Beendigung der Schwangerschaft in Erwägung gezogen werden. Liegt die Schwangerschaftswoche über 28 Wochen, kann nach einer vaginalen Entbindung eine Herzoperation erwogen werden. Allerdings bleibt das Risiko mütterlicher und fetaler Mortalität auch während einer kardiopulmonalen Bypass-Operation hoch. Eine Herzoperation wird nur empfohlen, wenn Medikamente oder andere interventionelle Therapien versagen und die Schwangere in Lebensgefahr schwebt (
1
,
88
,
152
).Bei Patienten mit chronisch thromboembolischer PAH ist die pulmonale Endarteriektomie eine mögliche kurative Methode, obwohl nicht alle Patienten für diese Form der chirurgischen Behandlung geeignet sind. Bei chronisch thromboembolischer PAH kann auch eine postpartale Thrombektomie oder Lungentransplantation erforderlich sein (
146
). Hochrisikopatientinnen, die sich für eine Fortsetzung der Schwangerschaft entscheiden, sollten umgehend auf eine Lungentransplantation untersucht werden (
6
).SchlussfolgerungenPAH gilt als irreversible Krankheit. Bei PAH jeder Schwere wird eine strikte Empfängnisverhütung oder ein frühzeitiger Schwangerschaftsabbruch empfohlen. Eine effektive frühzeitige Behandlung ist jedoch wichtig, um die Prognose schwangerer Frauen mit PAH zu verbessern, bei denen PAH erstmals während der Schwangerschaft entdeckt wurde oder die die Schwangerschaft unbedingt fortsetzen müssen. Strategien wie Antikoagulationstherapie, PAH-spezifische Therapie und operative Therapie sollten in Betracht gezogen werden. Da eine Schwangerschaft mit PAH eine seltene Erkrankung ist, handelt es sich bei den meisten relevanten Studien um retrospektive Studien, die auf Fallberichten und Fallserienanalysen basieren und nur über einen geringen Grad an evidenzbasierter medizinischer Evidenz verfügen. Daher sollten in Zukunft zusätzliche prospektive Multicenterstudien durchgeführt werden, um die klinischen Behandlungsstrategien für schwangere Frauen mit PAH zu optimieren.
Tabelle 3. Arzneimittel und Sicherheitsdaten. GeschäftsführungSchwangere Frauen mit PAH sollten übermäßige Aktivitäten vermeiden, aber dennoch ermutigt werden, im Rahmen der Symptomgrenzen aktiv zu sein (
16
,
80
). Wann immer möglich, sollte immer eine Seitenlage eingenommen werden, um die Kompression der unteren Hohlvene im dritten Trimester zu minimieren. Beim Gehen können auch elastische Stützstrümpfe getragen werden, um drastische Veränderungen des Blutvolumens zu vermeiden. Darüber hinaus sollte eine entsprechende Ergänzung von Eisen und Folsäure gefördert werden, um einer Anämie vorzubeugen, während zur Stärkung der Immunität eine Impfung zumindest gegen Influenza, Streptococcus pneumoniae und SARS-CoV-2 vor der Schwangerschaft empfohlen wird (
9
,
81
,
82
).Für Patientinnen mit PAH, die sich für eine Fortsetzung der Schwangerschaft entscheiden, sollte ein standardisierter, individualisierter und realistischer Diagnose- und Behandlungsplan erstellt werden. Während der Schwangerschaft sollten sie regelmäßig und streng von Ärzten mit unterschiedlichem disziplinären Hintergrund beurteilt und untersucht werden (
83
). Vor der 20. Schwangerschaftswoche sollten alle 2 Wochen und nach der 20. Schwangerschaftswoche einmal wöchentlich vorgeburtliche Kontrolluntersuchungen durchgeführt werden. Neben der routinemäßigen geburtshilflichen Untersuchung sollte auch auf die Klassifizierung der primären Erkrankung, die die PAH verursacht, die primären Symptome der PAH, die Herzfunktion, Echokardiographie, den 6-Minuten-Gehtest und biochemische Indikatoren wie Thrombozytenzahl, Hämoglobin, Werte des natriuretischen Peptids des Gehirns und arterielle Blutgasanalyse geachtet werden (
23
). Da Feten schwangerer Frauen mit PAH typischerweise unterschiedliche Grade von Wachstumsstörungen aufweisen, sollte bei jeder geburtshilflichen Untersuchung Ultraschall durchgeführt werden, um den Status des fetalen Wachstums zu überprüfen (
7
,
13
,
23
). Bei einer Verschlechterung des Zustands wäre ein Krankenhausaufenthalt erforderlich. Bei schwangeren Frauen mit mittelschwerer bis schwerer PAH (mWHO II-IV) ist die Behandlung durch ein multidisziplinäres Team erforderlich. Dieses Expertenteam sollte mindestens einen Kardiologen, einen Ophthalmologen und einen Anästhesisten mit Fachkenntnissen in der Behandlung von Hochrisikoschwangeren mit Herzerkrankungen umfassen. Darüber hinaus sollten, entsprechend der individuellen Situation jeder Patientin, weitere Spezialisten einbezogen werden, darunter solche mit umfassenden Kenntnissen in Pharmazie, Herz-Thorax-Chirurgie, Fetalmedizin, Neonatologie, Hämatologie, Krankenpflege und Pneumologie (
1
,
84
). Angesichts der hohen Prävalenz von Symptomen wie Depression, Angst und Anpassungsstörungen bei Patientinnen mit PAH ist eine empathische und hoffnungsvolle Kommunikation für Ärzte, die schwangere Frauen mit PAH betreuen, ebenfalls von entscheidender Bedeutung (
9
).Unterstützende TherapieSauerstofftherapieDie Inhalation von Sauerstoff wird empfohlen, wenn die periphere Sauerstoffsättigung < 90 % oder der arterielle Sauerstoffpartialdruck < 60 mmHg beträgt. Die Aufrechterhaltung des arteriellen Sauerstoffpartialdrucks bei > 70 mmHg und der Sauerstoffsättigung bei > 92 % kann den pulmonalvaskulären Widerstand, den Rechts-Links-Shunt und die Häufigkeit von Neugeborenen mit untergewichtigem Geburtsgewicht verringern (
85
). Bei schlafbezogener Entsättigung sollte eine nächtliche Sauerstofftherapie in Betracht gezogen werden (
86
). Die Sauerstoffinhalation sollte auch in Betracht gezogen werden, wenn schwangere Patientinnen mit PAH mit dem Flugzeug reisen, insbesondere wenn sie an einer PAH der Klasse III-IV der New York Heart Association (NYHA) leiden oder einen arteriellen Sauerstoffpartialdruck von < 8 kPa haben (
87
,
88
). Obwohl die Sauerstoffgabe den pulmonalvaskulären Widerstand senkt und die Belastungstoleranz bei Patienten mit PAH verbessert, gibt es keine Daten, die darauf hindeuten, dass eine langfristige Sauerstofftherapie einen nachhaltigen Nutzen für den Krankheitsverlauf hat (
9
).Diuretika, Kardiotonika und AntiarrhythmikaDiuretika können die Symptome einer Dekompensation nach Rechtsherzinsuffizienz lindern. Torasemid oder Furosemid sind Optionen für Schleifendiuretika während der Schwangerschaft. Spironolacton sollte jedoch während des ersten Trimesters aufgrund seiner antiandrogenen Wirkung vermieden werden (
13
,
66
,
89
,
90
). Während der Anwendung von Diuretika ist eine regelmäßige Überwachung der Nierenfunktion und der Serumelektrolyte erforderlich, um einen intravaskulären Volumenmangel und einen weiteren Abfall des Herzzeitvolumens und des systemischen Blutdrucks zu vermeiden.Kardiologische Mittel wie Digoxin oder Milrinon können das Herzzeitvolumen bei Patienten mit PAH verbessern, obwohl ihre langfristige Wirksamkeit unklar bleibt. Außerdem ist die Aufrechterhaltung des Sinusrhythmus wichtig, da Vorhofflimmern und supraventrikuläre Tachykardie mit dem Auftreten von Rechtsherzversagen und anschließender Mortalität verbunden sind (
91
). Intravenöses Adenosin ist die bevorzugte Behandlungsmethode bei akuten Episoden einer paroxysmalen supraventrikulären Tachykardie (PSVT). Im Gegensatz dazu sind β-adrenerge Rezeptorblocker, mit Ausnahme von Atenolol, Medikamente der ersten Wahl zur Vorbeugung von PSVT. Eine elektrische Kardioversion wird auch empfohlen, wenn Patienten mit Vorhofflimmern hämodynamisch instabil werden oder wenn bei ihnen ein hohes Mortalitätsrisiko besteht (
92
). Ibutilid- oder Flecainid-Injektionen können in Betracht gezogen werden, um Vorhofflattern und Vorhofflimmern bei PAH-Patienten mit strukturell normalen Herzen zu beseitigen (
93
). Da Patienten mit angeborenen Herzfehlern Vorhofflattern im Allgemeinen nicht gut tolerieren, sollte eine elektrische Kardioversion durchgeführt werden, um den Sinusrhythmus wiederherzustellen (
94
). Die idiopathische Tachykardie des rechtsventrikulären Ausflusstrakts ist die häufigste Art von ventrikulärer Tachykardie, die β-Rezeptorblocker, Verapamil oder andere antiarrhythmische Prophylaxemittel erfordert. Bei Versagen der medikamentösen Behandlung ist eine Katheterablation erforderlich. Wenn möglich, sollte die Katheterablation bis zum zweiten Trimester verschoben und in einem gut ausgerüsteten medizinischen Zentrum mit Experten mit umfassender Erfahrung durchgeführt werden (
95
,
96
). Außerdem kann eine gelegentliche Sinusbradykardie mit dem hypotensiven Syndrom in Rückenlage verbunden sein. Eine symptomatische Bradykardie sollte mit Veränderungen der mütterlichen Lage behandelt werden. Falls die klinischen Symptome anhalten, sollte anschließend ein temporärer Schrittmacher eingesetzt werden (
97
,
98
). Bei hämodynamisch stabilen Patienten sind temporäre Herzschrittmacher in der Regel nicht erforderlich. Sie werden jedoch während der Wehen bei Frauen mit Bradykardierisiko oder bei Frauen mit einer Synkopenanamnese empfohlen (
97
). Bei Patientinnen mit hohem Risiko für einen plötzlichen Herztod sollten implantierbare Kardioverter-Defibrillatoren auch vor einer Schwangerschaft in Betracht gezogen werden (
80
,
99
).AntikoagulanzientherapieSchwangere Frauen weisen häufig eine Hyperkoagulabilität auf, die das Thromboserisiko erhöhen kann. Wenn bei einer schwangeren Person mit PAH eine kardiopulmonale Dysfunktion festgestellt wurde, werden Antikoagulanzien zur Verringerung des Thromboserisikos empfohlen. Die Auswahl der gerinnungshemmenden Medikamente sollte umfassend unter Berücksichtigung der betroffenen Person, des Stadiums der Schwangerschaft, des mütterlichen Blutungsrisikos und teratogener Wirkungen abgewogen werden (
15
,
100
). Da niedermolekulares Heparin (NMH) geringere Auswirkungen auf den Fötus sowie ein geringeres Osteoporoserisiko aufweist, gilt es als bevorzugtes Medikament zur Vorbeugung und Behandlung venöser Thromboembolien während der Schwangerschaft und im Wochenbett. Der vorbeugende Effekt von NMH gegen Klappenthrombosen ist jedoch schwach (
38
). Wenn NMH oder unfraktioniertes Heparin (UFH) während der Schwangerschaft angewendet werden, wird empfohlen, die Anfangsdosis nach dem Gewicht der Mutter im ersten Trimenon (8.–10. Schwangerschaftswoche) zu berechnen. Die Dosis sollte anschließend durch wöchentliche Überwachung der Anti-Faktor-Xa-Spiegel oder der partiellen Thromboplastinzeit angepasst werden, bis die maximalen Anti-Xa-Spiegel nach 4 bis 6 Stunden 0,6–1,2 IU/ml erreicht haben (
1
,
101
). Fondaparinux kann sogar für PAH-Patienten in Betracht gezogen werden, wenn diese gegen NMH allergisch sind. Warfarin kann die Plazenta passieren und dosisabhängig teratogene Wirkungen haben, die zum „fetalen Warfarin-Syndrom“ führen können (
102
). Daher sollte Warfarin im ersten Trimester nur in begrenzten Dosen verwendet oder durch NMH ersetzt werden. Die Warfarin-Dosierung muss auf < 5 mg/Tag begrenzt und die International Normalized Ratio (INR) im zweiten und dritten Trimester auf 1,5–2,0 angepasst werden. Das Sicherheitsprofil von Warfarin bei Schwangeren ist jedoch nach wie vor umstritten, und daher sollte es während der Schwangerschaft wenn möglich vermieden werden
(
40
,
45
,
103–106
)
. Darüber hinaus fehlen weiterhin hochwertige Belege für die Sicherheit und Wirksamkeit neuer oraler Antikoagulanzien wie Dabigatran, Rivaroxaban und Apixaban bei schwangeren Frauen, was deren Anwendungsempfehlung verhindert (
107
,
108
). Eine Metaanalyse von 339 schwangeren Frauen, die neue direkte orale Antikoagulanzien einnahmen, ergab, dass 22,2 % Fehlgeburten erlitten und 3,6 % Föten mit Skelett- und Gesichtsdeformationen hatten (
109
). Insbesondere mussten alle Patientinnen die orale Antikoagulation während der ersten beiden Schwangerschaftsmonate absetzen, was darauf hindeutet, dass die während der Schwangerschaft angewendeten neuen oralen Antikoagulationsschemata möglicherweise mit einem höheren Risiko von Fehlgeburten und Geburtsfehlern verbunden sind (
110
).Orale Antikoagulanzien sollten 3–5 Tage vor der Entbindung durch LMWH oder UFH ersetzt werden, was die Durchführung eines Kaiserschnitts sicherer macht. LMWH sollte jedoch 12–24 Stunden vor der Entbindung abgesetzt werden, während UFH > 4–7 Tage vor der Entbindung abgesetzt werden sollte. Protaminantagonisten können vorsichtig bei Schwangeren eingesetzt werden, bei denen ein Schwangerschaftsabbruch notwendig ist, die Heparinbehandlung jedoch nicht abgebrochen wurde. Warfarin hingegen kann durch Vitamin-K1-Antagonisten antagonisiert werden (
15
,
111–113
)
.
Wenn 24 Stunden nach der Entbindung keine offensichtliche Blutung auftritt, kann die Antikoagulationstherapie wieder aufgenommen werden. Es ist jedoch zu beachten, dass Patientinnen, die zuvor mit Warfarin behandelt wurden, stattdessen LMWH erhalten und der INR-Wert mehrere Tage nach der Entbindung überwacht werden sollte. LMWH kann dann abgesetzt werden, wenn Warfarin zu wirken beginnt.PAH-spezifische TherapieDie derzeit verfügbaren Medikamente, die auf die pathologischen Bahnen abzielen, die der PAH zugrunde liegen, führten zwar nicht zu einer vollständigen Umkehrung der Erkrankung, senkten aber nachweislich den pulmonalarteriellen Druck und linderten die klinischen Symptome. Bei Patienten mit stabiler Hämodynamik wird die routinemäßige Anwendung von Vasodilatatoren und anderen Medikamenten, die die Hämodynamik beeinträchtigen können, nicht empfohlen. Bei Patienten mit instabiler Hämodynamik kann jedoch die kumulative Gabe von pulmonalen Vasodilatatoren zu den bestehenden allgemeinen Behandlungsschemata das Risiko der Müttersterblichkeit und von ungünstigen Schwangerschaftsausgängen deutlich senken (
14
,
114
). Zu diesen Vasodilatatoren zählen Kalziumkanalblocker (CCB) (
4
,
6
,
115
), Prostaglandine und assoziierte Analoga (
7
,
50
,
51
,
55
,
116
) sowie Phosphodiesterasehemmer (PDE-I) (
117
), jedoch keine Endothelin-Rezeptorantagonisten aufgrund des teratogenen Potenzials (
118
,
119
). Pieper et al. schlugen vor, mit der medikamentösen Behandlung der PAH mindestens drei Monate vor der Entbindung zu beginnen, da die optimale Wirkung erst drei Monate später eintrat (
14
). Da jedoch die Anwendung pulmonaler Vasodilatatoren bei Schwangeren die Sicherheit des Fötus gefährden kann, muss ihre Anwendung mit ihren Standardformulierungen und -anwendungen evaluiert werden, was zusätzliche Unterstützung durch hochwertige, evidenzbasierte Forschung erfordert.Prostaglandine und AnalogaProstacyclin kann die Proliferation glatter Muskeln hemmen, die Gefäßumgestaltung umkehren, den pulmonalen und systemischen Kreislauf erweitern, die Funktion des rechten Ventrikels verbessern und eine thrombozytenaggregationshemmende Wirkung haben (
120
). Allerdings können Thrombozytopenie und blutungsbedingte Komplikationen auftreten, wenn die Patienten gleichzeitig mit Antikoagulanzien und Prostacyclin behandelt werden. Daher sollten die Blutwerte und die Gerinnungsparameter engmaschig überwacht werden (
45
)
. Indikationen für den Beginn der Anwendung von Prostaglandinen sind typischerweise Patienten mit PAH der WHO-FC-Klasse III-IV oder eingeschränkter Funktion des rechten Ventrikels ( 88
,
121-123
)
.Derzeit ist Epoprostenol das am häufigsten verwendete zielgerichtete Medikament bei schwangeren Frauen mit PAH (62 %) und das Medikament der ersten Wahl zur Behandlung von Schwangerschaften mit PAH oder Eisenmenger-Syndrom ( 52
,
124–126
)
. Epoprostenol kann die körperliche Belastbarkeit, Lebensqualität und Überlebensrate verbessern (
120
). Aufgrund des langsamen Wirkungseintritts und der kurzen Halbwertszeit wird empfohlen, die Behandlung mit diesem Medikament mindestens 8 Wochen vor der Entbindung über einen zentralen Venenkatheter zu beginnen (
120
). Es kann auch postpartal zur Vorbeugung einer pulmonalarteriellen Hypertoniekrise und einer Rechtsherzinsuffizienz verwendet werden (
127
,
128 ). Zur Sicherheit dieses Medikaments für den Fötus liegen keine Daten und Erfahrungen
vor
, aber mehrere Studien haben gezeigt, dass es im dritten Trimenon keine fetalen Missbildungen oder intrauterine Wachstumsstörungen verursacht hat (
55
,
116
). Zu den Nebenwirkungen, die mit der Langzeitanwendung von Epoprostenol verbunden sind, können Gesichtsrötung, Kopfschmerzen, Durchfall, Bauchschmerzen, Gebärmutterkontraktionen und postpartale Blutungen gehören. Eine Dosisreduktion ist jedoch nur erforderlich, wenn die Nebenwirkungen schwerwiegend werden.Iloprost ist ein inhaliertes Prostacyclin-Analogon, das häufig zur Linderung von Dyspnoe während chirurgischer Eingriffe eingesetzt wird. Der Wirkungseintritt beträgt im Allgemeinen 15–20 Minuten, und die Wirkungsdauer beträgt 1–2 Stunden (
125
,
127
,
129
). Im Vergleich zur intravenösen Verabreichung neigt die kurzfristige Anwendung von Iloprost-Aerosol-Inhalationen dazu, den pulmonalarteriellen Druck wirksamer zu senken (
6
,
7
,
55
). Derzeit gibt es keine Hinweise darauf, dass inhaliertes Iloprost Müttersterblichkeit oder angeborene fetale Anomalien verursachen kann. Es gibt jedoch Hinweise darauf, dass die Inhalation von Iloprost innerhalb von 24 Schwangerschaftswochen und in der perinatalen Periode das Risiko fetaler Missbildungen und Mortalität signifikant senken kann (
55
,
114
,
130
). Es ist zu beachten, dass intravenöses Epoprostenol verabreicht werden sollte, wenn sich die Krankheit nach Inhalation von Iloprost verschlimmert (
52
,
114
). Inhalative Prostaglandine werden im Allgemeinen bei Patienten mit weniger schweren PAH-Symptomen eingesetzt, da die intermittierende Verabreichung mittels Vernebelung eine kurze Halbwertszeit hat und es zu einem erneuten Anstieg des pulmonalarteriellen Drucks kommen kann (
13
,
55
). Es ist jedoch ein Zeichen für einen ernsten Zustand, wenn Patienten mit PAH Iloprost vor der Empfängnis einnehmen.Treprostinil kann auf verschiedene Weise verabreicht werden, einschließlich subkutaner Infusion, intravenöser und oraler Verabreichung (
131
). Dieses Medikament kann bei Patienten mit Herzfunktionsklasse II-IV der WHO oder PAH der NYHA-Klasse III-IV eingesetzt werden. Es wurde berichtet, dass es die 6-Minuten-Gehstrecke, die periphere Blutsauerstoffsättigung und die Herzfunktion signifikant verbessert (
132
). Einige Patienten (etwa 8 %) lehnten die Einnahme dieses Medikaments jedoch aufgrund der Schmerzen an der Infusionsstelle ab (
133
).CCBsEinige schwangere Frauen mit PAH können von CCBs profitieren. CCBs werden jedoch normalerweise nur bei Patienten angewendet, deren Testergebnisse für akute pulmonale Vasodilatation positiv sind (
4
,
6
,
85
,
115
). Diltiazem ist das CCB der ersten Wahl für Patienten mit schnellem Herzrhythmus, während Nifedipin für Patienten mit langsamem Herzrhythmus verwendet wird. Zunächst sollte die Mindestdosis verwendet und die Dosis schrittweise entsprechend Blutdruck, Herzrhythmus, Herzfrequenz, EKG-Ergebnissen und klinischen Symptomen erhöht werden, bis die maximal verträgliche Dosis erreicht ist. Wenn die Struktur und Funktion des rechten Herzens auf physiologischem Niveau bleiben und der pulmonalarterielle Druck nach der CCB-Therapie normal oder annähernd normal ist (mittlerer pulmonalarterieller Druck ≤ 30 mmHg und pulmonaler Gefäßwiderstand < 4 WU), kann davon ausgegangen werden, dass der Patient kontinuierlich auf CCBs empfindlich reagiert, was bedeutet, dass die CCBs chronisch angewendet werden können. Wenn keine zufriedenstellende Reaktion eintritt, sollte eine zusätzliche PAH-Therapie eingeleitet werden. Verschiedene Studien haben jedoch gezeigt, dass CCBs keine langfristigen vasodilatatorischen Effekte bei Patienten mit PAH hervorrufen können. Eine Exposition gegenüber CCBs im dritten Trimester kann das Risiko für Krampfanfälle bei Neugeborenen erhöhen (Odd Ratio = 3,6) (
134
,
135
). Daher muss eine schrittweise Umstellung von CCBs auf Prostaglandine oder Analoga oder PDE-I in Betracht gezogen werden, wenn die Herzfunktion und der pulmonalarterielle Druck nicht auf einem normalen Niveau gehalten werden können (
127
).PDE-IPDE-5-Hemmer sind das bevorzugte Medikament für Frauen mit PAH der WHO-Herzfunktionsklasse I-II oder normaler rechtsventrikulärer Funktion (
5
,
71
,
136
). Die Expressionsgrade von PDE-5 im rechtsventrikulären Myokard sind bei Patientinnen mit PAH häufig erhöht. PDE-5-Hemmer können diese Veränderung umkehren, indem sie die Gefäßglattmuskulatur entspannen und den pulmonalarteriellen Druck senken (
6
). Darüber hinaus verändert die Verwendung von PDE-5-Hemmern weder den Laktatspiegel noch den pH-Wert des Fötus. Sildenafil ist der am häufigsten angewendete PDE-5-Hemmer. Es wurde bereits festgestellt, dass Sildenafil die klinischen Symptome, die Herzfunktion, die hämodynamischen Indizes und den Schwangerschaftsverlauf signifikant verbessern kann (
111
). Es kann auch die Rate erfolgreicher vaginaler Entbindungen erhöhen und die Häufigkeit von Frühgeburten oder Säuglingen mit geringem Geburtsgewicht verringern (
130
,
136
,
137
). Wenn sich die Herzfunktion weiter verschlechtert und der pulmonalvaskuläre Widerstand nach oraler Sildenafil-Behandlung steigt, kann die Inhalation von Iloprost zur Linderung der Symptome in Betracht gezogen werden (
136
,
137
). Darüber hinaus zeigte eine frühere Studie, dass fünf schwangere Frauen mit PAH, die PDE-5-Hemmer und Prostacyclin intravenös erhielten, bei der Langzeitnachbeobachtung in der Stillzeit keine signifikanten Komplikationen bei Mutter und Kind aufwiesen (
84
).Obwohl Sildenafil weit verbreitet ist, muss seine Sicherheit während der Schwangerschaft noch weiter untersucht werden. Eine Studie aus dem Jahr 2021 mit 77 Säuglingen von Frauen, die während der Schwangerschaft mit PDE-5-Hemmern behandelt wurden, ergab, dass neun Säuglinge Frühgeborene waren, sechs für ihr Gestationsalter zu klein waren, fünf bei ihren 5-Minuten-Tests für Aussehen, Puls, Grimasse, Aktivität und Atmung einen Wert von < 8 erreichten, 18 auf die Neugeborenen-Intensivstation eingeliefert wurden und bei acht Säuglingen Atemwegs- und Herz-Kreislauf-Erkrankungen diagnostiziert wurden (
138
). Darüber hinaus gibt es derzeit keine klinischen Belege für die Wirksamkeit von Vardenafil und Tadalafil bei schwangeren Frauen mit PAH.StatineNeben hypolipidämischen Effekten wurden von Statinen auch entzündungshemmende, antiproliferative und apoptotische Wirkungen berichtet. Zahlreiche klinische und experimentelle Studien haben gezeigt, dass Statine den pulmonalarteriellen Druck senken und die pulmonale vaskuläre Umgestaltung verbessern können, indem sie die Apoptose fördern, die Zellproliferation hemmen, entzündungshemmende Wirkungen haben, die Rho-Kinase-Signalgebung und die Endothelin-1-Freisetzung hemmen (
139
–
142
). Obwohl Statine auch die Rate an Geburtsfehlern oder die Rate an fetaler Teratogenität nicht erhöhten, war die Stichprobengröße relativ klein (
78
). Obwohl Statine derzeit im Allgemeinen während der Schwangerschaft und Stillzeit nicht empfohlen werden, können sie zur Langzeitbehandlung von postpartaler PAH nach der Stillzeit verwendet werden (
66
,
79
).ECMOECMO ist eine fortschrittliche Technologie zur Atmungs- und Kreislaufunterstützung, die für Patienten mit akutem, reversiblem Atemversagen vorgeschlagen wurde (
143
). ECMO kann den Sauerstoffsättigungsstatus von Patienten mit PAH aufrechterhalten, wenn die Herzfunktion dekompensiert ist (
144
,
145
). Verschiedene Fallberichte deuteten darauf hin, dass die ECMO-Behandlung bei der Mehrzahl der schwangeren Frauen mit PAH zu günstigen Schwangerschaftsergebnissen führte (
146
–
148
). Es wurde jedoch auch von Patienten mit PAH berichtet, die ECMO erhielten, die aufgrund einer schweren Rechtsherzinsuffizienz drei Monate nach der Entbindung nicht überlebten (
149
). Außerdem erfordert der kontinuierliche Betrieb von ECMO eine systemische Antikoagulation, wobei das kontinuierliche Nässen aus dem Operationsschnitt zu schweren Gerinnungsstörungen führen kann (
150
,
151
). Aufgrund der bisher berichteten geringen Stichprobengröße sind weitere Studien mit größeren Stichproben erforderlich.Operative TherapieEine PAH als Folge einer bekannten kardiopulmonalen Erkrankung erfordert eine aggressive Behandlung der Primärerkrankung mit Verfahren wie biventrikulärer Stimulation und Herzoperationen (
85
). Eine Herzoperation mit kardiopulmonalem Bypass kann bei Patientinnen erwogen werden, die auf eine medikamentöse Therapie angesprochen haben, bei denen aber die Möglichkeit einer Operation besteht. Die Operation sollte zwischen der 13. und 28. Schwangerschaftswoche durchgeführt werden. Liegt die Schwangerschaftswoche über 26 Wochen, kann vor der Durchführung der kardiopulmonalen Bypass-Operation ein Kaiserschnitt zur Beendigung der Schwangerschaft in Erwägung gezogen werden. Liegt die Schwangerschaftswoche über 28 Wochen, kann nach einer vaginalen Entbindung eine Herzoperation erwogen werden. Allerdings bleibt das Risiko mütterlicher und fetaler Mortalität auch während einer kardiopulmonalen Bypass-Operation hoch. Eine Herzoperation wird nur empfohlen, wenn Medikamente oder andere interventionelle Therapien versagen und die Schwangere in Lebensgefahr schwebt (
1
,
88
,
152
).Bei Patienten mit chronisch thromboembolischer PAH ist die pulmonale Endarteriektomie eine mögliche kurative Methode, obwohl nicht alle Patienten für diese Form der chirurgischen Behandlung geeignet sind. Bei chronisch thromboembolischer PAH kann auch eine postpartale Thrombektomie oder Lungentransplantation erforderlich sein (
146
). Hochrisikopatientinnen, die sich für eine Fortsetzung der Schwangerschaft entscheiden, sollten umgehend auf eine Lungentransplantation untersucht werden (
6
).SchlussfolgerungenPAH gilt als irreversible Krankheit. Bei PAH jeder Schwere wird eine strikte Empfängnisverhütung oder ein frühzeitiger Schwangerschaftsabbruch empfohlen. Eine effektive frühzeitige Behandlung ist jedoch wichtig, um die Prognose schwangerer Frauen mit PAH zu verbessern, bei denen PAH erstmals während der Schwangerschaft entdeckt wurde oder die die Schwangerschaft unbedingt fortsetzen müssen. Strategien wie Antikoagulationstherapie, PAH-spezifische Therapie und operative Therapie sollten in Betracht gezogen werden. Da eine Schwangerschaft mit PAH eine seltene Erkrankung ist, handelt es sich bei den meisten relevanten Studien um retrospektive Studien, die auf Fallberichten und Fallserienanalysen basieren und nur über einen geringen Grad an evidenzbasierter medizinischer Evidenz verfügen. Daher sollten in Zukunft zusätzliche prospektive Multicenterstudien durchgeführt werden, um die klinischen Behandlungsstrategien für schwangere Frauen mit PAH zu optimieren.


- 1 Abteilung für Gynäkologie und Geburtshilfe, Beijing Hospital, Nationales Zentrum für Gerontologie, Peking, China
- 2 Institut für Geriatrische Medizin, Chinesische Akademie der Medizinischen Wissenschaften, Peking, China
- 3 Peking Union Medical College, Graduiertenschule des Peking Union Medical College, Chinesische Akademie der Medizinischen Wissenschaften, Peking, China
- 4 Abteilung für Urologie, Changhai Hospital, Naval Medical University, Shanghai, China



OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Bitte Anmelden oder Registrieren um der Konversation beizutreten.
