- Beiträge: 1755
Sidebar
COPD, PH, inhalatives Prostacyclin
13 Aug 2024 13:07 #2176
von danny
OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
COPD, PH, inhalatives Prostacyclin wurde erstellt von danny
www.frontiersin.org/journals/medicine/ar...2023.1217156/fullAuf den Prostazyklin-Stoffwechselweg abzielende Inhalationstherapien bei pulmonaler Hypertonie aufgrund von COPD: systematische Übersicht
 Abdullah A. Alqarni
1,2 *
Abdullah A. Alqarni
1,2 *
 Abdulelah M. Aldhahir
3
Abdulelah M. Aldhahir
3
 Heba M. Bintalib
4,5
Heba M. Bintalib
4,5
 Jaber S. Alqahtani
6
Rayan A. Siraj 7
Jaber S. Alqahtani
6
Rayan A. Siraj 7
 Mansour Majrshi
8,9
Abdulkareem A. AlGarni 10,11
Mansour Majrshi
8,9
Abdulkareem A. AlGarni 10,11
 Abdallah Y. Naser
12
Sara A. Alghamdi 13
Abdallah Y. Naser
12
Sara A. Alghamdi 13
 Hassan Alwafi
14
Hassan Alwafi
14
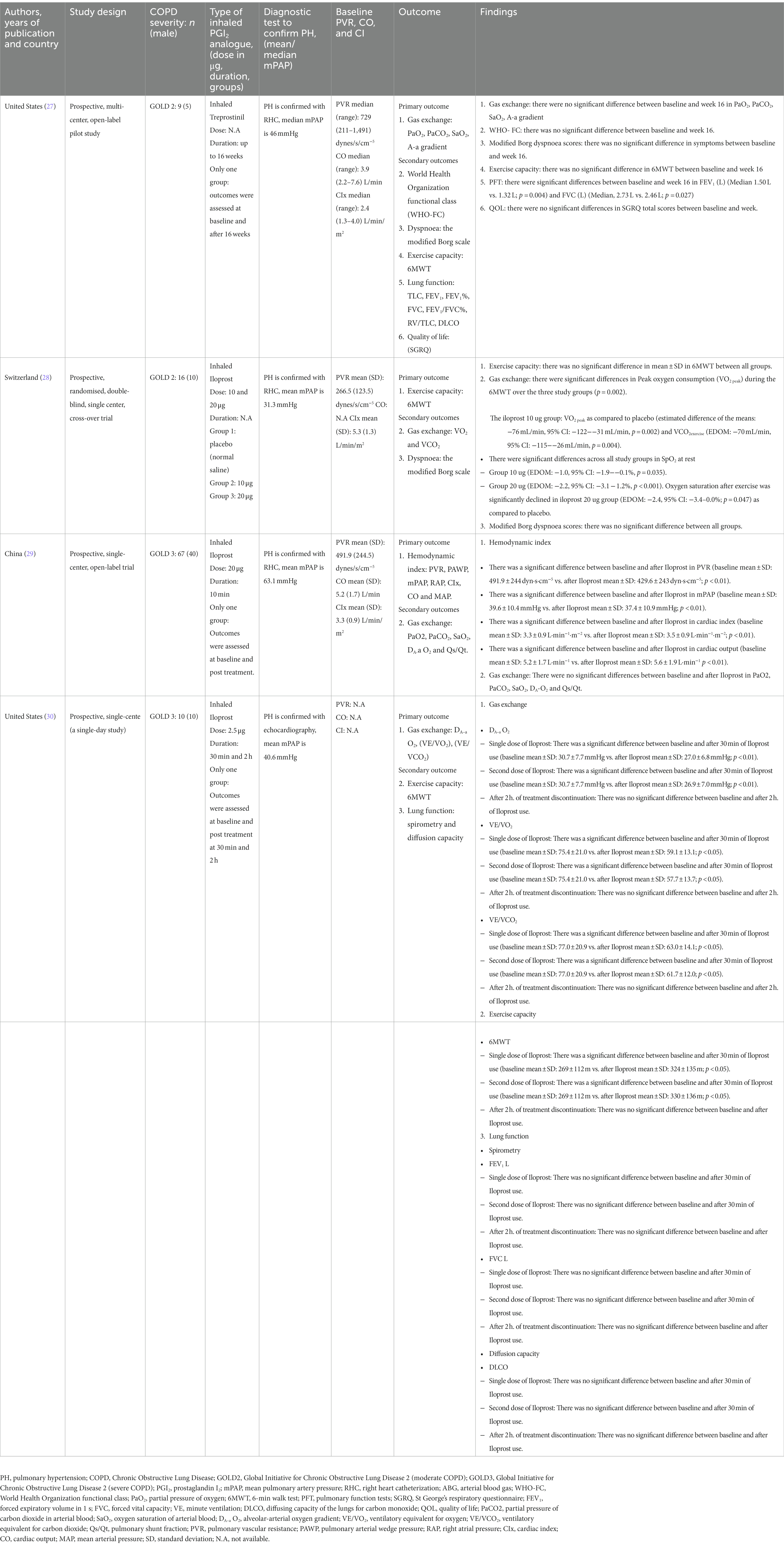 Tabelle 1. Zusammenfassung der eingeschlossenen Studien. 2.1. DatenauswahlMit Unterstützung eines Fachbibliothekars durchsuchten wir die elektronischen Datenbanken von Medline, Embase, Scopus und Cochrane von Beginn an bis zum 1. Februar 2023 nach Veröffentlichungen zur Behandlung von COPD-Patienten mit inhaliertem Prostacyclin (Suchstrategie siehe
Anhang S1
). Eingeschlossen wurden Artikel, die erwachsene Patienten mit einer bestätigten Diagnose von COPD-assoziierter pulmonaler Hypertonie beschreiben, die inhalierte Medikamente erhielten, die auf den Prostacyclin-Stoffwechselweg abzielen (z. B. Iloprost, Treprostinil und Flolan). Ausgeschlossen wurden Fallberichte, systematische Übersichtsarbeiten, Übersichtsartikel, Konferenzzusammenfassungen ohne Volltext (da sie nicht peer-reviewed waren), Artikel ohne Volltext, nicht englischsprachige Manuskripte, Meinungsartikel und Buchkapitel. Wir haben keine Mindeststichprobengröße für die Aufnahme in die Studie festgelegt. Um gezielte klinische Fragen zu entwickeln, verwendeten wir in unserer Suchstrategie das PICO-Framework: P: Population (Patienten mit einer bestätigten Diagnose einer COPD-bedingten pulmonalen Hypertonie), I: Intervention (inhalierte Medikamente, die auf den Prostacyclin-Stoffwechselweg abzielen), C: Vergleich (Placebo, übliche Behandlung), O: Ergebnis (Gasaustausch, körperliche Belastbarkeit, Schwere der Dyspnoe, Lungenfunktion und pulmonale Hämodynamik).2.2. Qualitative Bewertung der StudienmethodikDie Bewertung der Studienqualität wurde von zwei Autoren (AAlq und AAld) durchgeführt. Zur Bewertung der Qualität der in diesen Review einbezogenen Studien verwendeten wir Cochrane-Tools für das Verzerrungsrisiko (siehe
Anhänge S2
und
S3
). Für randomisierte Crossover-Studien verwendeten wir das überarbeitete Cochrane-Tool für das Verzerrungsrisiko (
31
). Das Tool umfasst sieben Bereiche: Verzerrungsrisiko aufgrund des Randomisierungsprozesses, Verzerrung aufgrund von Perioden- und Carryover-Effekten, Verzerrung aufgrund von Abweichungen von den beabsichtigten Interventionen, Verzerrung aufgrund von Abweichungen von den beabsichtigten Interventionen, Verzerrung aufgrund fehlender Ergebnisdaten, Verzerrung bei der Messung des Ergebnisses und Verzerrung bei der Auswahl des berichteten Ergebnisses. Zur Bewertung nicht randomisierter klinischer Studien wurde das Cochrane-Tool für die Bewertung des Verzerrungsrisikos in nicht randomisierten Studien verwendet (
32
). Das Tool besteht aus sieben Domänen und ähnelt dem für randomisierte Crossover-Studien verwendeten Tool, mit Ausnahme der ersten drei Domänen, bei denen sich Tools für nicht randomisierte klinische Studien auf Verzerrungen aufgrund von Störfaktoren, Verzerrungen bei der Auswahl der Studienteilnehmer und Verzerrungen bei der Klassifizierung der Interventionen konzentrieren. In jeder Domäne beantworteten die Autoren (AAlq und AAld) mehrere Fragen und stuften anschließend das Verzerrungsrisiko als niedrig, mittel oder hoch ein. Die Studie wurde als mit geringem Verzerrungsrisiko behaftet eingestuft, wenn alle Domänen als mit geringem Verzerrungsrisiko eingestuft wurden. Die Studie wurde als mit mittlerem Verzerrungsrisiko (nicht randomisierte klinische Studie) behaftet bzw. als bedenklich eingestuft (randomisierte Crossover-Studie), wenn die Domänen als niedriges Risiko gekennzeichnet waren und mindestens eine Domäne ein mittleres Verzerrungsrisiko aufwies.3. ErgebnisseDie Suche ergab zunächst 1.786 Studien, die als potenziell geeignet erachtet wurden. Nach dem Entfernen von Duplikaten wurden 1.324 Titel und Abstracts durchgesehen. Die Durchsicht der Titel und Abstracts ergab 31 Studien, die gemäß den Einschluss- und Ausschlusskriterien bewertet wurden. Von den 31 Studien wurden 22 ausgeschlossen, da es sich entweder um Konferenzabstracts handelte oder keine Volltexte verfügbar waren. Somit wurden neun Studien für die Lektüre des Volltextes in Betracht gezogen. Nach der Lektüre der Volltexte der neun verbleibenden Studien erfüllten vier Studien unsere Einschlusskriterien und wurden in diese systematische Übersichtsarbeit aufgenommen; siehe
Abbildung 1
. ABILDUNG 1
Tabelle 1. Zusammenfassung der eingeschlossenen Studien. 2.1. DatenauswahlMit Unterstützung eines Fachbibliothekars durchsuchten wir die elektronischen Datenbanken von Medline, Embase, Scopus und Cochrane von Beginn an bis zum 1. Februar 2023 nach Veröffentlichungen zur Behandlung von COPD-Patienten mit inhaliertem Prostacyclin (Suchstrategie siehe
Anhang S1
). Eingeschlossen wurden Artikel, die erwachsene Patienten mit einer bestätigten Diagnose von COPD-assoziierter pulmonaler Hypertonie beschreiben, die inhalierte Medikamente erhielten, die auf den Prostacyclin-Stoffwechselweg abzielen (z. B. Iloprost, Treprostinil und Flolan). Ausgeschlossen wurden Fallberichte, systematische Übersichtsarbeiten, Übersichtsartikel, Konferenzzusammenfassungen ohne Volltext (da sie nicht peer-reviewed waren), Artikel ohne Volltext, nicht englischsprachige Manuskripte, Meinungsartikel und Buchkapitel. Wir haben keine Mindeststichprobengröße für die Aufnahme in die Studie festgelegt. Um gezielte klinische Fragen zu entwickeln, verwendeten wir in unserer Suchstrategie das PICO-Framework: P: Population (Patienten mit einer bestätigten Diagnose einer COPD-bedingten pulmonalen Hypertonie), I: Intervention (inhalierte Medikamente, die auf den Prostacyclin-Stoffwechselweg abzielen), C: Vergleich (Placebo, übliche Behandlung), O: Ergebnis (Gasaustausch, körperliche Belastbarkeit, Schwere der Dyspnoe, Lungenfunktion und pulmonale Hämodynamik).2.2. Qualitative Bewertung der StudienmethodikDie Bewertung der Studienqualität wurde von zwei Autoren (AAlq und AAld) durchgeführt. Zur Bewertung der Qualität der in diesen Review einbezogenen Studien verwendeten wir Cochrane-Tools für das Verzerrungsrisiko (siehe
Anhänge S2
und
S3
). Für randomisierte Crossover-Studien verwendeten wir das überarbeitete Cochrane-Tool für das Verzerrungsrisiko (
31
). Das Tool umfasst sieben Bereiche: Verzerrungsrisiko aufgrund des Randomisierungsprozesses, Verzerrung aufgrund von Perioden- und Carryover-Effekten, Verzerrung aufgrund von Abweichungen von den beabsichtigten Interventionen, Verzerrung aufgrund von Abweichungen von den beabsichtigten Interventionen, Verzerrung aufgrund fehlender Ergebnisdaten, Verzerrung bei der Messung des Ergebnisses und Verzerrung bei der Auswahl des berichteten Ergebnisses. Zur Bewertung nicht randomisierter klinischer Studien wurde das Cochrane-Tool für die Bewertung des Verzerrungsrisikos in nicht randomisierten Studien verwendet (
32
). Das Tool besteht aus sieben Domänen und ähnelt dem für randomisierte Crossover-Studien verwendeten Tool, mit Ausnahme der ersten drei Domänen, bei denen sich Tools für nicht randomisierte klinische Studien auf Verzerrungen aufgrund von Störfaktoren, Verzerrungen bei der Auswahl der Studienteilnehmer und Verzerrungen bei der Klassifizierung der Interventionen konzentrieren. In jeder Domäne beantworteten die Autoren (AAlq und AAld) mehrere Fragen und stuften anschließend das Verzerrungsrisiko als niedrig, mittel oder hoch ein. Die Studie wurde als mit geringem Verzerrungsrisiko behaftet eingestuft, wenn alle Domänen als mit geringem Verzerrungsrisiko eingestuft wurden. Die Studie wurde als mit mittlerem Verzerrungsrisiko (nicht randomisierte klinische Studie) behaftet bzw. als bedenklich eingestuft (randomisierte Crossover-Studie), wenn die Domänen als niedriges Risiko gekennzeichnet waren und mindestens eine Domäne ein mittleres Verzerrungsrisiko aufwies.3. ErgebnisseDie Suche ergab zunächst 1.786 Studien, die als potenziell geeignet erachtet wurden. Nach dem Entfernen von Duplikaten wurden 1.324 Titel und Abstracts durchgesehen. Die Durchsicht der Titel und Abstracts ergab 31 Studien, die gemäß den Einschluss- und Ausschlusskriterien bewertet wurden. Von den 31 Studien wurden 22 ausgeschlossen, da es sich entweder um Konferenzabstracts handelte oder keine Volltexte verfügbar waren. Somit wurden neun Studien für die Lektüre des Volltextes in Betracht gezogen. Nach der Lektüre der Volltexte der neun verbleibenden Studien erfüllten vier Studien unsere Einschlusskriterien und wurden in diese systematische Übersichtsarbeit aufgenommen; siehe
Abbildung 1
. ABILDUNG 1
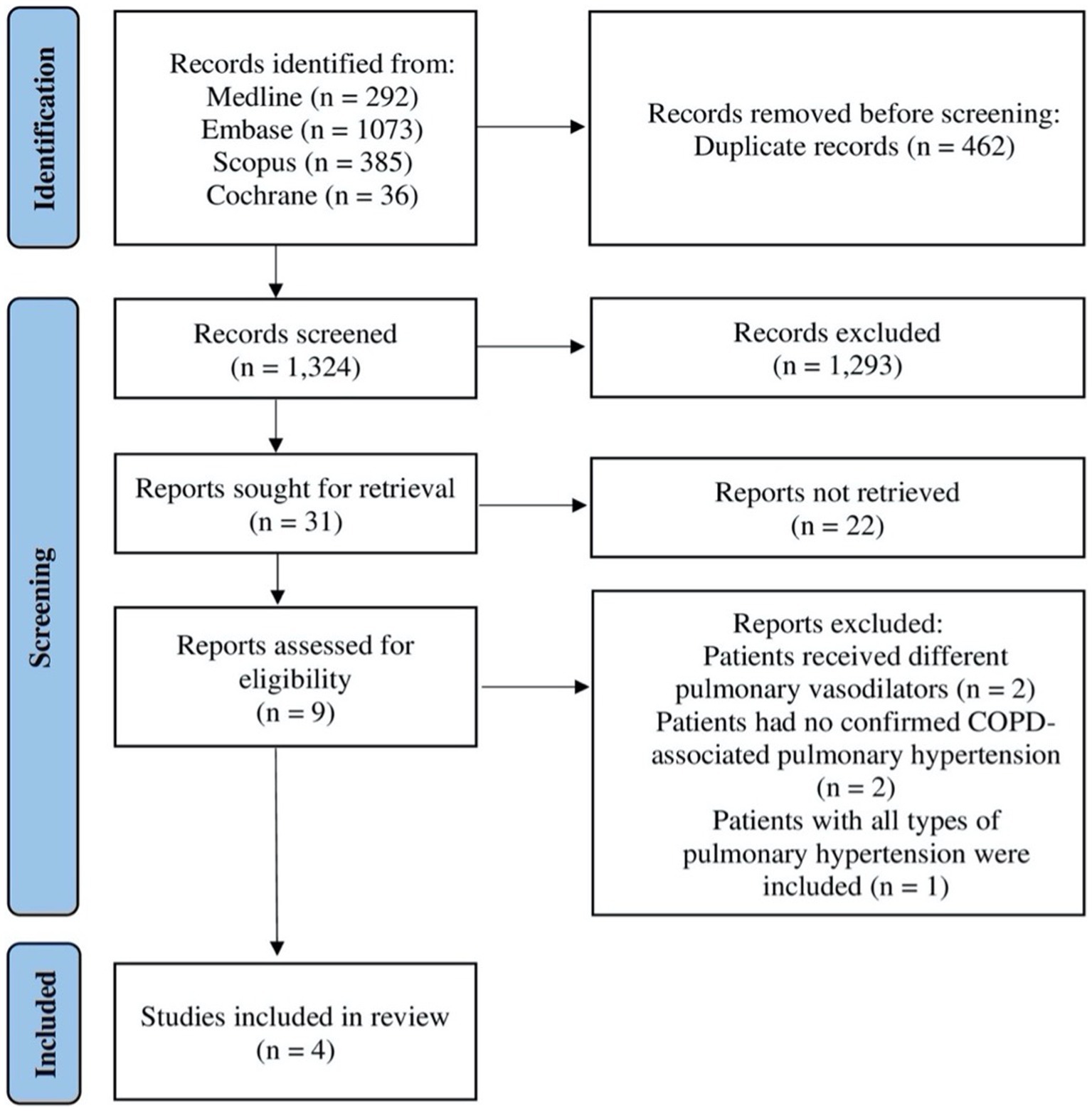 Abbildung 1. Flussdiagramm zur Veranschaulichung der systematischen Such- und Screeningstrategie auf Grundlage der Leitlinien für bevorzugte Berichtselemente für systematische Überprüfungen und Metaanalysen, einschließlich der Anzahl der Studien, die die Eignungskriterien erfüllen, und der Anzahl der ausgeschlossenen Studien. COPD: chronisch obstruktive Lungenerkrankung. 3.1. Die Beschreibung der eingeschlossenen StudienDie vier eingeschlossenen Studien umfassten eine prospektive, multizentrische, offene Pilotstudie mit einer Stichprobengröße von neun COPD-Patienten, die in den USA durchgeführt und 2017 veröffentlicht wurde (
27
), eine prospektive, randomisierte, doppelblinde, monozentrische Crossover-Studie mit einer Stichprobengröße von 16 COPD-Patienten, die in der Schweiz durchgeführt und 2012 veröffentlicht wurde (
28
), eine prospektive, monozentrische, offene Studie mit einer Stichprobengröße von 67 COPD-Patienten, die in China durchgeführt und 2017 veröffentlicht wurde (
29
), und eine prospektive Beobachtungsstudie mit einer Stichprobengröße von 10 COPD-Patienten, die in den USA durchgeführt und 2010 veröffentlicht wurde (
30
). Eine vollständige Beschreibung der eingeschlossenen Studien finden Sie in
Tabelle 1
.3.2. GasaustauschDie Verwendung des inhalativen Prostazyklin-Analogons Treprostinil oder Iloprost hatte im Vergleich mit Ausgangswerten in zwei Studien (27, 29) keinen signifikanten Einfluss auf die Gasaustauschparameter (gemessen anhand des Sauerstoffpartialdrucks im arteriellen Blut (PaO2 ) , des Kohlendioxidpartialdrucks im arteriellen Blut (PaCO2 ) , der arteriellen Sauerstoffsättigung (SaO2 ) , der pulmonalen Shuntfraktion (Qs/Qt) und des alveolar-arteriellen Sauerstoffkonzentrationsgradienten (Aa-Gradient). Im Gegensatz dazu wurde in
einer
Studie
festgestellt
, dass die Verwendung des inhalativen Prostazyklin-Analogons (Iloprost) alle Gasaustauschparameter (gemessen anhand des Aa-Gradienten, des Verhältnisses Minutenventilation (VE)/Kohlendioxidproduktion (VE/VCO2 ) und des Verhältnisses VE/Sauerstoffverbrauch (VE/VO2 ) ) im Vergleich mit Ausgangswerten nach 30-minütiger Inhalation der ersten und zweiten Dosis Iloprost signifikant verbesserte (
30
). Als diese Parameter jedoch 2 Stunden nach der Anwendung von Iloprost erneut gemessen wurden, waren alle Gasaustauschparameter wieder auf den Ausgangswert zurückgekehrt. Zusammengenommen lassen diese Beobachtungen darauf schließen, dass es unwahrscheinlich ist, dass die Inhalation eines Prostacyclin-Analogons (Treprostinil oder Iloprost) die Gasaustauschparameter bei Patienten mit pulmonaler Hypertonie aufgrund von COPD verbessern oder verschlechtern kann.3.3. TrainingskapazitätDie körperliche Belastbarkeit wurde in drei Studien (
27
,
28
,
30
) berichtet, in denen die Wirksamkeit von inhaliertem Prostazyklin im 6MGT bei COPD-Patienten mit pulmonaler Hypertonie beurteilt wurde. Zwei Studien berichteten von keinem signifikanten Effekt von inhaliertem Prostazyklin im Vergleich zum 6MGT-Ausgangswert (
27
) oder zur Placebogruppe (
28
). Nur eine Studie berichtete von einer signifikanten Verbesserung des 6MGT im Vergleich zum Ausgangswert bei COPD-Patienten mit pulmonaler Hypertonie (
30
). Laut einer prospektiven, multizentrischen, offenen Pilotstudie von Bajwa et al. (
27
) verbesserte inhaliertes Treprostinil die 6MGT-Distanz bei einer Beurteilung in Woche 16 bei neun COPD-Patienten mit mittelschwerer Erkrankung und pulmonaler Hypertonie nicht signifikant (
27
). Im Gegensatz dazu zeigte eine Kohortenstudie von Dernaika et al. (27) eine signifikante Verbesserung der 6MGT-Distanz bei (
30
) verbesserte eine Einzeldosis (Mittelwert ± SD zu Studienbeginn: 269 ± 112 m vs. Mittelwert nach Iloprost ± SD: 324 ± 135 m; p < 0,05) und eine zweite Dosis (Mittelwert ± SD zu Studienbeginn: 269 ± 112 m vs. Mittelwert nach Iloprost ± SD: 330 ± 136 m; p < 0,05) von inhaliertem Iloprost die 6MWT-Distanz im Vergleich zum Ausgangswert signifikant, wenn sie 30 Minuten nach der Behandlung bei zehn Patienten mit schwerer COPD und pulmonaler Hypertonie beurteilt wurde (
30
).3.4. LungenfunktionIn zwei Studien wurden Spirometrieparameter und Diffusionskapazitätstests als sekundäre Ergebnisse verwendet, um die Wirksamkeit von inhaliertem Prostacyclin zu beurteilen (
27
,
30
). Die Anwendung des inhalierten Prostacyclin-Analogons Treprostinil verringerte FEV1 und die forcierte Vitalkapazität (FVC), hatte jedoch keinen Einfluss auf die Diffusionskapazität der Lunge für Kohlenmonoxid (DLCO) in einer prospektiven, multizentrischen, offenen Pilotstudie mit einer Stichprobengröße von neun COPD-Patienten mit pulmonaler Hypertonie (
27
). Im Gegensatz zu diesen Befunden wurden Verbesserungen bei FEV1 und FVC (aber nicht bei DLCO) 30 Minuten nach Anwendung der ersten und zweiten Dosis von inhaliertem Iloprost im Vergleich zu den Ausgangsmessungen berichtet (
30
). Messungen der gleichen Parameter wurden 2 Stunden nach Anwendung von Iloprost vorgenommen. Interessanterweise waren weder die Spirometrieparameter noch die DLCO im Vergleich zum Ausgangswert beeinträchtigt (
30
). Diese Beobachtungen legen nahe, dass inhaliertes Prostacyclin die Lungenfunktion bei Patienten mit pulmonaler Hypertonie aufgrund von COPD wahrscheinlich nicht verbessert.3.5. Schweregrad der DyspnoeDer Schweregrad der Dyspnoe wurde in zwei Studien (
27
,
28
) mithilfe der modifizierten Borg-Skala gemessen, um die Wirksamkeit von inhaliertem Prostacyclin bei COPD-Patienten mit pulmonaler Hypertonie einzuschätzen. Zwei Studien berichteten von keinem signifikanten Effekt von inhaliertem Prostacyclin im Vergleich zur Ausgangsgruppe (
27
) oder zur Placebogruppe (
28
). Laut einer prospektiven, multizentrischen, offenen Pilotstudie von Bajwa et al. (
27
) verbesserte inhaliertes Treprostinil den Schweregrad der Dyspnoe bei einer Beurteilung in Woche 16 bei neun COPD-Patienten mit mittelschwerem Schweregrad und pulmonaler Hypertonie nicht signifikant (
27
). Darüber hinaus zeigten Boeck et al. in einer prospektiven, randomisierten, doppelblinden, monozentrischen Crossover-Studie keine signifikanten Verbesserungen. (
28
) verbesserte inhaliertes Iloprost den Schweregrad der Dyspnoe im Vergleich zur Placebogruppe bei 16 COPD-Patienten mit mittelschwerer Erkrankung und pulmonaler Hypertonie nicht signifikant (
28
).3.6. Die pulmonale HämodynamikBei den in dieser Übersicht enthaltenen Studien wurde in einer prospektiven, monozentrischen, offenen Studie die Wirkung von inhaliertem Iloprost auf die pulmonale Hämodynamik bei Patienten mit COPD-assoziierter pulmonaler Hypertonie untersucht (
29
). Bei 67 COPD-Patienten mit pulmonaler Hypertonie wurde berichtet, dass eine kurze Inhalation von Iloprost über 10 Minuten den mittleren pulmonalarteriellen Druck, den pulmonalarteriellen Gefäßwiderstand und den pulmonalarteriellen Verschlussdruck im Vergleich zum Ausgangswert signifikant senken kann. Infolgedessen wurden das Herzzeitvolumen und der Kontraktilitätsindex als Reaktion auf inhaliertes Iloprost signifikant erhöht (
29
). Diese Ergebnisse weisen darauf hin, dass inhaliertes Prostacyclin das Potenzial hat, die hämodynamischen Indizes zu verbessern und dadurch die Funktion des rechten Ventrikels zu verbessern. Es sind jedoch weitere Studien erforderlich, um die langfristige Wirkung von inhaliertem Prostacyclin auf die hämodynamischen Parameter bei COPD-assoziierter pulmonaler Hypertonie zu beurteilen.4. DiskussionNach bestem Wissen und Gewissen handelt es sich hierbei um die erste systematische Übersichtsarbeit von Studien, die die Auswirkungen der Anwendung inhalativer Prostaglandin-I2- Analoga auf die klinischen Ergebnisse bei Patienten mit pulmonaler Hypertonie aufgrund von COPD untersuchen. Unsere wichtigsten Erkenntnisse zeigten, dass inhalatives Prostacyclin zwar den Sauerstoffsättigungsstatus und die COPD-bezogenen Ergebnisse (z. B. die Lungenfunktion) nicht zu verbessern scheint, jedoch das Potenzial hat, den mittleren pulmonalarteriellen Druck und den pulmonalarteriellen Gefäßwiderstand zu senken und dadurch die Funktion des rechten Ventrikels bei Patienten mit pulmonaler Hypertonie aufgrund von COPD zu verbessern. Angesichts der Tatsache, dass inhalative Prostaglandin-I2- Analoga vor Kurzem für die Behandlung von ILD-bedingter pulmonaler Hypertonie zugelassen wurden und die derzeit verfügbaren Erkenntnisse auf einen potenziellen Nutzen der gezielten Behandlung der Prostacyclin-Stoffwechselwege über die Inhalationsmethode hinweisen, sind weitere strenge randomisierte klinische Studien und Beobachtungsstudien mit größeren Stichproben erforderlich.Es wurde berichtet, dass die Expression der Prostaglandin-I-Synthese (das Enzym, das für die Produktion von Prostacyclin verantwortlich ist) in den Lungenarterien von Patienten mit pulmonaler Hypertonie und von Patienten mit durch Zigarettenrauchen bedingten Lungenerkrankungen reduziert ist. Diese Beobachtungen liefern eine starke Begründung für den Einsatz von Prostacyclin-Analoga und Prostacyclin-Rezeptoragonisten bei der Behandlung dieser Patienten. Sowohl orales als auch inhaliertes Prostacyclin wird seit langem zur Behandlung von pulmonaler Hypertonie der Gruppe 1 eingesetzt. Trotz der hohen Prävalenz der COPD-bedingten pulmonalen Hypertonie gibt es aufgrund fehlender Beweise derzeit keine zugelassenen Therapien für diese Patienten. Damit haben Kliniker keine andere Wahl, als Medikamente zu verwenden, die für andere Formen der pulmonalen Hypertonie, insbesondere Gruppe 1, zugelassen sind. Es wurde gezeigt, dass inhaliertes Prostacyclin, insbesondere Treprostinil über 12 Wochen, die körperliche Belastbarkeit von Patienten mit pulmonaler Hypertonie der Gruppe 1 verbessert (
33
). Kürzlich zeigte eine multizentrische, randomisierte, doppelblinde, placebokontrollierte 16-wöchige Studie an 326 Patienten mit pulmonaler Hypertonie aufgrund von ILD eine Verbesserung der körperlichen Belastbarkeit (gemessen mittels 6MWT) bei der Anwendung von inhaliertem Prostacyclin (
34
). Aufgrund dieser Erkenntnisse erhielt inhaliertes Prostacyclin vor kurzem von der US-amerikanischen Food and Drug Administration die Zulassung als erstes Medikament zur Behandlung von pulmonaler Hypertonie der Gruppe 3 (pulmonale Hypertonie aufgrund von ILD). Da ILD und COPD ähnliche klinische Erscheinungsbilder aufweisen und von der WHO in einer Gruppe eingeteilt werden (
1
), sind weitere Studien nötig, um herauszufinden, ob bei COPD-Patienten ähnliche Wirkungen von inhaliertem Prostacyclin beobachtet werden können.Interessanterweise unterstützen die Ergebnisse zweier in dieser systematischen Übersichtsarbeit enthaltener Studien nicht die Verwendung von inhaliertem Prostazyklin zur Verbesserung der körperlichen Leistungsfähigkeit bei COPD-Patienten mit pulmonaler Hypertonie im Vergleich zu 6MGT-Basisstudien (
27
) oder Placebogruppen (
28
). Trotz der kleinen Stichprobengröße in beiden Studien (
27
,
28
) (9 bzw. 16 Studienpopulationen) und der Tatsache, dass eine Studie wegen geringerer Teilnehmerzahl als erwartet abgebrochen wurde (
27
), ist das Ausbleiben einer Verbesserung der körperlichen Leistungsfähigkeit wahrscheinlich darauf zurückzuführen, dass der 6MGT zu Studienbeginn in der Population beider Studien, deren COPD als mittelschwer (GOLD 2) eingestuft wurde, stabil war (
27
,
28
). Eine weitere Steigerung des stabilen 6MGT ist daher weniger wahrscheinlich. Es ist interessant festzustellen, dass bei der Beurteilung der Wirkung von inhaliertem Prostacyclin auf die körperliche Leistungsfähigkeit bei Patienten mit schwerer pulmonaler Hypertonie infolge von COPD eine Verbesserung des 6MGT berichtet wurde (
30
), was darauf hindeutet, dass inhaliertes Prostacyclin die körperliche Leistungsfähigkeit bei Patienten mit pulmonaler Hypertonie infolge schwerer (aber nicht mittelschwerer) COPD verbessern kann. Diese plausible Spekulation wird durch die Beobachtung gestützt, die eine Verbesserung des 6MGT als Reaktion auf inhaliertes Prostacyclin in der Untergruppe der COPD-Patienten mit schwerer Dyspnoe und schwerer Verringerung der Lungenfunktion berichtet (
28
). Zur Unterstützung dieser Annahme wurde die PERFECT-Studie, die 2018 mit dem Ziel begonnen wurde, vor allem zu bewerten, ob inhaliertes Prostacyclin die körperliche Leistungsfähigkeit von Patienten mit pulmonaler Hypertonie infolge von COPD verbessern kann, nach einer routinemäßigen Sicherheits- und Wirksamkeitsanalyse durch das Datensicherheitsüberwachungskomitee vor Kurzem abgebrochen (
35
). Obwohl die Ergebnisse der PERFECT-Studie noch nicht veröffentlicht sind und die bislang verfügbaren Belege gegen die Verwendung von inhaliertem Prostacyclin zur Verbesserung der körperlichen Leistungsfähigkeit sprechen, besteht weiterhin ein ungedeckter Bedarf an einer entsprechend leistungsstarken multizentrischen, randomisierten, doppelblinden, placebokontrollierten Crossover-Studie zum Einfluss von inhaliertem Prostacyclin auf die körperliche Leistungsfähigkeit und andere klinische Ergebnisse bei der Stratifizierung der Schweregrade von COPD und pulmonaler Hypertonie. Zusammen mit der derzeit laufenden klinischen Studie zur Bewertung der Wirkung des inhalierten löslichen Guanylatcyclase-Stimulators auf die körperliche Leistungsfähigkeit (
36
) können diese Studien klare Belege für den Einsatz selektiver inhalativer pulmonaler Vasodilatatoren bei COPD-bedingter pulmonaler Hypertonie liefern.Die Lungenfunktion, insbesondere die Spirometrieparameter (z. B. FEV1 und FVC) sind hilfreiche Tests zur Diagnose, Nachsorge und Behandlung von Patienten mit COPD. Neben seiner Bedeutung bei der Diagnose von COPD ist DLCO ein bekannter Prädiktor für das Überleben von Patienten mit pulmonaler Hypertonie (
37
). Die Tatsache, dass die Ergebnisse der in diese Übersicht einbezogenen Studien keine Verbesserung der Lungenfunktion (
27
,
30
) oder der Schwere der Dyspnoe (
27
,
28
) zeigten, deutet darauf hin, dass inhaliertes Prostacyclin die COPD-bezogenen Ergebnisse bei COPD-Patienten mit pulmonaler Hypertonie wahrscheinlich nicht verbessern wird. Im Gegensatz zu den Ergebnissen dieser systematischen Übersicht zeigte eine Post-hoc-Analyse der INCREASE-Studie eine Verbesserung der FVC im Vergleich zu Placebo nach 16 Wochen bei Patienten mit pulmonaler Hypertonie aufgrund von ILD (
38
). Die Unterschiede zwischen COPD und ILD hinsichtlich klinischem Phänotyp, Behandlungserfolg und -erfolg sowie die Tatsache, dass Treprostinil antifibrotisch wirkt (wahrscheinlich durch Aktivierung des Prostaglandin-E-Rezeptors 2) (
39
), könnten erklären, warum die Verbesserung der FVC nur bei Patienten mit pulmonaler Hypertonie aufgrund von ILD, nicht aber bei COPD beobachtet wurde. Unterstützt wird diese Annahme durch die Beobachtung der INCREASE-Studie, die die größte Verbesserung der FVC bei Patienten mit idiopathischer Lungenfibrose (IPF) (
38
) zeigte und die den Weg für die laufende TETON-Studie ebnete, in der die Wirkung von inhaliertem Treprostinil auf die FVC bei IPF-Patienten ohne pulmonale Hypertonie untersucht wurde (
39
).Pulmonale Hypertonie ist definiert als erhöhter mittlerer pulmonalarterieller Druck und pulmonaler Gefäßwiderstand. Zur Überwachung der Wirksamkeit von Medikamenten gegen pulmonale Hypertonie ist eine routinemäßige Beurteilung dieser hämodynamischen Parameter erforderlich. Da jedoch die nicht-invasive Messung der pulmonalen Hämodynamik bei COPD-Patienten aufgrund der Lungenüberblähung ungenau ist (
8
,
40
,
41
) und die Beurteilung mittels Rechtsherzkatheter als invasives und zeitaufwändiges Verfahren gilt, hat sich bisher nur eine Studie mit der Wirkung von inhaliertem Prostacyclin (Iloprost) auf hämodynamische Werte bei COPD-Patienten mit pulmonaler Hypertonie befasst (
29
). Die erhebliche Verbesserung des mittleren pulmonalarteriellen Drucks, des pulmonalarteriellen Widerstands und der Herzleistung als Reaktion auf die Inhalation von Prostacyclin (
29
) unterstützt den Einsatz von inhalierten Prostacyclin-Analoga bei der Behandlung von Patienten mit COPD-bedingter pulmonaler Hypertonie. Es ist jedoch zu beachten, dass das Kurzzeitdesign dieser Studie die Ergebnisse auf eine kurzfristige Anwendung beschränkt. Dies weist darauf hin, dass dringend klinische Studien erforderlich sind, um die langfristige Wirkung von inhaliertem Prostacyclin bei COPD-assoziierter pulmonaler Hypertonie zu beurteilen. Die Ergebnisse einer von Wang et al. durchgeführten Studie werden durch andere Studien gestützt, die eine Verbesserung der hämodynamischen Parameter bei COPD-Patienten mit pulmonaler Hypertonie nach der Anwendung von Sildenafil (erhöht Stickoxid durch die Hemmung der Phosphodiesterase Typ 5) (
42
) und inhaliertem Stickoxid (
43
) zeigten. Zusammengefasst weisen diese Ergebnisse darauf hin, dass selektive pulmonale Vasodilatatoren, die zur Behandlung der pulmonalen Hypertonie der Gruppe 1 zugelassen sind, zur Verbesserung der hämodynamischen Parameter bei COPD-Patienten mit pulmonaler Hypertonie eingesetzt werden können.Trotz der Verbesserung der hämodynamischen Parameter war die systemische Gabe von pulmonalen Vasodilatatoren mit einer schädlichen Wirkung auf den Gasaustausch verbunden. Bei Patienten mit COPD geht man davon aus, dass systemisch verabreichte pulmonale Vasodilatatoren (z. B. Sildenafil) die Gefäße sowohl um beatmete als auch um nicht beatmete Patienten erweitern können, was zu einer Hemmung der hypoxischen pulmonalen Vasokonstriktion und einer Beeinträchtigung des Gasaustausches führt (
42
,
44
). Wenn pulmonale Vasodilatatoren, darunter Prostacyclin, bei Patienten mit pulmonaler Hypertonie der Gruppe 3 durch Inhalation verabreicht werden, kann das Risiko von Ventilations- und Perfusionsdefiziten, die mit der Gabe systemischer Vasodilatatoren einhergehen, minimiert werden (
45
), wenn man bedenkt, dass bei diesen Patienten die inhalierten pulmonalen Vasodilatatoren gezielt auf die besser belüfteten Alveolen wirken können. Dieser Bericht enthält die Ergebnisse zweier Studien, die zeigen, dass inhaliertes Prostazyklin den Gasaustauschindex (z. B. AA-Gradienten) im Vergleich mit den Ausgangswerten nicht beeinflusst (
27
,
29
). Dies legt nahe, dass die Anwendung eines selektiven pulmonalen Vasodilatators (inhaliert) bei COPD-Patienten mit pulmonaler Hypertonie weniger wahrscheinlich zu Ventilations- und Perfusionsdefiziten führt. Diese Annahme wird zusätzlich durch die Beobachtung untermauert, dass sich bei Patienten mit COPD-bedingter pulmonaler Hypertonie 30 Minuten nach der Anwendung von inhaliertem Prostazyklin mehrere Gasaustauschparameter verbesserten (
30
). Interessant ist, dass diese Parameter 2 Stunden nach der Inhalation eines stabilen Prostazyklin-Analogons wieder auf den Ausgangswert zurückkehrten. Dies ist wahrscheinlich auf die kurzfristigen Effekte des Prostazyklins zurückzuführen, das innerhalb von 30 bis 60 Minuten abflacht (
46
), was eine wiederholte Verabreichung erforderlich macht. Trotz dieser Einschränkung belegen die aktuellen Erkenntnisse die Überlegenheit von inhalierten Vasodilatatoren (z. B. inhaliertes Prostacyclin) gegenüber oralen Vasodilatatoren (z. B. Sildenafil) bei der Behandlung von Patienten mit COPD-bedingter pulmonaler Hypertonie, da inhalierte Vasodilatatoren das Blut in besser belüftete Alveolen umleiten und dadurch die ungleiche Verteilung von Ventilation und Perfusion minimieren können.4.1. Stärke und BegrenzungNach bestem Wissen und Gewissen ist dies die erste systematische Übersicht, die die aktuellen Erkenntnisse zur Beurteilung der Auswirkungen der Verwendung inhalativer Prostaglandin-I2- Analoga auf die pulmonale Hämodynamik, die körperliche Leistungsfähigkeit, die Lungenfunktion und den Sauerstoffsättigungsstatus bei Patienten mit pulmonaler Hypertonie aufgrund von COPD zusammenfasst. Wir haben sowohl randomisierte Studien als auch Beobachtungsstudien einbezogen. Unsere Studie hatte jedoch einige Einschränkungen. Die in diese Übersicht einbezogenen Studien hatten eine kurze Nachbeobachtungszeit. Darüber hinaus sollten unsere Ergebnisse aufgrund der geringen Stichprobengröße der in diese Übersicht einbezogenen Studien mit Vorsicht interpretiert werden.5. FazitDie Ergebnisse der systematischen Überprüfung deuten darauf hin, dass die Verwendung von inhaliertem Prostacyclin das Potenzial hat, hämodynamische Parameter bei Patienten mit COPD-bedingter pulmonaler Hypertonie zu verbessern, ohne den Gasaustausch zu beeinträchtigen. Für andere klinische Ergebnisse (z. B. Lungenfunktion und körperliche Leistungsfähigkeit) konnten jedoch keine schlüssigen Vorteile nachgewiesen werden. Es besteht ein beispielloser ungedeckter Bedarf an einer großen randomisierten kontrollierten Studie, um den potenziellen Nutzen eines inhalierten Prostacyclin-Analogons zur Behandlung von pulmonaler Hypertonie aufgrund von COPD weiter zu untersuchen.DatenverfügbarkeitserklärungDie in der Studie vorgestellten Originalbeiträge sind im Artikel/Zusatzmaterial enthalten, weitere Anfragen können an den entsprechenden Autor gerichtet werden.AutorenbeiträgeAAlq, HB und AAld haben zur Konzeption und Gestaltung der Rezension beigetragen. AAlq, HB, AAld, HA, RS und MM haben zur Datenextraktion beigetragen. AAlq, AAld, JA, AAlG, AN, SA und HA interpretieren Daten und haben Abschnitte des Manuskripts verfasst. Alle Autoren haben zum Artikel beigetragen und die eingereichte Version genehmigt.
Abbildung 1. Flussdiagramm zur Veranschaulichung der systematischen Such- und Screeningstrategie auf Grundlage der Leitlinien für bevorzugte Berichtselemente für systematische Überprüfungen und Metaanalysen, einschließlich der Anzahl der Studien, die die Eignungskriterien erfüllen, und der Anzahl der ausgeschlossenen Studien. COPD: chronisch obstruktive Lungenerkrankung. 3.1. Die Beschreibung der eingeschlossenen StudienDie vier eingeschlossenen Studien umfassten eine prospektive, multizentrische, offene Pilotstudie mit einer Stichprobengröße von neun COPD-Patienten, die in den USA durchgeführt und 2017 veröffentlicht wurde (
27
), eine prospektive, randomisierte, doppelblinde, monozentrische Crossover-Studie mit einer Stichprobengröße von 16 COPD-Patienten, die in der Schweiz durchgeführt und 2012 veröffentlicht wurde (
28
), eine prospektive, monozentrische, offene Studie mit einer Stichprobengröße von 67 COPD-Patienten, die in China durchgeführt und 2017 veröffentlicht wurde (
29
), und eine prospektive Beobachtungsstudie mit einer Stichprobengröße von 10 COPD-Patienten, die in den USA durchgeführt und 2010 veröffentlicht wurde (
30
). Eine vollständige Beschreibung der eingeschlossenen Studien finden Sie in
Tabelle 1
.3.2. GasaustauschDie Verwendung des inhalativen Prostazyklin-Analogons Treprostinil oder Iloprost hatte im Vergleich mit Ausgangswerten in zwei Studien (27, 29) keinen signifikanten Einfluss auf die Gasaustauschparameter (gemessen anhand des Sauerstoffpartialdrucks im arteriellen Blut (PaO2 ) , des Kohlendioxidpartialdrucks im arteriellen Blut (PaCO2 ) , der arteriellen Sauerstoffsättigung (SaO2 ) , der pulmonalen Shuntfraktion (Qs/Qt) und des alveolar-arteriellen Sauerstoffkonzentrationsgradienten (Aa-Gradient). Im Gegensatz dazu wurde in
einer
Studie
festgestellt
, dass die Verwendung des inhalativen Prostazyklin-Analogons (Iloprost) alle Gasaustauschparameter (gemessen anhand des Aa-Gradienten, des Verhältnisses Minutenventilation (VE)/Kohlendioxidproduktion (VE/VCO2 ) und des Verhältnisses VE/Sauerstoffverbrauch (VE/VO2 ) ) im Vergleich mit Ausgangswerten nach 30-minütiger Inhalation der ersten und zweiten Dosis Iloprost signifikant verbesserte (
30
). Als diese Parameter jedoch 2 Stunden nach der Anwendung von Iloprost erneut gemessen wurden, waren alle Gasaustauschparameter wieder auf den Ausgangswert zurückgekehrt. Zusammengenommen lassen diese Beobachtungen darauf schließen, dass es unwahrscheinlich ist, dass die Inhalation eines Prostacyclin-Analogons (Treprostinil oder Iloprost) die Gasaustauschparameter bei Patienten mit pulmonaler Hypertonie aufgrund von COPD verbessern oder verschlechtern kann.3.3. TrainingskapazitätDie körperliche Belastbarkeit wurde in drei Studien (
27
,
28
,
30
) berichtet, in denen die Wirksamkeit von inhaliertem Prostazyklin im 6MGT bei COPD-Patienten mit pulmonaler Hypertonie beurteilt wurde. Zwei Studien berichteten von keinem signifikanten Effekt von inhaliertem Prostazyklin im Vergleich zum 6MGT-Ausgangswert (
27
) oder zur Placebogruppe (
28
). Nur eine Studie berichtete von einer signifikanten Verbesserung des 6MGT im Vergleich zum Ausgangswert bei COPD-Patienten mit pulmonaler Hypertonie (
30
). Laut einer prospektiven, multizentrischen, offenen Pilotstudie von Bajwa et al. (
27
) verbesserte inhaliertes Treprostinil die 6MGT-Distanz bei einer Beurteilung in Woche 16 bei neun COPD-Patienten mit mittelschwerer Erkrankung und pulmonaler Hypertonie nicht signifikant (
27
). Im Gegensatz dazu zeigte eine Kohortenstudie von Dernaika et al. (27) eine signifikante Verbesserung der 6MGT-Distanz bei (
30
) verbesserte eine Einzeldosis (Mittelwert ± SD zu Studienbeginn: 269 ± 112 m vs. Mittelwert nach Iloprost ± SD: 324 ± 135 m; p < 0,05) und eine zweite Dosis (Mittelwert ± SD zu Studienbeginn: 269 ± 112 m vs. Mittelwert nach Iloprost ± SD: 330 ± 136 m; p < 0,05) von inhaliertem Iloprost die 6MWT-Distanz im Vergleich zum Ausgangswert signifikant, wenn sie 30 Minuten nach der Behandlung bei zehn Patienten mit schwerer COPD und pulmonaler Hypertonie beurteilt wurde (
30
).3.4. LungenfunktionIn zwei Studien wurden Spirometrieparameter und Diffusionskapazitätstests als sekundäre Ergebnisse verwendet, um die Wirksamkeit von inhaliertem Prostacyclin zu beurteilen (
27
,
30
). Die Anwendung des inhalierten Prostacyclin-Analogons Treprostinil verringerte FEV1 und die forcierte Vitalkapazität (FVC), hatte jedoch keinen Einfluss auf die Diffusionskapazität der Lunge für Kohlenmonoxid (DLCO) in einer prospektiven, multizentrischen, offenen Pilotstudie mit einer Stichprobengröße von neun COPD-Patienten mit pulmonaler Hypertonie (
27
). Im Gegensatz zu diesen Befunden wurden Verbesserungen bei FEV1 und FVC (aber nicht bei DLCO) 30 Minuten nach Anwendung der ersten und zweiten Dosis von inhaliertem Iloprost im Vergleich zu den Ausgangsmessungen berichtet (
30
). Messungen der gleichen Parameter wurden 2 Stunden nach Anwendung von Iloprost vorgenommen. Interessanterweise waren weder die Spirometrieparameter noch die DLCO im Vergleich zum Ausgangswert beeinträchtigt (
30
). Diese Beobachtungen legen nahe, dass inhaliertes Prostacyclin die Lungenfunktion bei Patienten mit pulmonaler Hypertonie aufgrund von COPD wahrscheinlich nicht verbessert.3.5. Schweregrad der DyspnoeDer Schweregrad der Dyspnoe wurde in zwei Studien (
27
,
28
) mithilfe der modifizierten Borg-Skala gemessen, um die Wirksamkeit von inhaliertem Prostacyclin bei COPD-Patienten mit pulmonaler Hypertonie einzuschätzen. Zwei Studien berichteten von keinem signifikanten Effekt von inhaliertem Prostacyclin im Vergleich zur Ausgangsgruppe (
27
) oder zur Placebogruppe (
28
). Laut einer prospektiven, multizentrischen, offenen Pilotstudie von Bajwa et al. (
27
) verbesserte inhaliertes Treprostinil den Schweregrad der Dyspnoe bei einer Beurteilung in Woche 16 bei neun COPD-Patienten mit mittelschwerem Schweregrad und pulmonaler Hypertonie nicht signifikant (
27
). Darüber hinaus zeigten Boeck et al. in einer prospektiven, randomisierten, doppelblinden, monozentrischen Crossover-Studie keine signifikanten Verbesserungen. (
28
) verbesserte inhaliertes Iloprost den Schweregrad der Dyspnoe im Vergleich zur Placebogruppe bei 16 COPD-Patienten mit mittelschwerer Erkrankung und pulmonaler Hypertonie nicht signifikant (
28
).3.6. Die pulmonale HämodynamikBei den in dieser Übersicht enthaltenen Studien wurde in einer prospektiven, monozentrischen, offenen Studie die Wirkung von inhaliertem Iloprost auf die pulmonale Hämodynamik bei Patienten mit COPD-assoziierter pulmonaler Hypertonie untersucht (
29
). Bei 67 COPD-Patienten mit pulmonaler Hypertonie wurde berichtet, dass eine kurze Inhalation von Iloprost über 10 Minuten den mittleren pulmonalarteriellen Druck, den pulmonalarteriellen Gefäßwiderstand und den pulmonalarteriellen Verschlussdruck im Vergleich zum Ausgangswert signifikant senken kann. Infolgedessen wurden das Herzzeitvolumen und der Kontraktilitätsindex als Reaktion auf inhaliertes Iloprost signifikant erhöht (
29
). Diese Ergebnisse weisen darauf hin, dass inhaliertes Prostacyclin das Potenzial hat, die hämodynamischen Indizes zu verbessern und dadurch die Funktion des rechten Ventrikels zu verbessern. Es sind jedoch weitere Studien erforderlich, um die langfristige Wirkung von inhaliertem Prostacyclin auf die hämodynamischen Parameter bei COPD-assoziierter pulmonaler Hypertonie zu beurteilen.4. DiskussionNach bestem Wissen und Gewissen handelt es sich hierbei um die erste systematische Übersichtsarbeit von Studien, die die Auswirkungen der Anwendung inhalativer Prostaglandin-I2- Analoga auf die klinischen Ergebnisse bei Patienten mit pulmonaler Hypertonie aufgrund von COPD untersuchen. Unsere wichtigsten Erkenntnisse zeigten, dass inhalatives Prostacyclin zwar den Sauerstoffsättigungsstatus und die COPD-bezogenen Ergebnisse (z. B. die Lungenfunktion) nicht zu verbessern scheint, jedoch das Potenzial hat, den mittleren pulmonalarteriellen Druck und den pulmonalarteriellen Gefäßwiderstand zu senken und dadurch die Funktion des rechten Ventrikels bei Patienten mit pulmonaler Hypertonie aufgrund von COPD zu verbessern. Angesichts der Tatsache, dass inhalative Prostaglandin-I2- Analoga vor Kurzem für die Behandlung von ILD-bedingter pulmonaler Hypertonie zugelassen wurden und die derzeit verfügbaren Erkenntnisse auf einen potenziellen Nutzen der gezielten Behandlung der Prostacyclin-Stoffwechselwege über die Inhalationsmethode hinweisen, sind weitere strenge randomisierte klinische Studien und Beobachtungsstudien mit größeren Stichproben erforderlich.Es wurde berichtet, dass die Expression der Prostaglandin-I-Synthese (das Enzym, das für die Produktion von Prostacyclin verantwortlich ist) in den Lungenarterien von Patienten mit pulmonaler Hypertonie und von Patienten mit durch Zigarettenrauchen bedingten Lungenerkrankungen reduziert ist. Diese Beobachtungen liefern eine starke Begründung für den Einsatz von Prostacyclin-Analoga und Prostacyclin-Rezeptoragonisten bei der Behandlung dieser Patienten. Sowohl orales als auch inhaliertes Prostacyclin wird seit langem zur Behandlung von pulmonaler Hypertonie der Gruppe 1 eingesetzt. Trotz der hohen Prävalenz der COPD-bedingten pulmonalen Hypertonie gibt es aufgrund fehlender Beweise derzeit keine zugelassenen Therapien für diese Patienten. Damit haben Kliniker keine andere Wahl, als Medikamente zu verwenden, die für andere Formen der pulmonalen Hypertonie, insbesondere Gruppe 1, zugelassen sind. Es wurde gezeigt, dass inhaliertes Prostacyclin, insbesondere Treprostinil über 12 Wochen, die körperliche Belastbarkeit von Patienten mit pulmonaler Hypertonie der Gruppe 1 verbessert (
33
). Kürzlich zeigte eine multizentrische, randomisierte, doppelblinde, placebokontrollierte 16-wöchige Studie an 326 Patienten mit pulmonaler Hypertonie aufgrund von ILD eine Verbesserung der körperlichen Belastbarkeit (gemessen mittels 6MWT) bei der Anwendung von inhaliertem Prostacyclin (
34
). Aufgrund dieser Erkenntnisse erhielt inhaliertes Prostacyclin vor kurzem von der US-amerikanischen Food and Drug Administration die Zulassung als erstes Medikament zur Behandlung von pulmonaler Hypertonie der Gruppe 3 (pulmonale Hypertonie aufgrund von ILD). Da ILD und COPD ähnliche klinische Erscheinungsbilder aufweisen und von der WHO in einer Gruppe eingeteilt werden (
1
), sind weitere Studien nötig, um herauszufinden, ob bei COPD-Patienten ähnliche Wirkungen von inhaliertem Prostacyclin beobachtet werden können.Interessanterweise unterstützen die Ergebnisse zweier in dieser systematischen Übersichtsarbeit enthaltener Studien nicht die Verwendung von inhaliertem Prostazyklin zur Verbesserung der körperlichen Leistungsfähigkeit bei COPD-Patienten mit pulmonaler Hypertonie im Vergleich zu 6MGT-Basisstudien (
27
) oder Placebogruppen (
28
). Trotz der kleinen Stichprobengröße in beiden Studien (
27
,
28
) (9 bzw. 16 Studienpopulationen) und der Tatsache, dass eine Studie wegen geringerer Teilnehmerzahl als erwartet abgebrochen wurde (
27
), ist das Ausbleiben einer Verbesserung der körperlichen Leistungsfähigkeit wahrscheinlich darauf zurückzuführen, dass der 6MGT zu Studienbeginn in der Population beider Studien, deren COPD als mittelschwer (GOLD 2) eingestuft wurde, stabil war (
27
,
28
). Eine weitere Steigerung des stabilen 6MGT ist daher weniger wahrscheinlich. Es ist interessant festzustellen, dass bei der Beurteilung der Wirkung von inhaliertem Prostacyclin auf die körperliche Leistungsfähigkeit bei Patienten mit schwerer pulmonaler Hypertonie infolge von COPD eine Verbesserung des 6MGT berichtet wurde (
30
), was darauf hindeutet, dass inhaliertes Prostacyclin die körperliche Leistungsfähigkeit bei Patienten mit pulmonaler Hypertonie infolge schwerer (aber nicht mittelschwerer) COPD verbessern kann. Diese plausible Spekulation wird durch die Beobachtung gestützt, die eine Verbesserung des 6MGT als Reaktion auf inhaliertes Prostacyclin in der Untergruppe der COPD-Patienten mit schwerer Dyspnoe und schwerer Verringerung der Lungenfunktion berichtet (
28
). Zur Unterstützung dieser Annahme wurde die PERFECT-Studie, die 2018 mit dem Ziel begonnen wurde, vor allem zu bewerten, ob inhaliertes Prostacyclin die körperliche Leistungsfähigkeit von Patienten mit pulmonaler Hypertonie infolge von COPD verbessern kann, nach einer routinemäßigen Sicherheits- und Wirksamkeitsanalyse durch das Datensicherheitsüberwachungskomitee vor Kurzem abgebrochen (
35
). Obwohl die Ergebnisse der PERFECT-Studie noch nicht veröffentlicht sind und die bislang verfügbaren Belege gegen die Verwendung von inhaliertem Prostacyclin zur Verbesserung der körperlichen Leistungsfähigkeit sprechen, besteht weiterhin ein ungedeckter Bedarf an einer entsprechend leistungsstarken multizentrischen, randomisierten, doppelblinden, placebokontrollierten Crossover-Studie zum Einfluss von inhaliertem Prostacyclin auf die körperliche Leistungsfähigkeit und andere klinische Ergebnisse bei der Stratifizierung der Schweregrade von COPD und pulmonaler Hypertonie. Zusammen mit der derzeit laufenden klinischen Studie zur Bewertung der Wirkung des inhalierten löslichen Guanylatcyclase-Stimulators auf die körperliche Leistungsfähigkeit (
36
) können diese Studien klare Belege für den Einsatz selektiver inhalativer pulmonaler Vasodilatatoren bei COPD-bedingter pulmonaler Hypertonie liefern.Die Lungenfunktion, insbesondere die Spirometrieparameter (z. B. FEV1 und FVC) sind hilfreiche Tests zur Diagnose, Nachsorge und Behandlung von Patienten mit COPD. Neben seiner Bedeutung bei der Diagnose von COPD ist DLCO ein bekannter Prädiktor für das Überleben von Patienten mit pulmonaler Hypertonie (
37
). Die Tatsache, dass die Ergebnisse der in diese Übersicht einbezogenen Studien keine Verbesserung der Lungenfunktion (
27
,
30
) oder der Schwere der Dyspnoe (
27
,
28
) zeigten, deutet darauf hin, dass inhaliertes Prostacyclin die COPD-bezogenen Ergebnisse bei COPD-Patienten mit pulmonaler Hypertonie wahrscheinlich nicht verbessern wird. Im Gegensatz zu den Ergebnissen dieser systematischen Übersicht zeigte eine Post-hoc-Analyse der INCREASE-Studie eine Verbesserung der FVC im Vergleich zu Placebo nach 16 Wochen bei Patienten mit pulmonaler Hypertonie aufgrund von ILD (
38
). Die Unterschiede zwischen COPD und ILD hinsichtlich klinischem Phänotyp, Behandlungserfolg und -erfolg sowie die Tatsache, dass Treprostinil antifibrotisch wirkt (wahrscheinlich durch Aktivierung des Prostaglandin-E-Rezeptors 2) (
39
), könnten erklären, warum die Verbesserung der FVC nur bei Patienten mit pulmonaler Hypertonie aufgrund von ILD, nicht aber bei COPD beobachtet wurde. Unterstützt wird diese Annahme durch die Beobachtung der INCREASE-Studie, die die größte Verbesserung der FVC bei Patienten mit idiopathischer Lungenfibrose (IPF) (
38
) zeigte und die den Weg für die laufende TETON-Studie ebnete, in der die Wirkung von inhaliertem Treprostinil auf die FVC bei IPF-Patienten ohne pulmonale Hypertonie untersucht wurde (
39
).Pulmonale Hypertonie ist definiert als erhöhter mittlerer pulmonalarterieller Druck und pulmonaler Gefäßwiderstand. Zur Überwachung der Wirksamkeit von Medikamenten gegen pulmonale Hypertonie ist eine routinemäßige Beurteilung dieser hämodynamischen Parameter erforderlich. Da jedoch die nicht-invasive Messung der pulmonalen Hämodynamik bei COPD-Patienten aufgrund der Lungenüberblähung ungenau ist (
8
,
40
,
41
) und die Beurteilung mittels Rechtsherzkatheter als invasives und zeitaufwändiges Verfahren gilt, hat sich bisher nur eine Studie mit der Wirkung von inhaliertem Prostacyclin (Iloprost) auf hämodynamische Werte bei COPD-Patienten mit pulmonaler Hypertonie befasst (
29
). Die erhebliche Verbesserung des mittleren pulmonalarteriellen Drucks, des pulmonalarteriellen Widerstands und der Herzleistung als Reaktion auf die Inhalation von Prostacyclin (
29
) unterstützt den Einsatz von inhalierten Prostacyclin-Analoga bei der Behandlung von Patienten mit COPD-bedingter pulmonaler Hypertonie. Es ist jedoch zu beachten, dass das Kurzzeitdesign dieser Studie die Ergebnisse auf eine kurzfristige Anwendung beschränkt. Dies weist darauf hin, dass dringend klinische Studien erforderlich sind, um die langfristige Wirkung von inhaliertem Prostacyclin bei COPD-assoziierter pulmonaler Hypertonie zu beurteilen. Die Ergebnisse einer von Wang et al. durchgeführten Studie werden durch andere Studien gestützt, die eine Verbesserung der hämodynamischen Parameter bei COPD-Patienten mit pulmonaler Hypertonie nach der Anwendung von Sildenafil (erhöht Stickoxid durch die Hemmung der Phosphodiesterase Typ 5) (
42
) und inhaliertem Stickoxid (
43
) zeigten. Zusammengefasst weisen diese Ergebnisse darauf hin, dass selektive pulmonale Vasodilatatoren, die zur Behandlung der pulmonalen Hypertonie der Gruppe 1 zugelassen sind, zur Verbesserung der hämodynamischen Parameter bei COPD-Patienten mit pulmonaler Hypertonie eingesetzt werden können.Trotz der Verbesserung der hämodynamischen Parameter war die systemische Gabe von pulmonalen Vasodilatatoren mit einer schädlichen Wirkung auf den Gasaustausch verbunden. Bei Patienten mit COPD geht man davon aus, dass systemisch verabreichte pulmonale Vasodilatatoren (z. B. Sildenafil) die Gefäße sowohl um beatmete als auch um nicht beatmete Patienten erweitern können, was zu einer Hemmung der hypoxischen pulmonalen Vasokonstriktion und einer Beeinträchtigung des Gasaustausches führt (
42
,
44
). Wenn pulmonale Vasodilatatoren, darunter Prostacyclin, bei Patienten mit pulmonaler Hypertonie der Gruppe 3 durch Inhalation verabreicht werden, kann das Risiko von Ventilations- und Perfusionsdefiziten, die mit der Gabe systemischer Vasodilatatoren einhergehen, minimiert werden (
45
), wenn man bedenkt, dass bei diesen Patienten die inhalierten pulmonalen Vasodilatatoren gezielt auf die besser belüfteten Alveolen wirken können. Dieser Bericht enthält die Ergebnisse zweier Studien, die zeigen, dass inhaliertes Prostazyklin den Gasaustauschindex (z. B. AA-Gradienten) im Vergleich mit den Ausgangswerten nicht beeinflusst (
27
,
29
). Dies legt nahe, dass die Anwendung eines selektiven pulmonalen Vasodilatators (inhaliert) bei COPD-Patienten mit pulmonaler Hypertonie weniger wahrscheinlich zu Ventilations- und Perfusionsdefiziten führt. Diese Annahme wird zusätzlich durch die Beobachtung untermauert, dass sich bei Patienten mit COPD-bedingter pulmonaler Hypertonie 30 Minuten nach der Anwendung von inhaliertem Prostazyklin mehrere Gasaustauschparameter verbesserten (
30
). Interessant ist, dass diese Parameter 2 Stunden nach der Inhalation eines stabilen Prostazyklin-Analogons wieder auf den Ausgangswert zurückkehrten. Dies ist wahrscheinlich auf die kurzfristigen Effekte des Prostazyklins zurückzuführen, das innerhalb von 30 bis 60 Minuten abflacht (
46
), was eine wiederholte Verabreichung erforderlich macht. Trotz dieser Einschränkung belegen die aktuellen Erkenntnisse die Überlegenheit von inhalierten Vasodilatatoren (z. B. inhaliertes Prostacyclin) gegenüber oralen Vasodilatatoren (z. B. Sildenafil) bei der Behandlung von Patienten mit COPD-bedingter pulmonaler Hypertonie, da inhalierte Vasodilatatoren das Blut in besser belüftete Alveolen umleiten und dadurch die ungleiche Verteilung von Ventilation und Perfusion minimieren können.4.1. Stärke und BegrenzungNach bestem Wissen und Gewissen ist dies die erste systematische Übersicht, die die aktuellen Erkenntnisse zur Beurteilung der Auswirkungen der Verwendung inhalativer Prostaglandin-I2- Analoga auf die pulmonale Hämodynamik, die körperliche Leistungsfähigkeit, die Lungenfunktion und den Sauerstoffsättigungsstatus bei Patienten mit pulmonaler Hypertonie aufgrund von COPD zusammenfasst. Wir haben sowohl randomisierte Studien als auch Beobachtungsstudien einbezogen. Unsere Studie hatte jedoch einige Einschränkungen. Die in diese Übersicht einbezogenen Studien hatten eine kurze Nachbeobachtungszeit. Darüber hinaus sollten unsere Ergebnisse aufgrund der geringen Stichprobengröße der in diese Übersicht einbezogenen Studien mit Vorsicht interpretiert werden.5. FazitDie Ergebnisse der systematischen Überprüfung deuten darauf hin, dass die Verwendung von inhaliertem Prostacyclin das Potenzial hat, hämodynamische Parameter bei Patienten mit COPD-bedingter pulmonaler Hypertonie zu verbessern, ohne den Gasaustausch zu beeinträchtigen. Für andere klinische Ergebnisse (z. B. Lungenfunktion und körperliche Leistungsfähigkeit) konnten jedoch keine schlüssigen Vorteile nachgewiesen werden. Es besteht ein beispielloser ungedeckter Bedarf an einer großen randomisierten kontrollierten Studie, um den potenziellen Nutzen eines inhalierten Prostacyclin-Analogons zur Behandlung von pulmonaler Hypertonie aufgrund von COPD weiter zu untersuchen.DatenverfügbarkeitserklärungDie in der Studie vorgestellten Originalbeiträge sind im Artikel/Zusatzmaterial enthalten, weitere Anfragen können an den entsprechenden Autor gerichtet werden.AutorenbeiträgeAAlq, HB und AAld haben zur Konzeption und Gestaltung der Rezension beigetragen. AAlq, HB, AAld, HA, RS und MM haben zur Datenextraktion beigetragen. AAlq, AAld, JA, AAlG, AN, SA und HA interpretieren Daten und haben Abschnitte des Manuskripts verfasst. Alle Autoren haben zum Artikel beigetragen und die eingereichte Version genehmigt.







- 1 Abteilung für Atemtherapie, Fakultät für medizinische Rehabilitationswissenschaften, König-Abdulaziz-Universität, Dschidda, Saudi-Arabien
- 2 Atemtherapie-Einheit, King Abdulaziz University Hospital, Dschidda, Saudi-Arabien
- 3 Abteilung für Atemtherapie, Fakultät für angewandte Medizinwissenschaften, Jazan University, Jazan, Saudi-Arabien
- 4 Abteilung für Beatmungstherapie, König Saud bin Abdulaziz Universität für Gesundheitswissenschaften, Dschidda, Saudi-Arabien
- 5 King Abdullah International Medical Research Centre, Dschidda, Saudi-Arabien
- 6 Abteilung für Beatmungstherapie, Prince Sultan Military College of Health Sciences, Dammam, Saudi-Arabien
- 7 Abteilung für Beatmungstherapie, College of Applied Medical Sciences, King Faisal University, Al Ahsa, Saudi-Arabien
- 8 National Heart and Lung Institute, Imperial College London, London, Vereinigtes Königreich
- 9 Atemwegsmedizin, Royal Brompton Hospital, London, Vereinigtes Königreich
- 10 King Abdulaziz Hospital, Gesundheitsministerium der Nationalgarde, Al Ahsa, Saudi-Arabien
- 11 König Saud bin Abdulaziz Universität für Gesundheitswissenschaften, College of Applied Medical Sciences, Al Ahsa, Saudi-Arabien
- 12 Abteilung für angewandte Pharmaziewissenschaften und klinische Pharmazie, Fakultät für Pharmazie, Isra University, Amman, Jordanien
- 13 Abteilung für Beatmungspflege, Mediclinic Almurjan Hospital, Dschidda, Saudi-Arabien
- 14 Medizinische Fakultät, Umm Al-Qura Universität, Mekka, Saudi-Arabien


OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Bitte Anmelden oder Registrieren um der Konversation beizutreten.

