- Beiträge: 1755
Sidebar
- Forum
- PH-Forum
- Forschung und Wissen
- Die neue Rolle von Sacubitril/Valsartan bei pulmonaler Hypertonie mit Herzinsuff
Die neue Rolle von Sacubitril/Valsartan bei pulmonaler Hypertonie mit Herzinsuff
07 Jul 2024 13:46 #2146
von danny
OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Die neue Rolle von Sacubitril/Valsartan bei pulmonaler Hypertonie mit Herzinsuff wurde erstellt von danny
Die neue Rolle von Sacubitril/Valsartan bei pulmonaler Hypertonie mit HerzinsuffizienzPulmonale Hypertonie aufgrund einer Linksherzerkrankung (PH-LHD) macht etwa 65–80 % aller Patienten mit PH aus. Der Verlauf, die Prognose und die Mortalität von Personen mit Linksherzinsuffizienz (LHF) werden maßgeblich durch PH und Funktionsstörungen des rechten Ventrikels (RV) beeinflusst. Daher sollten Kardiologen dem Zusammenspiel zwischen HF und PH große Aufmerksamkeit widmen. Patienten mit PH und HF profitieren möglicherweise nicht optimal von den therapeutischen Wirkungen von Prostaglandinen, Endothelin-Rezeptor-Antagonisten oder Phosphodiesterasehemmern, die spezifische Medikamente gegen pulmonale arterielle Hypertonie (PAH) sind. Sacubitril/Valsartan, der Angiotensin-Rezeptor-II-Blocker-Neprilysin-Hemmer (ARNI), wurde in den Leitlinien der European Society of Cardiology von 2021 als Erstlinientherapie für Patienten mit Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) empfohlen. Obwohl ARNI bei der Behandlung einer Vergrößerung des linken Ventrikels (LV) und einer geringeren Auswurffraktion wirksam ist, ist seine Wirksamkeit bei der Behandlung von Personen mit PH und HF noch nicht ausreichend erforscht. Angesichts seiner gefäßerweiternden Wirkung auf präkapillärer Ebene und seiner natriuretischen Drainagefunktion auf postkapillärer Ebene wird angenommen, dass ARNI ein breites Spektrum potenzieller Anwendungen bei der Behandlung von PH-LHD hat. In dieser Übersicht werden die grundlegenden pathophysiologischen Zusammenhänge zwischen PH und HF erörtert, wobei die neuesten Forschungsergebnisse und potenziellen Vorteile von ARNI bei PH mit verschiedenen Arten von LHF- und RV-Dysfunktionen hervorgehoben werden. 1. EinleitungBei fortgeschrittener pulmonaler Hypertonie (PH) sind Belastungsintoleranz und ein Verlust von Kompensationsmechanismen weit verbreitet. Bei Patienten mit fortgeschrittener Linksherzinsuffizienz (LHF) kann die PH über einen längeren Zeitraum bestehen bleiben und als Marker für eine schlechte Prognose dienen. Durch die Umgestaltung der kleinen Pulmonalarterie erhöhen sich der pulmonalvaskuläre Widerstand (PVR) und der pulmonalarterielle Druck (PAP). Der rechte Ventrikel ist besonders anfällig für Drucküberlastung und kann das Herzzeitvolumen nicht länger durch Hypertrophie und erhöhte Kontraktilität aufrechterhalten (
1
,
2
). Im letzten Jahrzehnt haben PH und rechtsventrikuläre (RV) Dysfunktion bei LHF erhebliches Interesse geweckt (
3
,
4
). Allerdings ist eine wirksame Behandlung dieser komplexen Erkrankungen noch immer nicht verfügbar, sodass weitere Forschungen nach potenziellen Medikamenten erforderlich sind.Die Aktivierung des Renin-Angiotensin-Aldosteron-Systems (RAAS) trägt zunächst zu erhöhtem Blutdruck und erhöhter Herzkontraktilität bei, verschlimmert jedoch später das Herzinsuffizienz aufgrund von Flüssigkeitsretention. Eine Überaktivierung des RAAS fördert außerdem den Umbau der Lungengefäße und des rechten Ventrikels, indem sie Zellproliferation, Hypertrophie und Vasokonstriktion stimuliert (
5
). Der Umbau der Lungengefäße wird durch die Behandlung mit Angiotensin-Rezeptor-Antagonisten (ARBs) gemildert (
6
). Die Behandlung mit Angiotensin-Converting-Enzyme-Hemmern (ACEI) oder ARBs zeigte bei Patienten mit PAH günstige Sicherheits- und Verträglichkeitsprofile, und diese Personen mussten auch seltener wegen Herzinsuffizienz wieder ins Krankenhaus (
7
). Um den negativen Folgen einer abweichenden Aktivierung des RAAS entgegenzuwirken, setzt der Körper eine Gruppe vasoaktiver Peptide frei, die als natriuretische Peptide (NP) bezeichnet werden (
8
). Es wurde festgestellt, dass atriale NP (ANP), B-Typ NP (BNP) und C-Typ NP (CNP) vor einer PH-Progression schützen. Die Infusion von ANP und BNP verbesserte die Hämodynamik der menschlichen Lunge, während CNP die PH bei Versuchsratten verbesserte (
9
,
10
). ANP und BNP fördern die Gefäßerweiterung und verhindern eine Gefäßumgestaltung, wodurch sie den schädlichen Auswirkungen von RASS auf das Herz entgegenwirken. Sie üben auch eine antiproliferative Wirkung auf glatte Lungengefäßmuskelzellen aus (
11
,
12
). Trotz dieser Fortschritte bei der Abschwächung der PH-Progression bei HF haben Einzelmedikamente keine vielversprechenderen therapeutischen Wirkungen auf diese Erkrankung gezeigt.Sacubitril/Valsartan, bekannt als ARNI, behebt das Ungleichgewicht zwischen den RAAS- und NP-Systemen und zeigt eine signifikante Wirksamkeit bei LHF (
13
). Durch gleichzeitige Hemmung von Neprilysin und dem Angiotensin-AT1-Rezeptor unterdrückt ARNI profibrotische/prohypertrophe Mechanismen und fördert antifibrotische/antihypertrophe Mechanismen (
14
). Prostanoide, Endothelin-Rezeptorantagonisten oder Ca2 + -Kanalblocker wurden zur Behandlung von PH verwendet, aber die 5-Jahres-Überlebensrate bleibt unter 60 % (
15
). Echokardiographische Parameter einschließlich LVEF, systolischer PAP und Herzklappeninsuffizienz verbesserten sich nach einer ARNI-Therapie durchgängig (
16
). ARNI wirkt antitoxisch und vasodilatatorisch, indem es den cGMP-Signalweg verstärkt und den NP-Abbaud hemmt. Darüber hinaus bleibt ARNI wirksam, wenn andere Vasodilatatoren die PH nicht umkehren können. Durch Erhöhung des pulmonalarteriellen Pulsatilitätsindex und Senkung des PVR verbesserte ARNI die RV-PA-Kopplung, den Herzindex und die linksventrikuläre (LV) Funktion (
17
). Dieser Artikel konzentriert sich auf die neuesten Entwicklungen von ARNI in der Behandlung von PH, insbesondere in Verbindung mit LHF- und RV-Dysfunktion, da dies ein neuartiges und wenig erforschtes Gebiet ist.2. Pharmakologischer Mechanismus von Sacubitril/ValsartanKoronare Herzkrankheit und Bluthochdruck tragen zur systolischen LV-Dysfunktion bei und führen zu einer anhaltenden pathologischen Aktivierung des RAAS und des SNS (
8
). NPs werden freigesetzt, um die atriale und ventrikuläre Dilatation als Reaktion auf die Funktionsbeeinträchtigung des RAAS und des SNS auszugleichen. ANP, BNP und CNP besitzen natriuretische, diuretische, vasodilatatorische, antifibrotische und antihypertrophe Eigenschaften (
18
). Ihre Rolle bei HF wird jedoch durch die Vasokonstriktion und die Natriumrückhaltekapazität des RAAS überschattet.Die NP-Spaltung wird hauptsächlich durch die neutrale Endopeptidase Neprilysin (NEP) katalysiert. Die Hemmung von NEP erhöht die Bradykinin-, NP- und Adrenomedullin-Spiegel und mildert so die neurohormonale Aktivierung, die zu Natriumretention, Vasokonstriktion und kardialer Umgestaltung führt (
19
). NEP ist nicht nur am NP-Katabolismus beteiligt, sondern auch am Abbau anderer bioaktiver Peptide wie Adrenomedullin, Endothelin, Substanz P und Angiotensin II (Ang II). Obwohl die Hemmung von NEP allein die NP-Spiegel erhöht, könnte dieser Effekt durch einen gleichzeitigen Anstieg von Ang II und anderen Peptiden zunichte gemacht werden (
20
). Obwohl die diuretischen und natriuretischen Wirkungen von NEP-Hemmern nicht mit einer schädlichen RAAS-Aktivierung verbunden sind, führt die orale Verabreichung des Vorläuferarzneimittels Candoxatril nicht zu einer anhaltenden blutdrucksenkenden Wirkung. Das Ausbleiben eines blutdrucksenkenden Effekts durch NEP-Hemmer ist auf die Hemmung des NEP-Katabolismus zurückzuführen, welche zu einem Anstieg der Ang II- und Endothelin-1 (ET-1)-Spiegel führt und so den verstärkten gefäßerweiternden Effekt der NEP-Hemmung neutralisiert (
21
,
22
).Sacubitril/Valsartan ist ein ARNI des ersten Typs seiner Klasse, das aus dem molekularen Teil von Valsartan und dem NEP-Hemmer-Prodrug Sacubitril besteht. Im prospektiven Vergleich von ARNI mit ACEI zur Bestimmung der Auswirkungen auf die globale Mortalität und Morbidität bei Herzinsuffizienz (PARADIGM-HF) wurde beobachtet, dass ARNI die BNP- und cGMP-Werte durch NEP-Hemmung erhöhte (
23
). Die Blockade des Ang II-Rezeptors Typ 1 (AT1R) inaktivierte mehrere Tyrosin-phosphorylierte Proteine, die für Zellproliferation, Hypertrophie und Fibrose verantwortlich sind, darunter die JAK-Kinase-Familie (JAK2 und Tyk2) und die phosphorylierte Kinase C (PKC). Erhöhte NP-Werte erzeugten über den löslichen Guanosincyclase (sGC)/cGMP-Signalweg auch günstige biologische Wirkungen (
24
,
25
). Das Enzym PKG, das die Titinphosphorylierung vermittelt, wurde durch cGMP weiter verstärkt. Patienten mit Herzinsuffizienz mit erhaltener Ejektionsfraktion [HFpEF, definiert als linksventrikuläre Ejektionsfraktion (LVEF) ≥ 50 %] wiesen ein hohes Verhältnis von steifen (N2B) Isoformen zu nachgiebigen (N2BA) Isoformen auf. Die Phosphorylierung von N2B-Isoformen durch PKG verringerte die Ruhesteifigkeit der Kardiomyozyten (
14
). Darüber hinaus sanken während einer Nachbeobachtungszeit von 12 Wochen nach der Entlassung die NT-proBNP-Spiegel und das Risiko von Endpunktereignissen wie kardiovaskulärem Tod und erneuter Krankenhauseinweisung wegen HF bei Patienten mit HF, die weiterhin ARNI einnahmen, im Vergleich zu denen, die auf Enalapril umgestellt hatten, durchschnittlich um 30 % (
26
). Die Konzentrationen der Matrix-Metalloproteinase (MMP)-9 sowie ihres spezifischen Inhibitors, des Metalloproteinase-Gewebesinhibitors (TIMP)-1, und die Konzentrationen des Prokollagen-Aminoterminal-Präpropeptids Typ I (PINP) und Typ III (PIIINP) waren nach der ARNI-Behandlung verringert, was auf eine Abnahme der Kollagenfasern hindeutet (
27
).MicroRNAs (miRs) spielen eine Rolle bei der Regulierung der kardialen Apoptose, Angiogenese, Fibrose und Myokardhypertrophie und führen zu molekularen und strukturellen adaptiven Veränderungen, die sich auf die HF-Pathologie auswirken können (
28
). In einem Nagetiermodell für chronischen Myokardinfarkt führte die ARNI-Behandlung zur Herunterregulierung der miR-181a-Expression, was wiederum die Myokardfibrose und pathologische Hypertrophie abschwächte (
29
). Nach einem Jahr Nachbeobachtung bei Non-Respondern auf die kardiale Resynchronisationstherapie mit einem Defibrillator (CRTd) wiesen mit ARNI behandelte Patienten erhöhte miR-18- und miR-145-Spiegel und verringerte miR-181-Spiegel auf. Ein indirekter Beweis für die vorteilhaften epigenetischen Effekte von ARNI bei Patienten mit hohem Risiko und Therapieversagen wird durch die direkte Korrelation zwischen Plasma-miR-18- und miR-145-fachen Anstiegen mit EF-Verbesserungen und der inversen Korrelation mit NT-proBNP erbracht (
30
).3. Die RAAS und NPs in PHWenn das zirkulierende Blutvolumen (aufgrund von Blutverlust oder Dehydratation) oder das Herzzeitvolumen abnimmt, geben juxtaglomeruläre Zellen am lateralen Endothel der afferenten Arteriolen Renin in den Kreislauf ab. Die Hauptfunktion von Renin besteht in der Hydrolyse von aus der Leber ausgeschüttetem Angiotensinogen zu Angiotensin I (Ang I). In pulmonalarteriellen Endothelzellen spaltet ACE Ang I in Ang II, indem es zwei C-terminale Reste entfernt. Ang II reguliert die Freisetzung von Vasopressin aus dem zentralen Nervensystem hoch und induziert die Kontraktion von vaskulären glatten Muskelzellen im Lungenkreislauf sowie in systemischen arteriellen und venösen Kreisläufen (
31
).Tatsächlich ist das RAAS komplexer als der klassische Weg. Ang II kann durch Chymotrypsin in Mastzellen und Skelettmuskeln oder durch Cathepsin G in Entzündungszellen produziert werden (
32
). Die Bindung von Ang II an AT1-Rezeptoren verursacht eine Vasokonstriktion durch Hochregulierung von ET-1 oder Verringerung der NO-Bioverfügbarkeit. Die Stimulierung von AT1-Rezeptoren führt zur Migration und Proliferation von Gefäßglattmuskelzellen sowie zur Hypertrophie von Kardiomyozyten (
33
). ACE2, ein Homolog von ACE, konkurriert mit ACE1 um die Umwandlung von Ang II in Ang 1–7 und Ang 1–9. Die ACE2/Ang1–7/Mas-Rezeptorachse (MasR) hat bekanntermaßen kardioprotektive Wirkungen. Bei Patienten mit Typ-2-Diabetes (T2DM) und schlechter Glykämiekontrolle waren die Myokardspiegel von ACE2 und glykosyliertem ACE2 erhöht, während die Expression von Ang 1–9, Ang 1–7 und MasR reduziert war, was auf eine beeinträchtigte ACE2-Aktivität und die Anti-Remodelling-Wirkungen der Unterdrückung des Renin-Angiotensin-Systems (RAS) hindeutet. Anschließend wurden bei diesen Patienten und in explantierten Herzen von T2DM hohe Myokardfibrosewerte beobachtet (
34
,
35
). Ang (1–7) kann nicht nur durch Abspaltung eines Carboxylat-terminalen Rests von Ang II durch die Carboxypeptidase ACE2 produziert werden, sondern auch direkt aus Ang I durch NP und Prolyl-Carboxypeptidase. Die Bindung von Ang (1–7) an den G-Protein-gekoppelten MasR wirkt der Bindung von Ang II entgegen und erzeugt gefäßerweiternde Effekte, ohne die Aldosteronsekretion zu stimulieren (
36
,
37
). Die Plasma-Renin-Aktivität sowie die Werte von Ang I und Ang II waren bei Patienten mit PAH signifikant erhöht, was in positivem Zusammenhang mit der Krankheitsverschlechterung stand und das Risiko von Tod oder Lungentransplantation stark erhöhte. Die Rattengruppe mit arterieller Hypertonie, die eine Ang-II-Infusion erhielt, zeigte eine atriale und perivaskuläre Fibrose in der Aorta und den Pulmonalarterien mit erhöhter AT1-Rezeptorbindung in den großen Gefäßen, aber unveränderten Vorhöfen. Dies deutet darauf hin, dass diese Reaktionen nicht mit der Spannung der Ventrikelwände, sondern mit hormonellen Wirkungen des RAAS zusammenhingen (
38
). In Übereinstimmung damit förderte RAAS die Proliferation von glatten Muskelzellen der Pulmonalarterien durch eine erhöhte AT1-Rezeptorbindung bei Patienten mit idiopathischer PAH (iPAH) (
39
). In einem Ferkel-Überlaufmodell führte Losartan zu einer 51%igen bzw. 35%igen Reduktion des Shunt-induzierten PVR und der medialen Dicke. Der verringerte PVR ging mit einem anhaltenden Anstieg der ET-1-, ETB-Rezeptor- und Ang1-Expression einher, was darauf hindeutet, dass Ang-II-Antagonisten und ET-Rezeptorblocker bei früher PAH kombiniert werden könnten (
40
). Ang II bindet vorwiegend an den Angiotensin-Typ-1-Rezeptor (AGTR1), um die Kontraktion der Gefäßglattmuskulatur zu fördern. Chung WK et al. entdeckten eine Korrelation zwischen AGTR1 und dem Alter bei der Diagnose der iPAH, während keine solche Korrelation mit AGT, ACE, CMA1 oder CYP11B2 gefunden wurde. Dieser Befund legt nahe, dass Losartan eine Rolle bei der Verzögerung des Fortschreitens der PAH-Krankheit spielen könnte (
41
).Der pulmonalvaskuläre Umbau ist durch Hyperplasie der Media und Neomuskularisierung der subendothelialen Schicht gekennzeichnet, was zu vasodilatatorischer Dysfunktion, Verengung des Arterienlumens und erhöhtem PAP führt. ANP und BNP sind mit der Pathogenese von Myokardhypertrophie und -fibrose verbunden (
42
). Obwohl BNP primär durch die Dehnung von Kardiomyozyten ausgelöst wird, ist es bei PH hochreguliert (
43
). Durch Aktivierung des partikulären Guanylylcyclase-gekoppelten Rezeptors und des natriuretischen Peptidrezeptors A (NPR-A) vermittelt BNP traditionell vasodilatatorische Effekte, um die intrazellulären cGMP-Spiegel zu erhöhen (
44
). (
Abbildung 1
) Wijeyaratne CN et al. fanden heraus, dass BNP auch die Proliferation von Gefäßglattmuskelzellen hemmt und dem RAAS entgegenwirkt, wodurch der pulmonalvaskuläre Umbau abgeschwächt und die Synthese von Wachstumsfaktoren wie Endothelin gehemmt wird (
45
). Die Infusion des humanen BNP Nesiritid senkte bei Patienten mit HF und PH den rechten Vorhofdruck, den mittleren PAP und den postpulmonalen kapillären Verschlussdruck (PCWP) und erhöhte so das Herzzeitvolumen (
46
). Die Werte des vasodilatatorischen Stickoxids (NOx) waren bei Patienten mit PH reduziert, aber die Expression von NOx-Rezeptoren und ET-1 war erhöht. Nesiritid erhöhte die NOx- und cGMP-Spiegel signifikant und förderte so die Vasodilatation bei diesen Patienten (
47
). Nesiritid hat möglicherweise das therapeutische Potenzial, das Fortschreiten einer RV-Dysfunktion zu verlangsamen. Nesiritid senkte nach 3-stündiger Verabreichung schnell den PCWP und erhöhte das Schlagvolumen und das Herzzeitvolumen, wobei diese Wirkungen mindestens 24 Stunden anhielten (
48
). Obwohl BNP alleine keinen signifikanten Effekt auf die pulmonale Hämodynamik hatte, verstärkte es die diastolische Wirkung des Phosphodiesterase-5-Hemmers Sildenafil auf das pulmonale Gefäßsystem (
44
). Abbildung 1
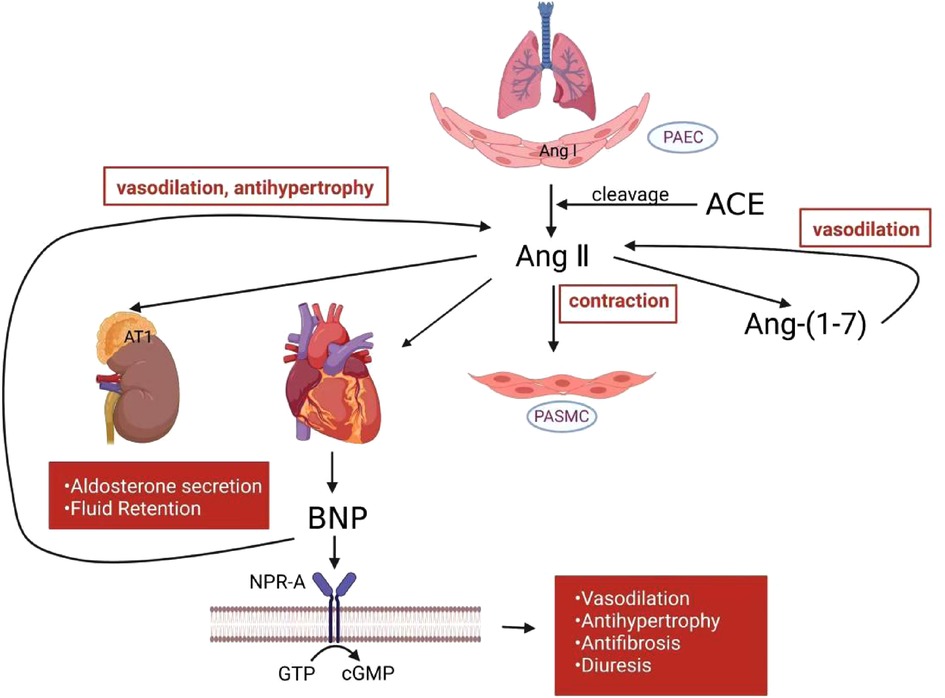 Abbildung 1 . RAAS- und NP-Mechanismus bei PH. Im Lungenkreislauf induzieren aktivierte RAAS eine Kontraktion glatter Muskelzellen. Angiotensin-(1–7) wirkt Angiotensin II entgegen und erzeugt gefäßerweiternde Wirkungen. Aus der Herzkammer freigesetztes BNP wirkt RAAS entgegen und schwächt Gefäßverengung, Hypertrophie, Fibrose und andere schädliche Wirkungen ab. RAAS, Renin-Angiotensin-Aldosteron-System; NP, natriuretisches Peptid; PH, pulmonale Hypertonie; PAEC, pulmonalarterielle Endothelzellen; PASMC, pulmonalarterielle glatte Muskelzelle; Ang I, Angiotensin I; Ang II, Angiotensin II; Ang-(1–7), Angiotensin-(1–7); ACE, Angiotensin-Converting-Enzym; BNP, B-Typ natriuretisches Peptid; NPR-A, natriuretischer Peptidrezeptor-A; GTP, Guanosintriphosphat; cGMP, zyklisches Guanosinmonophosphat. 4. Sacubitril/Valsartan bei PH mit verschiedenen LHF-TypenDas 5. Weltsymposium zur PH schlug vor, die PH in fünf Kategorien zu klassifizieren: (1) PH aufgrund einer pulmonal-vaskulären Erkrankung; (2) PH aufgrund einer Linksherzerkrankung; (3) PH aufgrund einer Lungenerkrankung oder Hypoxie; (4) PH aufgrund einer chronischen thromboembolischen Erkrankung; (5) eine gemischte Sammlung von PH-Syndromen, die durch eine Vielzahl von Krankheiten hervorgerufen werden, darunter hämolytische Anämien und Sarkoidose (
49
).4.1. Charakterisierung der PH in HFrEF und HFpEFLHD ist eine der häufigsten Ursachen für PH und wird üblicherweise als postkapilläre PH oder PH der Gruppe 2 klassifiziert. Zu den hämodynamischen Parametern, die das Überleben und die Prognose bei Patienten mit HF vorhersagen, zählen der pulmonalarterielle Verschlussdruck (PAWP), der mittlere PAP und PVR sowie die PA-Compliance/Kapazität (
50
,
51
). Bei postkapillärer PH führt eine Erhöhung des PAWP zu einer entsprechenden Erhöhung des mittleren PAP, um einen durchschnittlichen transpulmonalen Druckgradienten (TPG = mPAP—PAWP) von weniger als 12 mmHg aufrechtzuerhalten (
52
). Der TPG wird jedoch von der Volumenbelastung und der Herzfunktion beeinflusst, die bei PH-LHD keinen Rückschluss auf die Prognose zulassen. Der diastolische Druckgradient (DPG), der durch die Differenz zwischen diastolischem PAP und PAWP bestimmt wird, gilt als weniger abhängig vom Schlagvolumen und den Belastungsbedingungen. Bei Patienten mit prä- und postkapillärer (Cpc)-PH und mit DPG ≥ 7 mmHg wurden Intimahypertrophie, Fibrose der Intima und der äußeren Membran sowie Gefäßverschlüsse beobachtet, was darauf hindeutet, dass eine verringerte pulmonalvaskuläre Compliance auch eine proliferative Vaskulopathie kleiner Gefäße verursachen kann (
53
,
54
). Allerdings hatten Patienten mit PH-LDH und DPG ≥ 7 mmHg eine niedrigere Überlebensrate als Patienten mit DPG < 7 mmHg, und DPG war nur minimal aussagekräftig für eine idiopathische Kardiomyopathie (
55
). Durch Anwendung des Support Vector Machine-Recursive Feature Elimination Algorithm fand unsere Gruppe heraus, dass EPB42 und IFIT2 bei PAH-Patienten stark exprimiert waren, während FOSB und SNF1LK entgegengesetzte Trends zeigten. Diese vier potenziellen Gene könnten PH-Patienten von gesunden Personen unterscheiden und zur Frühdiagnose von PH verwendet werden (
56
).Bis zu 60 % der Patienten mit schwerer systolischer LV-Insuffizienz und 70 % der Patienten mit reiner diastolischer LV-Insuffizienz können eine PH entwickeln (
57
,
58
). Es gab auch Unterschiede zwischen PH-HFrEF [Herzinsuffizienz mit reduzierter Ejektionsfraktion, definiert als linksventrikuläre Ejektionsfraktion (LVEF) < 40 %] und PH-HFpEF. In einem Bericht, der retrospektive und prospektive Daten kombinierte und DPG > 7 mmHg als Diagnosekriterium verwendete, betrugen die Cpc-PH-Werte für HFpEF und HFrEF 22,6 % bzw. 18,8 % (
59
). Bei ähnlichen DPG-Grenzwerten war die bei PH-HFpEF beobachtete Cpc-PH-Rate mehr als doppelt so hoch wie die bei PH-HFrEF (
60
). Patienten mit HFrEF im Stadium D können jedoch auch einen Cpc-PH-LHD-Phänotyp mit spezifischen Manifestationen von mittlerem PAP > 25 mmHg, PCWP > 15 mmHg, DPG > 7 mmHg und PVR > 3 WU (
61
) aufweisen. Bei HFrEF und HFpEF ist der auslösende Faktor für PH eine beeinträchtigte diastolische und Füllungsfunktion des LV, wodurch ein erhöhter linksatrialer Druck schließlich die rechte Herzhälfte erreichen kann. Die Art der LV-Kardiomyozytenhypertrophie und das Ausmaß der reaktiven und alternativen Fibrose unterscheiden sich gut zwischen HFpEF und HFrEF (
62
). HFrEF tritt häufiger bei Erkrankungen wie ischämischer Kardiomyopathie, dilatativer Kardiomyopathie und sekundärer Mitralklappeninsuffizienz auf. Die primären Mechanismen der HFrEF-Entstehung sind Kardiomyozytenverlängerung und Verlust der LV-Compliance. Eine beeinträchtigte Kinetik des linken Vorhofs bildet die Grundlage für die PH-Erhöhung. HFrEF präsentiert sich vorwiegend durch eine erhöhte linksatriale und exzentrische Umgestaltung infolge einer schweren Mitralklappeninsuffizienz. Insbesondere bei Patienten mit HFrEF und LV-Dilatation ist eine funktionelle Mitralklappeninsuffizienz häufig und kann eine potenziell signifikante Ursache für PH sein. Bei diesen Patienten konnte durch eine Mitralklappenreparatur die pulmonale Hämodynamik signifikant verbessert werden, einschließlich der Senkung des mittleren PAP und PAWP (
63
,
64
). Patienten mit Hypertonie, Adipositas und Diabetes mellitus sind anfällig für HFpEF, die zu einer zentripetalen Hypertrophie des linken Ventrikels und einer erhöhten diastolischen Steifheit führt. Sogar in den frühen Stadien der HFpEF wurden bei körperlicher Belastung ungünstige diastolische ventrikuläre Interaktionen beobachtet, die als primärer Mechanismus einer erhöhten PAWP beim adipösen Phänotyp dienen (
65
).4.2. Klinische Anwendung von Sacubitril/Valsartan bei PH mit HFrEF und HFpEFEine retrospektive Kohortenstudie ergab, dass Patienten mit HFrEF sechs Monate nach Beginn der Behandlung mit ARNI eine signifikante Abnahme des systolischen Pulmonalarteriendrucks (PASP) aufwiesen, was in Verbindung mit einer umgekehrten LV-Umgestaltung zu einer besseren Prognose führte. Dieser Effekt von ARNI scheint nicht von anderen Medikamenten abhängig zu sein (
66
). In Realweltstudien wurde beobachtet, dass ARNI das endsystolische LV-Volumen und den systolischen PAP bei Patienten mit HFrEF über sechs Monate hinweg senkte, sogar bei einer reduzierten Furosemiddosis (
67
). Es wurden auch geschlechtsspezifische Unterschiede in der Wirkung der anfänglichen ARNI-Behandlung auf den PAP beobachtet. Nach bis zu 12 Monaten zeigten LVEF, relative Wanddicke und E/A bei Frauen keine größeren Verbesserungen als bei Männern, aber der linke Vorhofdurchmesser und der PAP waren bei Frauen überlegen (
68
). Bei Patienten mit HFrEF, die ACEI oder ARB einnahmen, kam es nach der Umstellung auf ARNI, einem neuen Mittel der ersten Wahl bei HF, zu einer raschen Senkung des PAP-Werts. ARNI erwies sich bei Patienten mit niedrigem TPG, relativ normalem PVR sowie erhöhtem TPG und (oder) PVR als ebenso wirksam (
69
).Die pulmonalarterielle Steifheit (PAS) ist ein entscheidender Faktor für die Entstehung von Pulmonalsklerose, die durch erhöhte Gefäßsteifigkeit, pulmonalarterielle endotheliale Dysfunktion und Entzündungen gekennzeichnet ist (
70
). Neue nicht-invasive Verfahren wie die Echokardiographie und die kardiale Magnetresonanztomographie (MRT) können PAP und Gefäßwiderstand quantifizieren (
71
). Die PAS war bei Patienten mit HFrEF signifikant erhöht und stand in unabhängigem Zusammenhang mit dem Schweregrad der funktionellen Klasse der New York Heart Association (NYHA). Eine aktuelle Studie hat gezeigt, dass nach sechsmonatiger ARNI-Gabe bei Patienten mit HFrEF eine signifikante Abnahme der PAS auftrat, berechnet aus der maximalen Frequenzverschiebung und Beschleunigungszeit der pulmonalarteriellen Flusskurve. Die Studie zeigte auch eine signifikante Verbesserung des LV-Remodelings, der RV-Funktion und der Belastungstoleranz (
72
).Bei PARAGON-HF (Prospective Comparison of ARNI With ARB Global Outcomes in HF With Preserved Ejection Fraction) handelt es sich um eine multizentrische, internationale, randomisierte, doppelblinde, ereignisgesteuerte Studie zum Vergleich der langfristigen Wirksamkeit und Sicherheit von ARNI vs. Valsartan allein bei Patienten mit chronischem HF und einer LVEF von > 45 %. Die Prävalenz von PH bei Patienten mit HFpEF lag bei fast einem Drittel, und ein erhöhter PASP könnte als unabhängiger Risikofaktor zur Vorhersage der Mortalität bei Patienten mit HFpEF in der Studie dienen (
73
). Bei hospitalisierten HF-Patienten mit deutlich erhöhtem PASP war bei HFpEF-PH eine höhere 5-Jahres-Mortalitätsrate festzustellen, möglicherweise weil mehrere Therapieschemata zur Senkung der HFrEF-Mortalität eingesetzt wurden. Bei einer Untergruppe der Patienten mit HFpEF schien eine intrinsische pulmonalvaskuläre Erkrankung zu entwickeln, was sich durch erhöhten mPAP und einen Anstieg von PVR und TPG zeigte (
74
). Aktuelle Studien haben gezeigt, dass ARNI bei Patienten mit HFpEF-PH ebenso wirksam war und dass selbst die niedrigste ARNI-Dosis den PAP und den mittleren PCWP bei Patienten mit HFpEF signifikant reduzierte. Es verbesserten sich nicht nur die hämodynamischen Parameter, sondern auch die NYHA-Funktionsklasse wurde um mindestens eine Stufe angehoben (
75
) (
Tabelle 1
). Tabelle 1
Abbildung 1 . RAAS- und NP-Mechanismus bei PH. Im Lungenkreislauf induzieren aktivierte RAAS eine Kontraktion glatter Muskelzellen. Angiotensin-(1–7) wirkt Angiotensin II entgegen und erzeugt gefäßerweiternde Wirkungen. Aus der Herzkammer freigesetztes BNP wirkt RAAS entgegen und schwächt Gefäßverengung, Hypertrophie, Fibrose und andere schädliche Wirkungen ab. RAAS, Renin-Angiotensin-Aldosteron-System; NP, natriuretisches Peptid; PH, pulmonale Hypertonie; PAEC, pulmonalarterielle Endothelzellen; PASMC, pulmonalarterielle glatte Muskelzelle; Ang I, Angiotensin I; Ang II, Angiotensin II; Ang-(1–7), Angiotensin-(1–7); ACE, Angiotensin-Converting-Enzym; BNP, B-Typ natriuretisches Peptid; NPR-A, natriuretischer Peptidrezeptor-A; GTP, Guanosintriphosphat; cGMP, zyklisches Guanosinmonophosphat. 4. Sacubitril/Valsartan bei PH mit verschiedenen LHF-TypenDas 5. Weltsymposium zur PH schlug vor, die PH in fünf Kategorien zu klassifizieren: (1) PH aufgrund einer pulmonal-vaskulären Erkrankung; (2) PH aufgrund einer Linksherzerkrankung; (3) PH aufgrund einer Lungenerkrankung oder Hypoxie; (4) PH aufgrund einer chronischen thromboembolischen Erkrankung; (5) eine gemischte Sammlung von PH-Syndromen, die durch eine Vielzahl von Krankheiten hervorgerufen werden, darunter hämolytische Anämien und Sarkoidose (
49
).4.1. Charakterisierung der PH in HFrEF und HFpEFLHD ist eine der häufigsten Ursachen für PH und wird üblicherweise als postkapilläre PH oder PH der Gruppe 2 klassifiziert. Zu den hämodynamischen Parametern, die das Überleben und die Prognose bei Patienten mit HF vorhersagen, zählen der pulmonalarterielle Verschlussdruck (PAWP), der mittlere PAP und PVR sowie die PA-Compliance/Kapazität (
50
,
51
). Bei postkapillärer PH führt eine Erhöhung des PAWP zu einer entsprechenden Erhöhung des mittleren PAP, um einen durchschnittlichen transpulmonalen Druckgradienten (TPG = mPAP—PAWP) von weniger als 12 mmHg aufrechtzuerhalten (
52
). Der TPG wird jedoch von der Volumenbelastung und der Herzfunktion beeinflusst, die bei PH-LHD keinen Rückschluss auf die Prognose zulassen. Der diastolische Druckgradient (DPG), der durch die Differenz zwischen diastolischem PAP und PAWP bestimmt wird, gilt als weniger abhängig vom Schlagvolumen und den Belastungsbedingungen. Bei Patienten mit prä- und postkapillärer (Cpc)-PH und mit DPG ≥ 7 mmHg wurden Intimahypertrophie, Fibrose der Intima und der äußeren Membran sowie Gefäßverschlüsse beobachtet, was darauf hindeutet, dass eine verringerte pulmonalvaskuläre Compliance auch eine proliferative Vaskulopathie kleiner Gefäße verursachen kann (
53
,
54
). Allerdings hatten Patienten mit PH-LDH und DPG ≥ 7 mmHg eine niedrigere Überlebensrate als Patienten mit DPG < 7 mmHg, und DPG war nur minimal aussagekräftig für eine idiopathische Kardiomyopathie (
55
). Durch Anwendung des Support Vector Machine-Recursive Feature Elimination Algorithm fand unsere Gruppe heraus, dass EPB42 und IFIT2 bei PAH-Patienten stark exprimiert waren, während FOSB und SNF1LK entgegengesetzte Trends zeigten. Diese vier potenziellen Gene könnten PH-Patienten von gesunden Personen unterscheiden und zur Frühdiagnose von PH verwendet werden (
56
).Bis zu 60 % der Patienten mit schwerer systolischer LV-Insuffizienz und 70 % der Patienten mit reiner diastolischer LV-Insuffizienz können eine PH entwickeln (
57
,
58
). Es gab auch Unterschiede zwischen PH-HFrEF [Herzinsuffizienz mit reduzierter Ejektionsfraktion, definiert als linksventrikuläre Ejektionsfraktion (LVEF) < 40 %] und PH-HFpEF. In einem Bericht, der retrospektive und prospektive Daten kombinierte und DPG > 7 mmHg als Diagnosekriterium verwendete, betrugen die Cpc-PH-Werte für HFpEF und HFrEF 22,6 % bzw. 18,8 % (
59
). Bei ähnlichen DPG-Grenzwerten war die bei PH-HFpEF beobachtete Cpc-PH-Rate mehr als doppelt so hoch wie die bei PH-HFrEF (
60
). Patienten mit HFrEF im Stadium D können jedoch auch einen Cpc-PH-LHD-Phänotyp mit spezifischen Manifestationen von mittlerem PAP > 25 mmHg, PCWP > 15 mmHg, DPG > 7 mmHg und PVR > 3 WU (
61
) aufweisen. Bei HFrEF und HFpEF ist der auslösende Faktor für PH eine beeinträchtigte diastolische und Füllungsfunktion des LV, wodurch ein erhöhter linksatrialer Druck schließlich die rechte Herzhälfte erreichen kann. Die Art der LV-Kardiomyozytenhypertrophie und das Ausmaß der reaktiven und alternativen Fibrose unterscheiden sich gut zwischen HFpEF und HFrEF (
62
). HFrEF tritt häufiger bei Erkrankungen wie ischämischer Kardiomyopathie, dilatativer Kardiomyopathie und sekundärer Mitralklappeninsuffizienz auf. Die primären Mechanismen der HFrEF-Entstehung sind Kardiomyozytenverlängerung und Verlust der LV-Compliance. Eine beeinträchtigte Kinetik des linken Vorhofs bildet die Grundlage für die PH-Erhöhung. HFrEF präsentiert sich vorwiegend durch eine erhöhte linksatriale und exzentrische Umgestaltung infolge einer schweren Mitralklappeninsuffizienz. Insbesondere bei Patienten mit HFrEF und LV-Dilatation ist eine funktionelle Mitralklappeninsuffizienz häufig und kann eine potenziell signifikante Ursache für PH sein. Bei diesen Patienten konnte durch eine Mitralklappenreparatur die pulmonale Hämodynamik signifikant verbessert werden, einschließlich der Senkung des mittleren PAP und PAWP (
63
,
64
). Patienten mit Hypertonie, Adipositas und Diabetes mellitus sind anfällig für HFpEF, die zu einer zentripetalen Hypertrophie des linken Ventrikels und einer erhöhten diastolischen Steifheit führt. Sogar in den frühen Stadien der HFpEF wurden bei körperlicher Belastung ungünstige diastolische ventrikuläre Interaktionen beobachtet, die als primärer Mechanismus einer erhöhten PAWP beim adipösen Phänotyp dienen (
65
).4.2. Klinische Anwendung von Sacubitril/Valsartan bei PH mit HFrEF und HFpEFEine retrospektive Kohortenstudie ergab, dass Patienten mit HFrEF sechs Monate nach Beginn der Behandlung mit ARNI eine signifikante Abnahme des systolischen Pulmonalarteriendrucks (PASP) aufwiesen, was in Verbindung mit einer umgekehrten LV-Umgestaltung zu einer besseren Prognose führte. Dieser Effekt von ARNI scheint nicht von anderen Medikamenten abhängig zu sein (
66
). In Realweltstudien wurde beobachtet, dass ARNI das endsystolische LV-Volumen und den systolischen PAP bei Patienten mit HFrEF über sechs Monate hinweg senkte, sogar bei einer reduzierten Furosemiddosis (
67
). Es wurden auch geschlechtsspezifische Unterschiede in der Wirkung der anfänglichen ARNI-Behandlung auf den PAP beobachtet. Nach bis zu 12 Monaten zeigten LVEF, relative Wanddicke und E/A bei Frauen keine größeren Verbesserungen als bei Männern, aber der linke Vorhofdurchmesser und der PAP waren bei Frauen überlegen (
68
). Bei Patienten mit HFrEF, die ACEI oder ARB einnahmen, kam es nach der Umstellung auf ARNI, einem neuen Mittel der ersten Wahl bei HF, zu einer raschen Senkung des PAP-Werts. ARNI erwies sich bei Patienten mit niedrigem TPG, relativ normalem PVR sowie erhöhtem TPG und (oder) PVR als ebenso wirksam (
69
).Die pulmonalarterielle Steifheit (PAS) ist ein entscheidender Faktor für die Entstehung von Pulmonalsklerose, die durch erhöhte Gefäßsteifigkeit, pulmonalarterielle endotheliale Dysfunktion und Entzündungen gekennzeichnet ist (
70
). Neue nicht-invasive Verfahren wie die Echokardiographie und die kardiale Magnetresonanztomographie (MRT) können PAP und Gefäßwiderstand quantifizieren (
71
). Die PAS war bei Patienten mit HFrEF signifikant erhöht und stand in unabhängigem Zusammenhang mit dem Schweregrad der funktionellen Klasse der New York Heart Association (NYHA). Eine aktuelle Studie hat gezeigt, dass nach sechsmonatiger ARNI-Gabe bei Patienten mit HFrEF eine signifikante Abnahme der PAS auftrat, berechnet aus der maximalen Frequenzverschiebung und Beschleunigungszeit der pulmonalarteriellen Flusskurve. Die Studie zeigte auch eine signifikante Verbesserung des LV-Remodelings, der RV-Funktion und der Belastungstoleranz (
72
).Bei PARAGON-HF (Prospective Comparison of ARNI With ARB Global Outcomes in HF With Preserved Ejection Fraction) handelt es sich um eine multizentrische, internationale, randomisierte, doppelblinde, ereignisgesteuerte Studie zum Vergleich der langfristigen Wirksamkeit und Sicherheit von ARNI vs. Valsartan allein bei Patienten mit chronischem HF und einer LVEF von > 45 %. Die Prävalenz von PH bei Patienten mit HFpEF lag bei fast einem Drittel, und ein erhöhter PASP könnte als unabhängiger Risikofaktor zur Vorhersage der Mortalität bei Patienten mit HFpEF in der Studie dienen (
73
). Bei hospitalisierten HF-Patienten mit deutlich erhöhtem PASP war bei HFpEF-PH eine höhere 5-Jahres-Mortalitätsrate festzustellen, möglicherweise weil mehrere Therapieschemata zur Senkung der HFrEF-Mortalität eingesetzt wurden. Bei einer Untergruppe der Patienten mit HFpEF schien eine intrinsische pulmonalvaskuläre Erkrankung zu entwickeln, was sich durch erhöhten mPAP und einen Anstieg von PVR und TPG zeigte (
74
). Aktuelle Studien haben gezeigt, dass ARNI bei Patienten mit HFpEF-PH ebenso wirksam war und dass selbst die niedrigste ARNI-Dosis den PAP und den mittleren PCWP bei Patienten mit HFpEF signifikant reduzierte. Es verbesserten sich nicht nur die hämodynamischen Parameter, sondern auch die NYHA-Funktionsklasse wurde um mindestens eine Stufe angehoben (
75
) (
Tabelle 1
). Tabelle 1
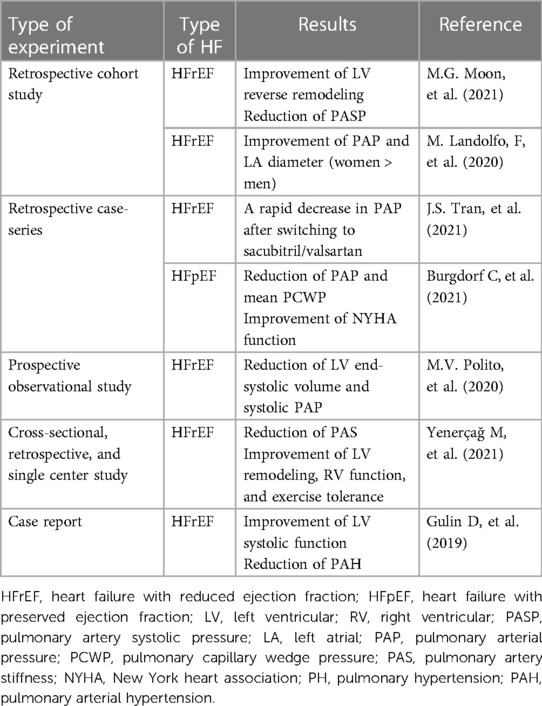 Tabelle 1. Auswirkungen von Sacubitril/Valsartan auf PH bei Patienten mit HFrEF und HFpEF. 5. Auswirkungen von Sacubitril/Valsartan auf PH mit rechtsventrikulärer DysfunktionEin erhöhter mittlerer PAP reicht nicht aus, um eine pulmonalvaskuläre Erkrankung zu definieren, da die Ursachen für PH unterschiedlich sein können, darunter erhöhtes Herzzeitvolumen, erhöhter pulmonaler Verschlussdruck und Hyperviskosität. Beim 6. Weltsymposium zu PH wurde zudem empfohlen, DPG von der Definition der Cpc-PH auszuschließen, da es nicht unbedingt ein schlechter Prognosefaktor ist (
76
). Daher bleibt es umstritten, ob DPG für die Prognose der LHD-PH wichtig ist, da die zugrunde liegenden Krankheiten, die eine LV-Dysfunktion verursachen, unterschiedlich sein können. Eine Beeinträchtigung der kontraktilen Funktion des rechten Ventrikels und eine erhöhte Nachlast infolge einer PAH können beide zu einer RV-Dysfunktion beitragen (
77
).Chronische Rechtsherzinsuffizienz (RHF) ist das Ergebnis einer langfristigen Erhöhung der RV-Nachlast, die die Kompensationsmechanismen des RV schließlich überfordert. Adrenalin stimuliert die kompensierenden Antriebsmechanismen, die die systolische Herzfunktion bei erhöhter RV-Nachlast aufrechterhalten, führt aber letztendlich zu einer Myokardfunktionsstörung, wenn es über einen längeren Zeitraum anhält (
33
). Darüber hinaus führt die anhaltende Erhöhung des adrenergen Tonus zu einer Herunterregulierung der myokardialen Betarezeptoren des RV und zur Erschöpfung der Noradrenalinreserven (
78
). Eine kürzlich durchgeführte nuklearbildgebende Studie an einer kleinen Gruppe von Patienten mit PAH legte nahe, dass diese Patienten möglicherweise eine erhebliche sympathische Funktionsstörung haben. Im Vergleich zur Kontrollgruppe zeigte die kardiale (
79
) Jod-Metaiodobenzylguanidin-Aufnahme eine verringerte LVEF in der PH-Gruppe. Herz-Mediastinum-Verhältnisse und Auswaschrate sind mit PVR, rechtem Vorhofdruck, systolischer Exkursion in der Trikuspidalebene, NT-proBNP und maximalem VO2 assoziiert ( 80
)
. In einem Kaninchenmodell mit systemischer RV-Nachlast, die durch ein Pulmonalarterienband induziert wurde, führten ventrikulär-ventrikuläre Interaktionen über die TGF-b1-, CTGF- und ET-1-Signalwege nicht nur zu RV-Hypertrophie, sondern auch zu sekundärer LV-Fibrose und RV-Apoptose. Eine Blockade des Ang-II-Rezeptors mit Losartan linderte jedoch diese interventrikuläre Wechselwirkung. Bemerkenswerterweise nahm die LV-CTGF-mRNA-Expression nach der Behandlung mit einem Pulmonalarterienband zu, und Losartan verringerte die durch das Pulmonalarterienband induzierte CTGF-mRNA-Expression (
81
). Da die pulmonale RAAS-Aktivität mit der Prognose bei Patienten mit iPAH korreliert, kann aus diesem Experiment die Hypothese abgeleitet werden, dass Losartan durch Blockierung profibrotischer Signale die RV-Hypertrophie umkehren und die LV-Belastung verringern kann. Es wurde auch festgestellt, dass Telmisartan die RV-Umgestaltung verbessert, möglicherweise durch Hemmung der MMP-2- und MMP-9-Aktivität (
82
). Borgdorff MA et al. entdeckten jedoch, dass Losartan in Kombination mit Eplerenon weder die systolische und diastolische RV-Funktion verbesserte noch Myokardfibrose und RV-Hypertrophie verhinderte (
83
). Der Grund für diesen Kontrast könnte der physiologische Unterschied zwischen LV und RV sein oder die Hemmung des RAAS als Folge der Blockade von AT1R auf das Lungengefäßsystem und nicht die direkte myokardiale Wirkung auf den RV. Doppler-Ultraschall und kardiopulmonale Belastungstests zeigten, dass Losartan PAP und den Durchmesser des rechten Vorhofs senkte und die Belastungstoleranz der Patienten verbesserte (
84
). Unterschiede in der Physiologie und der komplexen pathologischen Struktur des Herzens von Mensch und Nagetier könnten das Problem erklären. Um den Druck auf der rechten Seite des Herzens genau messen zu können, sind zuverlässigere Beweise aus invasiven Tests (Platzierung von Herzkathetern) erforderlich.Eine RV-Dysfunktion bedeutet ein Fortschreiten der Herzinsuffizienz und kann sogar zu einem schlechteren Prognosefaktor werden (
85
). Im Vergleich mit dem unabhängigen RV-Versagensmodell, das durch eine Bänderung des Lungenstamms induziert wurde, reduzierte ARNI den systolischen RV-Druck (RVSP), die RV-Hypertrophie sowie das enddiastolische und endsystolische RV-Volumen in der Gruppe mit PH signifikant. Dies deutet darauf hin, dass ARNI die RV-Umgestaltung möglicherweise nicht direkt beeinflusst, aber Vorteile für die rechte Herzhälfte bringt, indem es die pulmonalvaskuläre Funktion verbessert (
86
). Die transmurale Neuausrichtung von Kollagen und Myofasern durch RV-Hypertrophie wurde ebenfalls geschwächt, was darauf hindeutet, dass die Wirkung von ARNI auf die RV-Umgestaltung sich nicht nur in der Hämodynamik, sondern auch in den biomechanischen Eigenschaften des RV auf Gewebeebene manifestierte (
87
). ARNI allein kann PAP und RV-Umgestaltung durch eine Erhöhung der endogenen NP verringern. Clements RT et al. behandelten das durch SU5146 und Hypoxie induzierte PH-Rattenmodell sechs Wochen lang mit ARNI und stellten einen Rückgang des RV-Drucks und der Fibrose fest, begleitet von einem Anstieg der pulmonalen ANP-, BNP- und cGMP-Spiegel (
88
). Bosentan, ein spezifischer und kompetitiver dualer Endothelin-Rezeptorblocker mit niedrigem Molekulargewicht, ist das erste neuartige orale Medikament, das zur Behandlung von PAH zugelassen wurde. Bosentan wirkt jedoch in erster Linie über die Erweiterung der Lungengefäße, ohne direkt eine RHF zu verhindern. Im Monocrotalin-induzierten Rattenmodell mit schwerer PH verstärkte ARNI die Wirkung von Bosentan auf die Verringerung von PVR, RV-Hypertrophie und Fibrose. Gleichzeitig bestätigten kultivierte menschliche pulmonalarterielle glatte Muskelzellen von iPAH-Patienten die antiproliferative Wirkung von ARNI (
89
). ARNI könnte also eine synergistische Wirkung auf traditionelle Medikamente zur Behandlung von PH haben. Der Verlust des NO-Signalwegs führt bei PH-Patienten typischerweise zu einer endothelialen Dysfunktion, gefolgt von einer kompensatorischen Vasodilatation, die durch den natriuretischen Peptid-Clearance-Rezeptor (NPR-C) vermittelt wird. Die Aktivierung des NPR-C-Signalwegs kann antiproliferative Effekte aufweisen, während eine durch Hypoxie induzierte Herunterregulierung der NPR-C-Expression zu einer Umgestaltung der Lungengefäße und erhöhtem PAP führen kann (
90
).Ein weiterer Mechanismus in der Pathogenese von Lungengefäßerkrankungen ist die entzündliche Infiltration, bei der es zur Ansammlung von extrazellulären Matrixproteinen wie Fibronektin kommt (
91
). Bei Ratten, die mit Monocrotalin oder Hypoxie behandelt wurden, erhöhte ARNI nicht nur die ANP- und CNP-Spiegel im zirkulierenden Blut und Lungengewebe, sondern zeigte auch die gleiche Tendenz bei der Expression von NPR-A, C und cGMP. Die zirkulierenden IL-1β-, IL-6- und TNF-α-Spiegel, die einer ARNI-Intervention unterzogen wurden, waren in beiden Tiermodellen reduziert, und die entzündungshemmende Wirkung könnte mit dem ANP/NPR-A/cGMP-Signalweg zusammenhängen (
92
).6. Wirkungen und Nebenwirkungen von Sacubitril/Valsartan bei PH bei fortgeschrittener HF und chronischer NierenerkrankungLangfristiger Druck im linken Vorhof führt bei Patienten mit fortgeschrittener HFrEF zu schwerer PH, was sie für eine Herztransplantation disqualifizieren könnte. Während konventionelle Behandlungen wie Diurese, Vasodilatationstherapie und mechanische Unterstützung keine erkennbare Wirksamkeit zeigten, führte experimentelles ARNI zu besseren Ergebnissen als erwartet. Nach 24-stündiger ARNI-Gabe waren PASP und PVR signifikant reduziert, sodass vier Patienten in realen Fällen wieder für eine Herztransplantation geeignet waren, ohne dass postoperativer RHF oder Hypotonie eine vaskuläre Kompressionsunterstützung erforderlich machte (
17
).Zusätzlich zur HFrEF entwickeln erwachsene Patienten mit angeborenen Herzfehlern eine subpulmonalarterielle ventrikuläre Dysfunktion und PH. Lluri G et al. berichteten, dass bei vier Patienten mit Zyanose, komplizierter koronarer Herzkrankheit und hohem PAP eine deutliche Besserung der Symptome nach der Einnahme von ARNI auftrat und sich ihr Zustand der NYHA-Klasse III auf Klasse II verbesserte (
93
). In einem Fallbericht wurde beobachtet, dass ein Patient im zweiten Jahr nach der Herztransplantation eine reduzierte LVEF- und RVSP-Kapazität mit PH entwickelte. Nach der praktischen Anwendung von ARNI zeigte dieser Patient eine erhöhte Aktivitätsausdauer und eine verbesserte systolische LV-Funktion (LVEF von 29 % auf 41 %) bei einer Verringerung der PAH (RVSP von 65 % auf 50 %) (
94
). Sogar bei Patienten mit refraktärer HFrEF in Kombination mit PH hat ARNI eine überraschende Wirksamkeit gezeigt. Die stufenweise Erhöhung der ARNI-Dosis senkte den Füllungsdruck, ohne die normale Nierenfunktion zu beeinträchtigen. Unter hämodynamischer Unterstützung einer Senkung des rechtsatrialen Druck/PCWP-Verhältnisses zeigte sich in der Echokardiographie eine Verringerung des E/A-Verhältnisses und der linksatrialen Volumenmetrie (
67
).Patienten mit HF weisen häufig eine eingeschränkte Nierenfunktion auf, während Patienten mit chronischer Nierenerkrankung (CKD) oft einem hohen Risiko für kardiovaskuläre Ereignisse ausgesetzt sind (
95
). Im Vergleich zum RAS-Hemmer erhöhte ARNI die geschätzte glomeruläre Filtrationsrate (eGFR) signifikant und senkte NT-proBNP bei Patienten sowohl mit HF als auch mit CKD (
96
). In einer Realweltstudie mit Patienten in allen Stadien von CKD wurde eine niedrige Baseline-GFR von <30 ml/min/1,73 m2 als unabhängiger Prädiktor für schlechtere klinische Ergebnisse identifiziert. Die Daten zeigten, dass die Behandlung mit ARNI zu weniger kardiovaskulären Todesfällen oder Krankenhausaufenthalten wegen HF führte als die Behandlung mit der Standardtherapie ohne ARNI, und zwar sowohl bei Patienten mit GFR ≥ 30 ml/min/1,73 m2 als auch mit GFR < 30 ml/min/1,73 m2 ( 97
)
. Eine einjährige Behandlung mit ARNI verbesserte die systolische und diastolische Herzfunktion bei Patienten mit terminaler Niereninsuffizienz und HFrEF signifikant, erhöhte bei diesen Patienten jedoch weder das Hyperkaliämie- noch das Hypotonierisiko (
98
). Eine frühzeitige Verschlechterung der Nierenfunktion (WRF), definiert als >20%ige Abnahme der eGFR, trat bei Patienten mit ARNI-Therapie nach einem Monat auf. Nach drei Monaten erholte sich die Nierenfunktion dieser Patienten jedoch, und nach einem Jahr war eine Verbesserung der eGFR im Vergleich zum Ausgangswert zu verzeichnen. Darüber hinaus hatte die frühe WRF in den folgenden 650 Tagen keinen Einfluss auf die klinischen Ergebnisse (
99
).Durch Aktivierung der RAAS- und NP-Hemmung bewirkt ARNI eine stärkere Blutdrucksenkung als ARB allein (
100
). In den britischen Studien Heart and Renal Protection III (UK HARP III) und PARADIGM-HF wurde bei Patienten, die mit ARNI behandelt wurden, Hypotonie beobachtet (
101
,
102
). Das Auftreten von Hypotonie ist vorhersehbar, und nur eine signifikante symptomatische Hypotonie, die zu Präsynkopen, Synkopen oder anderen Organschäden führt, sollte eine Verringerung der ARNI-Dosis rechtfertigen (
103
). Obwohl Hyperkaliämie in der ARNI-Gruppe seltener auftrat als in der Enalapril-Gruppe, wird empfohlen, nach der ARNI-Gabe Kreatinin und Serumkalium zu überprüfen (
102
). Der Konsens deutet darauf hin, dass Angioödeme die primäre Nebenwirkung sind, die zum Absetzen des Arzneimittels führt (
104
), aber das Auftreten von Angioödemen ist selten, und zur weiteren Untersuchung sind weitere Studien erforderlich. Das Risiko einer Alzheimer-Erkrankung (AD) weckt zunehmend Aufmerksamkeit, da eine Hemmung von NEP den Abbau des Amyloid-beta-Proteins (Aβ) verringern kann, das mit der Progression von AD in Zusammenhang steht (
105
,
106
). Durch die Hemmung von NEP1 wurde Aβ in Drosophila sowohl für das Mittel- als auch für das Langzeitgedächtnis schädlich, während eine Überexpression von NEP1 die Gedächtnisdefizite behob (
107
). Die oben genannten Tiermodelle legen nahe, dass ARNI die kognitive Funktion beeinträchtigen kann; Nebenwirkungen im Zusammenhang mit Kognition, Gedächtnis und Demenz traten in der ARNI-Gruppe in PARADIGM-HF jedoch nicht häufiger auf (
108
). Es sind weitere Untersuchungen in klinischen Studien erforderlich, um festzustellen, ob ARNI einen Einfluss auf die Kognition bei Patienten mit HF und/oder CKD hat.7. Diagnosewerkzeuge und Überwachungsgeräte für PHDie transthorakale Echokardiographie ermöglicht die Messung der maximalen Trikuspidalinsuffizienzgeschwindigkeit und die Berechnung von PASP zur Beurteilung der RV-Funktion (
109
). Die systolische Exkursion der Trikuspidalannulebene (TAPSE), die aus dem RV-DTI abgeleitete systolische Geschwindigkeitswelle der trikuspidallateralen Annularebene (RV S') und die fraktionale Flächenänderung (RV FAC) sind empfohlene echokardiographische Parameter zur Beurteilung der systolischen RV-Funktion in klinischen Studien (
110
,
111
). Nach 12-monatiger Therapie mit ARNI in einem Realwelt-Register berichteten Correale M et al., dass die Verbesserungen von PASP und TAPSE proportional zu den Ausgangswerten und unabhängig von der LV-Funktion waren (
112
). Kürzlich zeigten sie außerdem, dass der RV S'-Ausgangswert ein unabhängiger Prädiktor der RV-Verbesserung ist. Die maximale Längsdehnung der freien RV-Wand (RV-FW-LS), ein genaueres und empfindlicheres Instrument zur Beurteilung der RV-Funktion, und die RV-Vierkammerdehnung (RV-4Ch-LS), ein Parameter, der die Analyse des interventrikulären Septums umfasst, wurden in dieser Studie ebenfalls verbessert (
85
) (
Tabelle 2
). Forfia et al. stellten fest, dass TAPSE das Überleben bei 47 Patienten mit PAH vorhersagte, nicht jedoch die Mortalität bei Patienten mit präkapillärer PH in Kombination mit RV-Dilatation (
113
). Eine Echokardiographie unter Verwendung eines multivariablen Modells auf Basis von 2D-Messungen ergab eine RV-Dyssynchronie bei Patienten mit einem mittleren PAP zwischen 20 und 25 mmHg, was darauf hindeutet, dass die RV-Deformation sogar bei leichter/kritischer PH beeinträchtigt sein kann (
114
). Die Kardio-MRT bietet Zugang zum dreidimensionalen strukturellen RV und wird als Goldstandard für die Beurteilung des enddiastolischen und systolischen RV-Volumens, der RV-Masse, der lokalen Ventrikelwandbewegung und des pulmonalarteriellen Blutflusses empfohlen (
115
). Die RV-Qualität hat sich als Vorhersagegröße für die PH-Prognose erwiesen, und sowohl ein niedrigerer Schlagvolumenindex als auch ein reduzierter Schlagvolumenindex während der Behandlung waren mit einer erhöhten Mortalität assoziiert (
116
). Tabelle 2
Tabelle 1. Auswirkungen von Sacubitril/Valsartan auf PH bei Patienten mit HFrEF und HFpEF. 5. Auswirkungen von Sacubitril/Valsartan auf PH mit rechtsventrikulärer DysfunktionEin erhöhter mittlerer PAP reicht nicht aus, um eine pulmonalvaskuläre Erkrankung zu definieren, da die Ursachen für PH unterschiedlich sein können, darunter erhöhtes Herzzeitvolumen, erhöhter pulmonaler Verschlussdruck und Hyperviskosität. Beim 6. Weltsymposium zu PH wurde zudem empfohlen, DPG von der Definition der Cpc-PH auszuschließen, da es nicht unbedingt ein schlechter Prognosefaktor ist (
76
). Daher bleibt es umstritten, ob DPG für die Prognose der LHD-PH wichtig ist, da die zugrunde liegenden Krankheiten, die eine LV-Dysfunktion verursachen, unterschiedlich sein können. Eine Beeinträchtigung der kontraktilen Funktion des rechten Ventrikels und eine erhöhte Nachlast infolge einer PAH können beide zu einer RV-Dysfunktion beitragen (
77
).Chronische Rechtsherzinsuffizienz (RHF) ist das Ergebnis einer langfristigen Erhöhung der RV-Nachlast, die die Kompensationsmechanismen des RV schließlich überfordert. Adrenalin stimuliert die kompensierenden Antriebsmechanismen, die die systolische Herzfunktion bei erhöhter RV-Nachlast aufrechterhalten, führt aber letztendlich zu einer Myokardfunktionsstörung, wenn es über einen längeren Zeitraum anhält (
33
). Darüber hinaus führt die anhaltende Erhöhung des adrenergen Tonus zu einer Herunterregulierung der myokardialen Betarezeptoren des RV und zur Erschöpfung der Noradrenalinreserven (
78
). Eine kürzlich durchgeführte nuklearbildgebende Studie an einer kleinen Gruppe von Patienten mit PAH legte nahe, dass diese Patienten möglicherweise eine erhebliche sympathische Funktionsstörung haben. Im Vergleich zur Kontrollgruppe zeigte die kardiale (
79
) Jod-Metaiodobenzylguanidin-Aufnahme eine verringerte LVEF in der PH-Gruppe. Herz-Mediastinum-Verhältnisse und Auswaschrate sind mit PVR, rechtem Vorhofdruck, systolischer Exkursion in der Trikuspidalebene, NT-proBNP und maximalem VO2 assoziiert ( 80
)
. In einem Kaninchenmodell mit systemischer RV-Nachlast, die durch ein Pulmonalarterienband induziert wurde, führten ventrikulär-ventrikuläre Interaktionen über die TGF-b1-, CTGF- und ET-1-Signalwege nicht nur zu RV-Hypertrophie, sondern auch zu sekundärer LV-Fibrose und RV-Apoptose. Eine Blockade des Ang-II-Rezeptors mit Losartan linderte jedoch diese interventrikuläre Wechselwirkung. Bemerkenswerterweise nahm die LV-CTGF-mRNA-Expression nach der Behandlung mit einem Pulmonalarterienband zu, und Losartan verringerte die durch das Pulmonalarterienband induzierte CTGF-mRNA-Expression (
81
). Da die pulmonale RAAS-Aktivität mit der Prognose bei Patienten mit iPAH korreliert, kann aus diesem Experiment die Hypothese abgeleitet werden, dass Losartan durch Blockierung profibrotischer Signale die RV-Hypertrophie umkehren und die LV-Belastung verringern kann. Es wurde auch festgestellt, dass Telmisartan die RV-Umgestaltung verbessert, möglicherweise durch Hemmung der MMP-2- und MMP-9-Aktivität (
82
). Borgdorff MA et al. entdeckten jedoch, dass Losartan in Kombination mit Eplerenon weder die systolische und diastolische RV-Funktion verbesserte noch Myokardfibrose und RV-Hypertrophie verhinderte (
83
). Der Grund für diesen Kontrast könnte der physiologische Unterschied zwischen LV und RV sein oder die Hemmung des RAAS als Folge der Blockade von AT1R auf das Lungengefäßsystem und nicht die direkte myokardiale Wirkung auf den RV. Doppler-Ultraschall und kardiopulmonale Belastungstests zeigten, dass Losartan PAP und den Durchmesser des rechten Vorhofs senkte und die Belastungstoleranz der Patienten verbesserte (
84
). Unterschiede in der Physiologie und der komplexen pathologischen Struktur des Herzens von Mensch und Nagetier könnten das Problem erklären. Um den Druck auf der rechten Seite des Herzens genau messen zu können, sind zuverlässigere Beweise aus invasiven Tests (Platzierung von Herzkathetern) erforderlich.Eine RV-Dysfunktion bedeutet ein Fortschreiten der Herzinsuffizienz und kann sogar zu einem schlechteren Prognosefaktor werden (
85
). Im Vergleich mit dem unabhängigen RV-Versagensmodell, das durch eine Bänderung des Lungenstamms induziert wurde, reduzierte ARNI den systolischen RV-Druck (RVSP), die RV-Hypertrophie sowie das enddiastolische und endsystolische RV-Volumen in der Gruppe mit PH signifikant. Dies deutet darauf hin, dass ARNI die RV-Umgestaltung möglicherweise nicht direkt beeinflusst, aber Vorteile für die rechte Herzhälfte bringt, indem es die pulmonalvaskuläre Funktion verbessert (
86
). Die transmurale Neuausrichtung von Kollagen und Myofasern durch RV-Hypertrophie wurde ebenfalls geschwächt, was darauf hindeutet, dass die Wirkung von ARNI auf die RV-Umgestaltung sich nicht nur in der Hämodynamik, sondern auch in den biomechanischen Eigenschaften des RV auf Gewebeebene manifestierte (
87
). ARNI allein kann PAP und RV-Umgestaltung durch eine Erhöhung der endogenen NP verringern. Clements RT et al. behandelten das durch SU5146 und Hypoxie induzierte PH-Rattenmodell sechs Wochen lang mit ARNI und stellten einen Rückgang des RV-Drucks und der Fibrose fest, begleitet von einem Anstieg der pulmonalen ANP-, BNP- und cGMP-Spiegel (
88
). Bosentan, ein spezifischer und kompetitiver dualer Endothelin-Rezeptorblocker mit niedrigem Molekulargewicht, ist das erste neuartige orale Medikament, das zur Behandlung von PAH zugelassen wurde. Bosentan wirkt jedoch in erster Linie über die Erweiterung der Lungengefäße, ohne direkt eine RHF zu verhindern. Im Monocrotalin-induzierten Rattenmodell mit schwerer PH verstärkte ARNI die Wirkung von Bosentan auf die Verringerung von PVR, RV-Hypertrophie und Fibrose. Gleichzeitig bestätigten kultivierte menschliche pulmonalarterielle glatte Muskelzellen von iPAH-Patienten die antiproliferative Wirkung von ARNI (
89
). ARNI könnte also eine synergistische Wirkung auf traditionelle Medikamente zur Behandlung von PH haben. Der Verlust des NO-Signalwegs führt bei PH-Patienten typischerweise zu einer endothelialen Dysfunktion, gefolgt von einer kompensatorischen Vasodilatation, die durch den natriuretischen Peptid-Clearance-Rezeptor (NPR-C) vermittelt wird. Die Aktivierung des NPR-C-Signalwegs kann antiproliferative Effekte aufweisen, während eine durch Hypoxie induzierte Herunterregulierung der NPR-C-Expression zu einer Umgestaltung der Lungengefäße und erhöhtem PAP führen kann (
90
).Ein weiterer Mechanismus in der Pathogenese von Lungengefäßerkrankungen ist die entzündliche Infiltration, bei der es zur Ansammlung von extrazellulären Matrixproteinen wie Fibronektin kommt (
91
). Bei Ratten, die mit Monocrotalin oder Hypoxie behandelt wurden, erhöhte ARNI nicht nur die ANP- und CNP-Spiegel im zirkulierenden Blut und Lungengewebe, sondern zeigte auch die gleiche Tendenz bei der Expression von NPR-A, C und cGMP. Die zirkulierenden IL-1β-, IL-6- und TNF-α-Spiegel, die einer ARNI-Intervention unterzogen wurden, waren in beiden Tiermodellen reduziert, und die entzündungshemmende Wirkung könnte mit dem ANP/NPR-A/cGMP-Signalweg zusammenhängen (
92
).6. Wirkungen und Nebenwirkungen von Sacubitril/Valsartan bei PH bei fortgeschrittener HF und chronischer NierenerkrankungLangfristiger Druck im linken Vorhof führt bei Patienten mit fortgeschrittener HFrEF zu schwerer PH, was sie für eine Herztransplantation disqualifizieren könnte. Während konventionelle Behandlungen wie Diurese, Vasodilatationstherapie und mechanische Unterstützung keine erkennbare Wirksamkeit zeigten, führte experimentelles ARNI zu besseren Ergebnissen als erwartet. Nach 24-stündiger ARNI-Gabe waren PASP und PVR signifikant reduziert, sodass vier Patienten in realen Fällen wieder für eine Herztransplantation geeignet waren, ohne dass postoperativer RHF oder Hypotonie eine vaskuläre Kompressionsunterstützung erforderlich machte (
17
).Zusätzlich zur HFrEF entwickeln erwachsene Patienten mit angeborenen Herzfehlern eine subpulmonalarterielle ventrikuläre Dysfunktion und PH. Lluri G et al. berichteten, dass bei vier Patienten mit Zyanose, komplizierter koronarer Herzkrankheit und hohem PAP eine deutliche Besserung der Symptome nach der Einnahme von ARNI auftrat und sich ihr Zustand der NYHA-Klasse III auf Klasse II verbesserte (
93
). In einem Fallbericht wurde beobachtet, dass ein Patient im zweiten Jahr nach der Herztransplantation eine reduzierte LVEF- und RVSP-Kapazität mit PH entwickelte. Nach der praktischen Anwendung von ARNI zeigte dieser Patient eine erhöhte Aktivitätsausdauer und eine verbesserte systolische LV-Funktion (LVEF von 29 % auf 41 %) bei einer Verringerung der PAH (RVSP von 65 % auf 50 %) (
94
). Sogar bei Patienten mit refraktärer HFrEF in Kombination mit PH hat ARNI eine überraschende Wirksamkeit gezeigt. Die stufenweise Erhöhung der ARNI-Dosis senkte den Füllungsdruck, ohne die normale Nierenfunktion zu beeinträchtigen. Unter hämodynamischer Unterstützung einer Senkung des rechtsatrialen Druck/PCWP-Verhältnisses zeigte sich in der Echokardiographie eine Verringerung des E/A-Verhältnisses und der linksatrialen Volumenmetrie (
67
).Patienten mit HF weisen häufig eine eingeschränkte Nierenfunktion auf, während Patienten mit chronischer Nierenerkrankung (CKD) oft einem hohen Risiko für kardiovaskuläre Ereignisse ausgesetzt sind (
95
). Im Vergleich zum RAS-Hemmer erhöhte ARNI die geschätzte glomeruläre Filtrationsrate (eGFR) signifikant und senkte NT-proBNP bei Patienten sowohl mit HF als auch mit CKD (
96
). In einer Realweltstudie mit Patienten in allen Stadien von CKD wurde eine niedrige Baseline-GFR von <30 ml/min/1,73 m2 als unabhängiger Prädiktor für schlechtere klinische Ergebnisse identifiziert. Die Daten zeigten, dass die Behandlung mit ARNI zu weniger kardiovaskulären Todesfällen oder Krankenhausaufenthalten wegen HF führte als die Behandlung mit der Standardtherapie ohne ARNI, und zwar sowohl bei Patienten mit GFR ≥ 30 ml/min/1,73 m2 als auch mit GFR < 30 ml/min/1,73 m2 ( 97
)
. Eine einjährige Behandlung mit ARNI verbesserte die systolische und diastolische Herzfunktion bei Patienten mit terminaler Niereninsuffizienz und HFrEF signifikant, erhöhte bei diesen Patienten jedoch weder das Hyperkaliämie- noch das Hypotonierisiko (
98
). Eine frühzeitige Verschlechterung der Nierenfunktion (WRF), definiert als >20%ige Abnahme der eGFR, trat bei Patienten mit ARNI-Therapie nach einem Monat auf. Nach drei Monaten erholte sich die Nierenfunktion dieser Patienten jedoch, und nach einem Jahr war eine Verbesserung der eGFR im Vergleich zum Ausgangswert zu verzeichnen. Darüber hinaus hatte die frühe WRF in den folgenden 650 Tagen keinen Einfluss auf die klinischen Ergebnisse (
99
).Durch Aktivierung der RAAS- und NP-Hemmung bewirkt ARNI eine stärkere Blutdrucksenkung als ARB allein (
100
). In den britischen Studien Heart and Renal Protection III (UK HARP III) und PARADIGM-HF wurde bei Patienten, die mit ARNI behandelt wurden, Hypotonie beobachtet (
101
,
102
). Das Auftreten von Hypotonie ist vorhersehbar, und nur eine signifikante symptomatische Hypotonie, die zu Präsynkopen, Synkopen oder anderen Organschäden führt, sollte eine Verringerung der ARNI-Dosis rechtfertigen (
103
). Obwohl Hyperkaliämie in der ARNI-Gruppe seltener auftrat als in der Enalapril-Gruppe, wird empfohlen, nach der ARNI-Gabe Kreatinin und Serumkalium zu überprüfen (
102
). Der Konsens deutet darauf hin, dass Angioödeme die primäre Nebenwirkung sind, die zum Absetzen des Arzneimittels führt (
104
), aber das Auftreten von Angioödemen ist selten, und zur weiteren Untersuchung sind weitere Studien erforderlich. Das Risiko einer Alzheimer-Erkrankung (AD) weckt zunehmend Aufmerksamkeit, da eine Hemmung von NEP den Abbau des Amyloid-beta-Proteins (Aβ) verringern kann, das mit der Progression von AD in Zusammenhang steht (
105
,
106
). Durch die Hemmung von NEP1 wurde Aβ in Drosophila sowohl für das Mittel- als auch für das Langzeitgedächtnis schädlich, während eine Überexpression von NEP1 die Gedächtnisdefizite behob (
107
). Die oben genannten Tiermodelle legen nahe, dass ARNI die kognitive Funktion beeinträchtigen kann; Nebenwirkungen im Zusammenhang mit Kognition, Gedächtnis und Demenz traten in der ARNI-Gruppe in PARADIGM-HF jedoch nicht häufiger auf (
108
). Es sind weitere Untersuchungen in klinischen Studien erforderlich, um festzustellen, ob ARNI einen Einfluss auf die Kognition bei Patienten mit HF und/oder CKD hat.7. Diagnosewerkzeuge und Überwachungsgeräte für PHDie transthorakale Echokardiographie ermöglicht die Messung der maximalen Trikuspidalinsuffizienzgeschwindigkeit und die Berechnung von PASP zur Beurteilung der RV-Funktion (
109
). Die systolische Exkursion der Trikuspidalannulebene (TAPSE), die aus dem RV-DTI abgeleitete systolische Geschwindigkeitswelle der trikuspidallateralen Annularebene (RV S') und die fraktionale Flächenänderung (RV FAC) sind empfohlene echokardiographische Parameter zur Beurteilung der systolischen RV-Funktion in klinischen Studien (
110
,
111
). Nach 12-monatiger Therapie mit ARNI in einem Realwelt-Register berichteten Correale M et al., dass die Verbesserungen von PASP und TAPSE proportional zu den Ausgangswerten und unabhängig von der LV-Funktion waren (
112
). Kürzlich zeigten sie außerdem, dass der RV S'-Ausgangswert ein unabhängiger Prädiktor der RV-Verbesserung ist. Die maximale Längsdehnung der freien RV-Wand (RV-FW-LS), ein genaueres und empfindlicheres Instrument zur Beurteilung der RV-Funktion, und die RV-Vierkammerdehnung (RV-4Ch-LS), ein Parameter, der die Analyse des interventrikulären Septums umfasst, wurden in dieser Studie ebenfalls verbessert (
85
) (
Tabelle 2
). Forfia et al. stellten fest, dass TAPSE das Überleben bei 47 Patienten mit PAH vorhersagte, nicht jedoch die Mortalität bei Patienten mit präkapillärer PH in Kombination mit RV-Dilatation (
113
). Eine Echokardiographie unter Verwendung eines multivariablen Modells auf Basis von 2D-Messungen ergab eine RV-Dyssynchronie bei Patienten mit einem mittleren PAP zwischen 20 und 25 mmHg, was darauf hindeutet, dass die RV-Deformation sogar bei leichter/kritischer PH beeinträchtigt sein kann (
114
). Die Kardio-MRT bietet Zugang zum dreidimensionalen strukturellen RV und wird als Goldstandard für die Beurteilung des enddiastolischen und systolischen RV-Volumens, der RV-Masse, der lokalen Ventrikelwandbewegung und des pulmonalarteriellen Blutflusses empfohlen (
115
). Die RV-Qualität hat sich als Vorhersagegröße für die PH-Prognose erwiesen, und sowohl ein niedrigerer Schlagvolumenindex als auch ein reduzierter Schlagvolumenindex während der Behandlung waren mit einer erhöhten Mortalität assoziiert (
116
). Tabelle 2
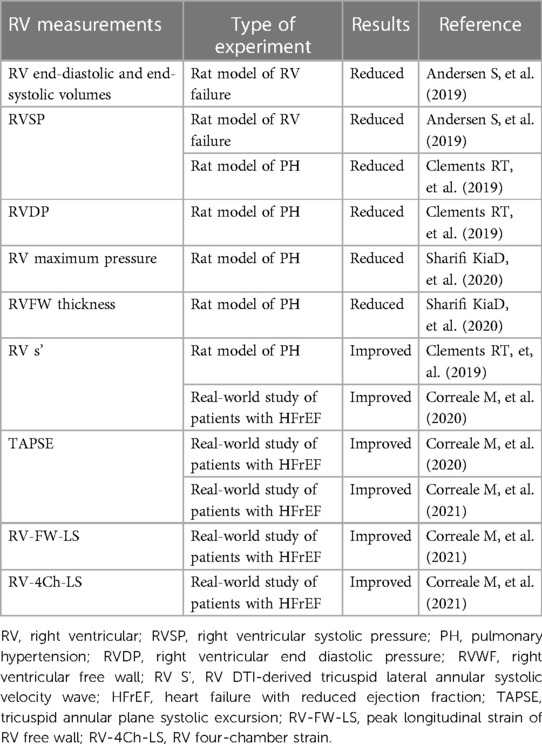 Tabelle 2. Wirkungen von Sacubitril/Valsartan bei Patienten mit RV-Dysfunktion. Patienten mit systolischem Herzinsuffizienz im Endstadium sind aufgrund der irreversiblen PH keine Kandidaten für eine Herztransplantation. Diese kann jedoch nach 6 Monaten Implantation eines linksventrikulären Dauerstromunterstützungssystems (cfLVAD) rückgängig gemacht werden (
117
,
118
). Das CfLVAD senkt PAP und PVR, indem es den linken Ventrikel entlastet und den enddiastolischen Druck und das Volumen des linken Ventrikels senkt. Obwohl sich TPG und PVR nach der Implantation eines cfLVAD wieder normalisieren, können histologische Veränderungen im pulmonalen Gefäßbett irreversibel sein. Unterschiede in den DPG-Gradienten zwischen eingestellten und maximalen Geschwindigkeiten > 3 mmHg bei cfLVAD-Basiswerten können auf eine anhaltende kapilläre PH hinweisen, die positiv mit einer erhöhten HF-Krankenhausaufenthaltsrate und Mortalität verbunden ist (
119
).CardioMEMS™ ist ein implantierbares Gerät, das in die Pulmonalarterie implantiert wird, um bei Patienten mit HF den Herzfüllungsdruck zu messen, unabhängig vom LVEF-Wert, der tendenziell mehr als zwei Wochen vor einer symptomatischen klinischen Stauung ansteigt (
120
,
121
). Die pulmonaldruckgesteuerte Therapie stellt eine neuartige Strategie dar, um das Rezidivrisiko bei Patienten mit chronischem HF zu senken, indem sie mithilfe von CardioMEMS™ eine engmaschigere, nicht-invasive hämodynamische Überwachung im Krankenhaus ermöglicht. Nach der Implantation von CardioMEMS™ bei einem 53-jährigen Patienten mit idiopathischer dilatativer Kardiomyopathie erkannte das System eine Abnahme des PAP, begleitet von einer Zunahme der LV-Ejektionsfraktion und einer Abnahme von NT-pro-BNP. Dieser Fall ist der erste gemeldete Fall, in dem ARNI, wie durch Telemetriedaten festgestellt, den PAP und die Herzfunktion bei einem Patienten mit HFrEF verbessert hat (
122
,
123
). Bei HFrEF-Patienten mit zuvor implantierten CardioMEMS™-Sensoren zeigte der Übergang von ACEI/ARB zu ARNI eine schnelle Abnahme des PAP (
69
). Durch die Überwachung des PAP konnte das CardioMEMS™-System Flüssigkeitsaufnahme und -abgabe ausgleichen, eine personalisierte Medikamenteneinnahme erleichtern und die Zahl der Krankenhausaufenthalte senken. Nach der PAP-Anpassung durch CardioMEMS™ zur Vermeidung einer frühen Verstopfung wurde ARNI eingesetzt, um die Verwendung zyklischer Diuretika, das Risiko einer neurohormonellen Aktivierung und Elektrolytstörungen zu verringern (
79
).8. SchlussfolgerungenErhöhte Füllungsdrücke im linken Herzen führen zu einer Beeinträchtigung der pulmonalvenösen Refluxobstruktion, die eine Hauptursache für PH-LHD ist und letztendlich zu einer vollständigen Herzinsuffizienz führt (
Abbildung 2
). ARNI ist aufgrund seiner dualen Hemmung der RAAS- und NPs-Systeme zu einem Forschungsschwerpunkt im kardiovaskulären Bereich geworden. Zusätzlich zu experimentellen Daten deuten Beweise aus klinischen Studien darauf hin, dass ARNI bei der Verzögerung des Fortschreitens von PH bei Patienten mit HFrEF, HFpEF oder RV-Dysfunktion, einschließlich derjenigen, die auf eine Herztransplantation warten, wirksam sein kann. Obwohl keine schwerwiegenden Nebenwirkungen beobachtet wurden, sind für die zukünftige Wirksamkeit und Sicherheit von ARNI bei HF, das mit PH kompliziert ist, weitere groß angelegte und multizentrische klinische Studien erforderlich. Figur 2
Tabelle 2. Wirkungen von Sacubitril/Valsartan bei Patienten mit RV-Dysfunktion. Patienten mit systolischem Herzinsuffizienz im Endstadium sind aufgrund der irreversiblen PH keine Kandidaten für eine Herztransplantation. Diese kann jedoch nach 6 Monaten Implantation eines linksventrikulären Dauerstromunterstützungssystems (cfLVAD) rückgängig gemacht werden (
117
,
118
). Das CfLVAD senkt PAP und PVR, indem es den linken Ventrikel entlastet und den enddiastolischen Druck und das Volumen des linken Ventrikels senkt. Obwohl sich TPG und PVR nach der Implantation eines cfLVAD wieder normalisieren, können histologische Veränderungen im pulmonalen Gefäßbett irreversibel sein. Unterschiede in den DPG-Gradienten zwischen eingestellten und maximalen Geschwindigkeiten > 3 mmHg bei cfLVAD-Basiswerten können auf eine anhaltende kapilläre PH hinweisen, die positiv mit einer erhöhten HF-Krankenhausaufenthaltsrate und Mortalität verbunden ist (
119
).CardioMEMS™ ist ein implantierbares Gerät, das in die Pulmonalarterie implantiert wird, um bei Patienten mit HF den Herzfüllungsdruck zu messen, unabhängig vom LVEF-Wert, der tendenziell mehr als zwei Wochen vor einer symptomatischen klinischen Stauung ansteigt (
120
,
121
). Die pulmonaldruckgesteuerte Therapie stellt eine neuartige Strategie dar, um das Rezidivrisiko bei Patienten mit chronischem HF zu senken, indem sie mithilfe von CardioMEMS™ eine engmaschigere, nicht-invasive hämodynamische Überwachung im Krankenhaus ermöglicht. Nach der Implantation von CardioMEMS™ bei einem 53-jährigen Patienten mit idiopathischer dilatativer Kardiomyopathie erkannte das System eine Abnahme des PAP, begleitet von einer Zunahme der LV-Ejektionsfraktion und einer Abnahme von NT-pro-BNP. Dieser Fall ist der erste gemeldete Fall, in dem ARNI, wie durch Telemetriedaten festgestellt, den PAP und die Herzfunktion bei einem Patienten mit HFrEF verbessert hat (
122
,
123
). Bei HFrEF-Patienten mit zuvor implantierten CardioMEMS™-Sensoren zeigte der Übergang von ACEI/ARB zu ARNI eine schnelle Abnahme des PAP (
69
). Durch die Überwachung des PAP konnte das CardioMEMS™-System Flüssigkeitsaufnahme und -abgabe ausgleichen, eine personalisierte Medikamenteneinnahme erleichtern und die Zahl der Krankenhausaufenthalte senken. Nach der PAP-Anpassung durch CardioMEMS™ zur Vermeidung einer frühen Verstopfung wurde ARNI eingesetzt, um die Verwendung zyklischer Diuretika, das Risiko einer neurohormonellen Aktivierung und Elektrolytstörungen zu verringern (
79
).8. SchlussfolgerungenErhöhte Füllungsdrücke im linken Herzen führen zu einer Beeinträchtigung der pulmonalvenösen Refluxobstruktion, die eine Hauptursache für PH-LHD ist und letztendlich zu einer vollständigen Herzinsuffizienz führt (
Abbildung 2
). ARNI ist aufgrund seiner dualen Hemmung der RAAS- und NPs-Systeme zu einem Forschungsschwerpunkt im kardiovaskulären Bereich geworden. Zusätzlich zu experimentellen Daten deuten Beweise aus klinischen Studien darauf hin, dass ARNI bei der Verzögerung des Fortschreitens von PH bei Patienten mit HFrEF, HFpEF oder RV-Dysfunktion, einschließlich derjenigen, die auf eine Herztransplantation warten, wirksam sein kann. Obwohl keine schwerwiegenden Nebenwirkungen beobachtet wurden, sind für die zukünftige Wirksamkeit und Sicherheit von ARNI bei HF, das mit PH kompliziert ist, weitere groß angelegte und multizentrische klinische Studien erforderlich. Figur 2
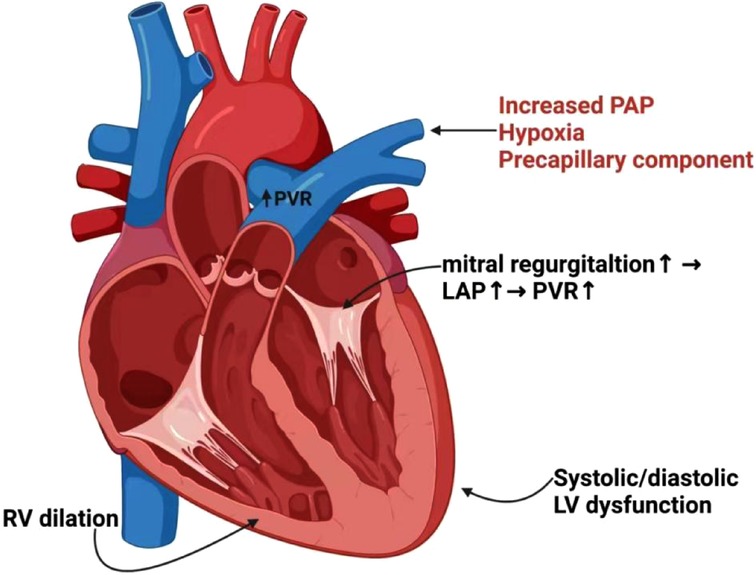 Abbildung 2. Interaktion und Pathogenese von PH bei LV/RV-Herzinsuffizienz. Hypoxie, präkapilläre Komponente und erhöhter PAP können eine pulmonalarterielle Vasokonstriktion auslösen, was zu erhöhtem PVR und reduzierter PA-Compliance führt. Eine funktionelle Mitralklappeninsuffizienz führt außerdem zu erhöhten LAP- und PVR-Werten. Erhöhte Füllungsdrücke verursachen PH, die eine Folge einer systolischen oder diastolischen LV-Dysfunktion ist. Die anhaltenden Erhöhungen des pulmonalen Drucks und PVR führen zu einer Dilatation und maladaptiven Umgestaltung der rechten Herzkammern und schließlich zu einem RV-Versagen. PH, pulmonale Hypertonie; PAP, pulmonalarterieller Druck; PVR, pulmonalvaskulärer Widerstand; PA, Pulmonalarterie; LAP, linker Vorhofdruck; LV, linker Ventrikel; RV, rechter Ventrikel.
Abbildung 2. Interaktion und Pathogenese von PH bei LV/RV-Herzinsuffizienz. Hypoxie, präkapilläre Komponente und erhöhter PAP können eine pulmonalarterielle Vasokonstriktion auslösen, was zu erhöhtem PVR und reduzierter PA-Compliance führt. Eine funktionelle Mitralklappeninsuffizienz führt außerdem zu erhöhten LAP- und PVR-Werten. Erhöhte Füllungsdrücke verursachen PH, die eine Folge einer systolischen oder diastolischen LV-Dysfunktion ist. Die anhaltenden Erhöhungen des pulmonalen Drucks und PVR führen zu einer Dilatation und maladaptiven Umgestaltung der rechten Herzkammern und schließlich zu einem RV-Versagen. PH, pulmonale Hypertonie; PAP, pulmonalarterieller Druck; PVR, pulmonalvaskulärer Widerstand; PA, Pulmonalarterie; LAP, linker Vorhofdruck; LV, linker Ventrikel; RV, rechter Ventrikel.




OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Bitte Anmelden oder Registrieren um der Konversation beizutreten.
