- Beiträge: 1755
Sidebar
- Forum
- PH-Forum
- Forschung und Wissen
- Oxygeniertes Hämoglobin als prognostischer Marker bei Systemischer Sklerose
Oxygeniertes Hämoglobin als prognostischer Marker bei Systemischer Sklerose
02 Feb 2023 17:10 #1708
von danny
OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Oxygeniertes Hämoglobin als prognostischer Marker bei Systemischer Sklerose wurde erstellt von danny
www.nature.com/articles/s41598-023-28608-xOxygeniertes Hämoglobin als prognostischer Marker bei Patienten mit systemischer Sklerose, die auf pulmonale Hypertonie untersucht wurden AbstraktOxygeniertes Hämoglobin (OxyHem) im arteriellen Blut kann die Schwere der Erkrankung bei Patienten mit systemischer Sklerose (SSc) widerspiegeln. Ziel dieser Studie war es, den prädiktiven Wert von OxyHem bei SSc-Patienten zu analysieren, die auf pulmonale Hypertonie (PH) gescreent wurden. OxyHem (g/dl) wurde gemessen, indem die Hämoglobinkonzentration mit der fraktionierten Sauerstoffsättigung in arterialisiertem Kapillarblut multipliziert wurde. Die prognostische Aussagekraft wurde mit bekannten prognostischen Parametern in SSc unter Verwendung von uni- und multivariablen Analysen verglichen. Insgesamt wurden 280 SSc-Patienten gescreent, 267 wurden in die Analyse eingeschlossen. Bei 126 Patienten wurden keine Anzeichen einer Lungengefäßerkrankung gefunden, während 141 Patienten einen mittleren pulmonalarteriellen Druck von ≥ 21 mmHg aufwiesen. Bei 70 Patienten wurde eine interstitielle Lungenerkrankung (ILD) festgestellt. Niedriger OxyHem ≤ 12.P = 0,046). In der multivariablen Analyse waren das Vorhandensein einer ILD, ein Alter ≥ 60 Jahre und eine Diffusionskapazität für Kohlenmonoxid (DLCO) ≤ 65 % negativ mit dem Überleben assoziiert. Die Kombination aus niedrigem DLCO und niedrigem OxyHem zu Studienbeginn konnte den PH zu Studienbeginn vorhersagen (Sensitivität 76,1 %). In dieser Studie wurde erstmals OxyHem ≤ 12,5 g/dl als prognostischer Prädiktor bei SSc-Patienten nachgewiesen. Weitere Studien sind erforderlich, um diese Ergebnisse zu bestätigen.EinführungSystemische Sklerose (SSc) ist eine seltene Autoimmunerkrankung, die durch diffuse Fibrose, Entzündung und Vaskulopathie gekennzeichnet ist und nach wie vor eine der komplexesten und tödlichsten Erkrankungen unter den Bindegewebserkrankungen ist
1
. Die Schwere der Organbeteiligung sagt das Ergebnis bei SSc-Patienten voraus
2
,
3
.Pulmonale Komplikationen, hauptsächlich pulmonale arterielle Hypertonie (PAH) und interstitielle Lungenerkrankung (ILD), bleiben die häufigste Todesursache bei SSc-Patienten
1
. Folglich sind das Screening und die frühzeitige Diagnose sowohl der Krankheit als auch der Organbeteiligung entscheidend für die Prognose.Die Etablierung von Risikostratifizierungsmethoden ist unerlässlich, um das Überleben durch schnelle medizinische und therapeutische Interventionen zu verbessern. Die Mehrheit der verfügbaren Bewertungsmodelle muss noch validiert werden
1
. Frühere Studien haben bereits über die prognostische Bedeutung einer beeinträchtigten Sauerstoffsättigung (SaO 2 ) während des Trainings für das Überleben und den Krankheitsverlauf bei Patienten mit SSc-ILD berichtet
4
,
5
. SaO 2 kann sowohl durch kardiale als auch pulmonale Komorbiditäten beeinflusst werden. Darüber hinaus wurde gezeigt, dass Anämie ein prognostischer Prädiktor für das Überleben bei Patienten mit SSc
6
ist . Eine Kombination dieser Parameter könnte daher für die Risikostratifizierung und Prognose von Vorteil sein.Trudzinskiet al. zeigten, dass neben der Leukozytenzahl auch oxygeniertes Hämoglobin (OxyHem), das Produkt aus Hämoglobinkonzentration und fraktionierter Sauerstoffsättigung (SaO 2 ) in der arteriellen kapillaren Blutgasanalyse, ein geeigneter und einfach abzuschätzender neuartiger Biomarker für die Prognose von Patienten mit Chronisch obstruktive Lungenerkrankung (COPD)
7
. OxyHem, gemessen bei Patienten mit stabiler COPD, aber auch während akuter COPD-Exazerbationen, war unabhängig mit einer höheren Sterblichkeit bei diesen Patienten verbunden
8
. OxyHem im arteriellen Blut könnte auch ein neuer Biomarker für die Prognose bei Patienten mit SSc sein.Daher war das Ziel dieser Studie, den prognostischen Wert von OxyHem bei SSc-Patienten zu analysieren, die zum Screening auf pulmonale Hypertonie (PH) überwiesen wurden. Darüber hinaus untersuchte die Studie den Zusammenhang von OxyHem mit der Entwicklung von Lungengefäßerkrankungen (PVD) bei diesen Patienten.ErgebnisseBaseline klinische und demografische MerkmaleInsgesamt 280 Patienten mit SSc wurden auf pulmonale Hypertonie untersucht. Von dieser Kohorte erfüllten 13 Patienten die Ausschlusskriterien, was zu einer endgültigen Studiengruppe von 267 Patienten führte (Abb.
1
, Tabelle
1
). Das Durchschnittsalter der Patienten betrug 59,8 ± 13,4 Jahre, 82 % waren weiblich, 73,8 % hatten eine begrenzte kutane SSc (lcSSc) und 26,2 % eine diffuse kutane SSc (dcSSc). Die mittlere Dauer der SSc zu Studienbeginn betrug 9,0 ± 9,3 Jahre. Von diesen hatten 70 eine signifikante ILD (26,2 %) und 141 (52,8 %) einen mittleren pulmonalarteriellen Druck (mPAP) ≥ 21 mmHg (Abb.
1
), während 126 keine Anzeichen einer PH aufwiesen (41,6 %). Von den 141 Patienten mit PH stellten sich 19 mit PH aufgrund einer Linksherzerkrankung vor (Abb.
1
). Patienten mit PAH erhielten zielgerichtete PAH-Medikamente gemäß den aktuellen Leitlinien
9
. Von 267 Patienten gehörten 46,4 % der Funktionsklasse der Weltgesundheitsorganisation (WHO-FC) II, 30,3 % der WHO-FC III und 2,6 % der WHO-FC IV an. Die mittlere 6-Minuten-Gehstrecke (6MWD) betrug 427,7 ± 102,5 m. Komorbiditäten wurden bei 166 Patienten identifiziert: 101 (37,8 %) litten an arterieller Hypertonie, 58 (21,7 %) hatten eine koronare Herzkrankheit, einer (0,4 %) berichtete über eine Magen-Antralgefäß-Ektasie, drei (1 %) hatten in der Vorgeschichte ein Lymphom und 41 (15,4 %) waren fettleibig und hatten einen Body-Mass-Index (BMI) > 30 kg/m 2 .Abbildung 1
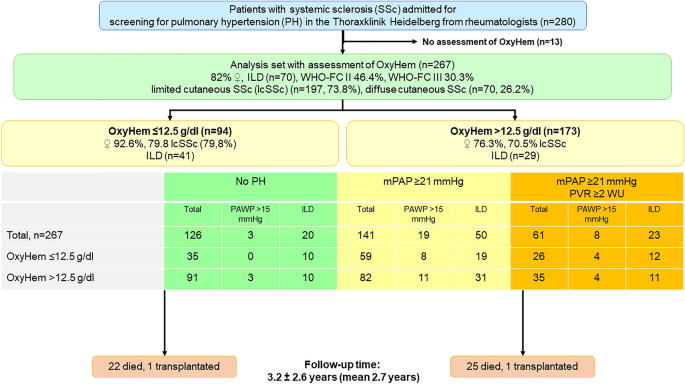 Flussdiagramm studieren. Das Flussdiagramm der Studienkohorte gibt Gründe für den Ausschluss aus dem Analyseset, die Verteilung der Patienten nach OxyHem und nach hämodynamischen Kriterien an.
Tabelle 1 Klinische Charakteristika der Studienkohorte.
Klinische Parameter, die Patienten mit niedrigem OxyHem charakterisierenDer Median von OxyHem in dieser Kohorte betrug 12,89 g/dl (Interquartilsabstand: 151,
Flussdiagramm studieren. Das Flussdiagramm der Studienkohorte gibt Gründe für den Ausschluss aus dem Analyseset, die Verteilung der Patienten nach OxyHem und nach hämodynamischen Kriterien an.
Tabelle 1 Klinische Charakteristika der Studienkohorte.
Klinische Parameter, die Patienten mit niedrigem OxyHem charakterisierenDer Median von OxyHem in dieser Kohorte betrug 12,89 g/dl (Interquartilsabstand: 151, . Receiver Operating Characteristic (ROC)-Analysen für OxyHem entsprachen dem Grenzwert aus Literatur
7
von 12,5 g/dl (ROC-Fläche unter der Kurve P = 0,004). Insgesamt hatten 94 SSc-Patienten OxyHem ≤ 12,5 g/dl und 173 SSc-Patienten OxyHem-Werte über 12,5 g/dl (Tabelle
2
). Im Vergleich zu Patienten mit OxyHem > 12,5 g/dl waren Patienten mit niedrigem OxyHem hauptsächlich weiblich (n = 87, 92,6 % vs. n = 132, 76,3 %, p = 0,001), hatten überwiegend lcSSc (n = 75, 79,8 % vs n = 122, 70,5 %, P = 0,011), ein stärker beeinträchtigter Eisenstoffwechsel in Bezug auf niedrigere Ferritinwerte (75,3 ± 83,6 vs. 126,7 ± 150,6 µg/l, P = 0,004) im Normalbereich, mittleres korpuskuläres Erythrozytenvolumen (MCV) (88,1 ± 8,7 vs. 90,3 ± 5,2 fl, P = 0,027) und mittleres korpuskuläres Hämoglobin in Erythrozyten (29,1 ± 3,0 vs. 30,1 ± 2,4 pg, P = 0,006) . ). Darüber hinaus waren sie klinisch eingeschränkter in Bezug auf WHO-FC ( P = 0,001), kürzere 6MGT (408,6 ± 101,3 vs. 437,8 ± 102,0 m, P = 0,036) und größere hämodynamische Beeinträchtigung mit einem höheren pulmonalen Gefäßwiderstand (PVR) ( 3,2 ± 2,6 vs. 2,4 ± 1,9 Wood Units (WU), P = 0,018) und mPAP (25,6 ± 11,7 vs. 21,6 ± 9,3 mmHg, P = 0,005) (Tabelle
2
). Es gab keinen signifikanten Unterschied im N-terminalen natriuretischen Pro-Gehirn-Peptid (NTproBNP) zwischen den beiden Gruppen. Von 94 Patienten mit OxyHem ≤ 12,5 g/dl litten 29 an ILD (23,7 %). Bei 59 Patienten mit niedrigem OxyHem lag der mPAP bei ≥ 21 mmHg (Abb.
1
). Eine begleitende ILD wurde bei 70 Patienten diagnostiziert, von denen 50 einen mPAP ≥ 21 mmHg aufwiesen. Bei 22 Patienten wurde eine Erhöhung des pulmonalarteriellen Keildrucks (PAWP) > 15 mmHg festgestellt, 19 wiesen einen mPAP ≥ 21 mmHg auf (Abb.
1
). Sechs Patienten hatten eine PH aufgrund einer Erkrankung des linken Herzens und der Lunge. Die Parameter des Lungenfunktionstests (PFT) waren bei Patienten mit niedrigerem OxyHem signifikant stärker beeinträchtigt, einschließlich der maximalen Vitalkapazität (VCmax), des forcierten exspiratorischen Volumens in einer Sekunde (FEV 1) und Gesamtlungenkapazität (TLC). In der Laboranalyse war das C-reaktive Protein (CRP) in der niedrigen OxyHem-Gruppe höher ( p = 0,020) und diese Patienten hatten signifikant niedrigere Hämoglobinwerte (Hb) ( p < 0,0001). Es gab keinen Unterschied in der Nierenfunktion zwischen den beiden Gruppen (Tabelle
2
).Tabelle 2 Klinische Merkmale der OxyHem-Untergruppen.
Überleben bei SSc-PatientenInnerhalb des Beobachtungszeitraums von 3,2 ± 2,6 (Median 2,7; Interquartilsabstand 3,5) Jahren starben 47 Patienten (17,6 %): 22 an PH (46,8 %), 4 an PH und/oder ILD (8,5 %), 3 an ILD (6,4 %), 7 aufgrund von Krebs (14,9 %), eine aufgrund einer Lungensepsis (2,1 %) und 3 aufgrund einer Linksherzerkrankung (6,4 %). Zwei Patienten wurden aufgrund von PH und ILD einer Lungentransplantation unterzogen. In sieben Fällen blieb die Todesursache unbekannt (14,9 %). Das mittlere geschätzte Gesamtüberleben betrug 7,7 ± 0,3 Standardfehler der mittleren Jahre (95 % Konfidenzintervall 7,1 bis 8,2) vom Ausgangswert. Das Überleben war bei männlichen und weiblichen Patienten ähnlich ( p = 0,624) und zwischen Patienten mit dcSSc und lcSSc ( p = 0,694).In der univariablen Kaplan-Meier-Analyse waren OxyHem ≤ 12,5 g/dl ( P = 0,046), Alter zu Studienbeginn ≥ 60 Jahre ( P = 0,002), das Vorhandensein von ILD ( P < 0,0001), hoher PVR ≥ 2 WU ( P = 0,002) und ein niedriger DLCO von ≤ 65 % des Sollwerts ( P < 0,001) waren signifikant mit einem schlechteren Überleben verbunden (Tabelle
3
). Die Anzahl der weißen Blutkörperchen (WBC) ≥ 10.000/ml wurde zusammen mit OxyHem in der ursprünglich beschriebenen COPD-Kohorte analysiert
7
. Es war auch ein signifikanter prognostischer Parameter für das Überleben in unserer Kohorte ( p = 0,02).Tabelle 3 Uni- und multivariable Cox-Regressionsanalyse für das Überleben.
Patienten mit niedrigem OxyHem ≤ 12,5 g/dl zeigten eine signifikant schlechtere Überlebenszeit als Patienten mit OxyHem > 12,5 g/dl mit 1-, 3-, 5-Jahres-Überlebensraten von 98,7 %, 82,9 % und 71,2 % gegenüber 99,3 %, 95,7 % und 80,3 % (Kaplan-Meier P = 0,046, Abb.
2
). In der multivariablen Cox-Regressionsanalyse wurden ein niedriger DLCO, das Vorhandensein einer ILD und ein höheres Alter als unabhängige prognostische Prädiktoren für das Überleben identifiziert (kombiniert P < 0,0001, Abb.
3
).Figur 2
. Receiver Operating Characteristic (ROC)-Analysen für OxyHem entsprachen dem Grenzwert aus Literatur
7
von 12,5 g/dl (ROC-Fläche unter der Kurve P = 0,004). Insgesamt hatten 94 SSc-Patienten OxyHem ≤ 12,5 g/dl und 173 SSc-Patienten OxyHem-Werte über 12,5 g/dl (Tabelle
2
). Im Vergleich zu Patienten mit OxyHem > 12,5 g/dl waren Patienten mit niedrigem OxyHem hauptsächlich weiblich (n = 87, 92,6 % vs. n = 132, 76,3 %, p = 0,001), hatten überwiegend lcSSc (n = 75, 79,8 % vs n = 122, 70,5 %, P = 0,011), ein stärker beeinträchtigter Eisenstoffwechsel in Bezug auf niedrigere Ferritinwerte (75,3 ± 83,6 vs. 126,7 ± 150,6 µg/l, P = 0,004) im Normalbereich, mittleres korpuskuläres Erythrozytenvolumen (MCV) (88,1 ± 8,7 vs. 90,3 ± 5,2 fl, P = 0,027) und mittleres korpuskuläres Hämoglobin in Erythrozyten (29,1 ± 3,0 vs. 30,1 ± 2,4 pg, P = 0,006) . ). Darüber hinaus waren sie klinisch eingeschränkter in Bezug auf WHO-FC ( P = 0,001), kürzere 6MGT (408,6 ± 101,3 vs. 437,8 ± 102,0 m, P = 0,036) und größere hämodynamische Beeinträchtigung mit einem höheren pulmonalen Gefäßwiderstand (PVR) ( 3,2 ± 2,6 vs. 2,4 ± 1,9 Wood Units (WU), P = 0,018) und mPAP (25,6 ± 11,7 vs. 21,6 ± 9,3 mmHg, P = 0,005) (Tabelle
2
). Es gab keinen signifikanten Unterschied im N-terminalen natriuretischen Pro-Gehirn-Peptid (NTproBNP) zwischen den beiden Gruppen. Von 94 Patienten mit OxyHem ≤ 12,5 g/dl litten 29 an ILD (23,7 %). Bei 59 Patienten mit niedrigem OxyHem lag der mPAP bei ≥ 21 mmHg (Abb.
1
). Eine begleitende ILD wurde bei 70 Patienten diagnostiziert, von denen 50 einen mPAP ≥ 21 mmHg aufwiesen. Bei 22 Patienten wurde eine Erhöhung des pulmonalarteriellen Keildrucks (PAWP) > 15 mmHg festgestellt, 19 wiesen einen mPAP ≥ 21 mmHg auf (Abb.
1
). Sechs Patienten hatten eine PH aufgrund einer Erkrankung des linken Herzens und der Lunge. Die Parameter des Lungenfunktionstests (PFT) waren bei Patienten mit niedrigerem OxyHem signifikant stärker beeinträchtigt, einschließlich der maximalen Vitalkapazität (VCmax), des forcierten exspiratorischen Volumens in einer Sekunde (FEV 1) und Gesamtlungenkapazität (TLC). In der Laboranalyse war das C-reaktive Protein (CRP) in der niedrigen OxyHem-Gruppe höher ( p = 0,020) und diese Patienten hatten signifikant niedrigere Hämoglobinwerte (Hb) ( p < 0,0001). Es gab keinen Unterschied in der Nierenfunktion zwischen den beiden Gruppen (Tabelle
2
).Tabelle 2 Klinische Merkmale der OxyHem-Untergruppen.
Überleben bei SSc-PatientenInnerhalb des Beobachtungszeitraums von 3,2 ± 2,6 (Median 2,7; Interquartilsabstand 3,5) Jahren starben 47 Patienten (17,6 %): 22 an PH (46,8 %), 4 an PH und/oder ILD (8,5 %), 3 an ILD (6,4 %), 7 aufgrund von Krebs (14,9 %), eine aufgrund einer Lungensepsis (2,1 %) und 3 aufgrund einer Linksherzerkrankung (6,4 %). Zwei Patienten wurden aufgrund von PH und ILD einer Lungentransplantation unterzogen. In sieben Fällen blieb die Todesursache unbekannt (14,9 %). Das mittlere geschätzte Gesamtüberleben betrug 7,7 ± 0,3 Standardfehler der mittleren Jahre (95 % Konfidenzintervall 7,1 bis 8,2) vom Ausgangswert. Das Überleben war bei männlichen und weiblichen Patienten ähnlich ( p = 0,624) und zwischen Patienten mit dcSSc und lcSSc ( p = 0,694).In der univariablen Kaplan-Meier-Analyse waren OxyHem ≤ 12,5 g/dl ( P = 0,046), Alter zu Studienbeginn ≥ 60 Jahre ( P = 0,002), das Vorhandensein von ILD ( P < 0,0001), hoher PVR ≥ 2 WU ( P = 0,002) und ein niedriger DLCO von ≤ 65 % des Sollwerts ( P < 0,001) waren signifikant mit einem schlechteren Überleben verbunden (Tabelle
3
). Die Anzahl der weißen Blutkörperchen (WBC) ≥ 10.000/ml wurde zusammen mit OxyHem in der ursprünglich beschriebenen COPD-Kohorte analysiert
7
. Es war auch ein signifikanter prognostischer Parameter für das Überleben in unserer Kohorte ( p = 0,02).Tabelle 3 Uni- und multivariable Cox-Regressionsanalyse für das Überleben.
Patienten mit niedrigem OxyHem ≤ 12,5 g/dl zeigten eine signifikant schlechtere Überlebenszeit als Patienten mit OxyHem > 12,5 g/dl mit 1-, 3-, 5-Jahres-Überlebensraten von 98,7 %, 82,9 % und 71,2 % gegenüber 99,3 %, 95,7 % und 80,3 % (Kaplan-Meier P = 0,046, Abb.
2
). In der multivariablen Cox-Regressionsanalyse wurden ein niedriger DLCO, das Vorhandensein einer ILD und ein höheres Alter als unabhängige prognostische Prädiktoren für das Überleben identifiziert (kombiniert P < 0,0001, Abb.
3
).Figur 2
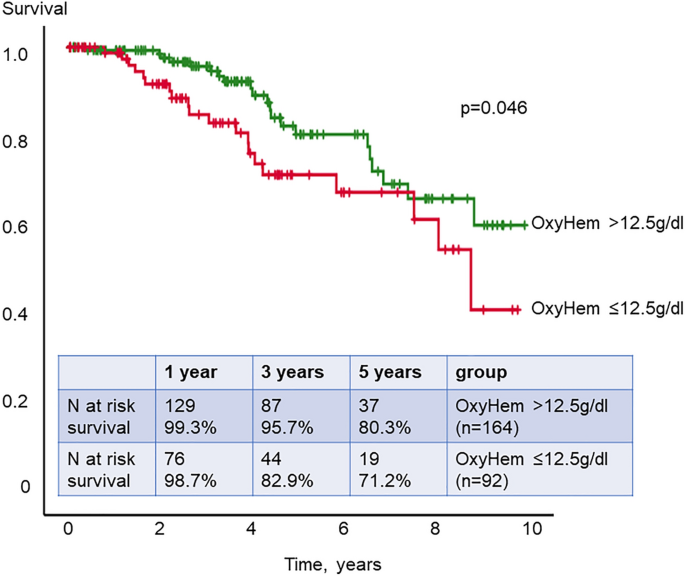 Kaplan-Meier-Analyse von OxyHem. Patienten mit einem OxyHem-Wert von gleich oder weniger als 12,5 g/dl hatten in unserer Studienkohorte ein signifikant kürzeres Überleben.
Figur 3
Kaplan-Meier-Analyse von OxyHem. Patienten mit einem OxyHem-Wert von gleich oder weniger als 12,5 g/dl hatten in unserer Studienkohorte ein signifikant kürzeres Überleben.
Figur 3
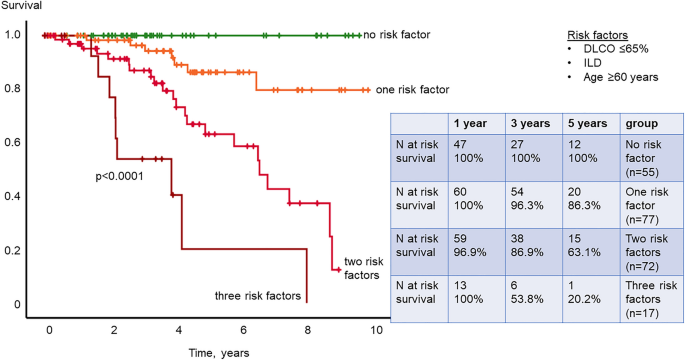 Kaplan-Meier-Analyse des multivariablen Risikosatzes. Zur Risikostratifizierung wurde ein multivariables Risikoset verwendet, das DLCO ≤ 65 % des Sollwerts, ILD und Alter ≥ 60 Jahre umfasste.
OxyHem bei LungengefäßerkrankungenZu Studienbeginn hatten Patienten mit PH (mPAP ≥ 21 mmHg) die höchste Rate an niedrigem OxyHem (41,8 %) im Vergleich zu Patienten mit normaler Hämodynamik (27,8 % niedriges OxyHem; Chi-Quadrat P = 0,016). Niedriges OxyHem bei der Nachuntersuchung war jedoch nicht mit dem hämodynamischen Status assoziiert ( p = 0,562) (Tabelle
4
). PH zu Studienbeginn konnte mit 41,8 % Sensitivität und 72,7 % Spezifität durch niedriges OxyHem vorhergesagt werden. Bei Kombination von niedrigem DLCO und niedrigem OxyHem hatte die Vorhersage des PH zu Studienbeginn eine Sensitivität von 76,1 % und eine Spezifität von 50,6 %. Im Vergleich dazu erreichte Schritt 1 des DETECT-Algorithmus
10
eine Sensitivität von 85,3 % und eine Spezifität von 37,0 %. In Schritt 2 des DETECT-Algorithmus
10
konnten zu Studienbeginn 79,4 % Sensitivität und 73,6 % Spezifität für PH erreicht werden.Tabelle 4 Häufigkeit von niedrigem OxyHem bei Patienten mit PH oder PAH.
Bei Verwendung der drei unabhängigen Risikofaktoren DLCO ≤ 65 % vorhergesagt, Alter ≥ 60 Jahre und Vorliegen einer ILD konnte das Auftreten einer PH mit mPAP ≥ 21 mmHg während der Nachsorge mit einer Sensitivität von 91,1 % und einer Spezifität von 34,6 % vorhergesagt werden mindestens einer der drei Risikofaktoren war erfüllt. Die Kombination von DLCO ≤ 65 % vorhergesagt und OxyHem ≤ 12,5 g/dl hatte eine Sensitivität von 58,7 % und eine Spezifität von 72,9 % für die Vorhersage von PH während der Nachbeobachtung, wenn mindestens einer der beiden Risikofaktoren erfüllt war (Vorhersage von 44 von 44 von 57; richtig negativ 35 von 66).DiskussionIn dieser Studie wurde erstmals nachgewiesen, dass SSc-Patienten mit einem OxyHem-Spiegel ≤ 12,5 g/dl ein signifikant schlechteres Überleben haben als Patienten mit einem OxyHem-Spiegel > 12,5 g/dl ( P = 0,046). ILD, niedriger DLCO, höheres Alter waren robuste prognostische Faktoren im Zusammenhang mit dem Überleben in der multivariablen Analyse. Darüber hinaus waren niedriges OxyHem in Kombination mit niedrigem DLCO zu Studienbeginn Prädiktoren für PH zu Studienbeginn und während der Nachbeobachtung (Sensitivität 76,1 % bzw. 58,7 %, Spezifität 50,6 % bzw. 72,9 %). Unseres Wissens ist dies die erste Studie, die den Einfluss von OxyHem als Prädiktor für das Überleben bei SSc-Patienten aufzeigt.OxyHem- und SSc-PrognoseLower OxyHem wurde bei Patienten mit kürzerer Überlebenszeit identifiziert, was den Einfluss der Oxygenierung und die Bedeutung des Sauerstofftransports bei Patienten mit ausgedehnter Fibrose und Vaskulopathie hervorhebt, die typischerweise SSc charakterisieren
11
. Patienten mit niedrigem OxyHem zeigten häufiger klinische Merkmale mit schlechterem Überleben in zuvor beschriebenen Risikostratifizierungsmodellen, wie z. B. größere WHO-FC
12
, erhöhtes CRP
1
, Vorhandensein von ILD
1
, niedrigere VCmax und DLCO
13
sowie niedrigeres Hb und kürzere 6MGT
12
,
13
. Patienten mit lcSSc und Patientinnen hatten in unserer Kohorte signifikant häufiger einen niedrigen OxyHem-Spiegel. Da bei diesen Patienten kein Risiko für ein beeinträchtigtes Ergebnis vermutet wird, unterstreicht dies die Wichtigkeit, auch Patienten mit niedrigem Risiko zu untersuchen
1
,
12
,
13
,
14
,
15
,
16
.SSc und OxygenierungDie Bedeutung der Sauerstoffsättigung nach dem Training als Prädiktor für die Sterblichkeit bei SSc-ILD-Patienten wurde zuvor evaluiert
5
. Die belastungsinduzierte Entsättigung erwies sich im PHAROS-Register auch als Prädiktor für die Mortalität bei Patienten mit PH-Risiko, obwohl sich die SaO 2 in Ruhe zwischen den Gruppen nicht unterschied
17
und in der DIBOSA-Studie ein Zusammenhang mit dem 3-Jahres-Überleben festgestellt wurde
18
. Wu et al. berichteten, dass eine Entsättigung < 94 % bei 6MGT in Kombination mit dem Vorhandensein von Arthritis mit einer Krankheitsprogression bei SSc-ILD
4 assoziiert war
. Im Gegensatz dazu kann für die Berechnung von OxyHem die Ruhesauerstoffsättigung herangezogen werden, was den Parameter im Vergleich zur Messung der Sauerstoffsättigung unter Belastung einfacher zu bestimmen und für den Patienten weniger anstrengend macht.PVDIn unserer Kohorte war OxyHem nur zu Studienbeginn, aber nicht bei der Nachbeobachtung mit pulmonaler Vaskulopathie assoziiert. Dies könnte durch den Beginn einer zielgerichteten PAH-Therapie nach der Diagnose verursacht werden. Höper et al. berichteten, dass die Oxygenierung kein prognostischer Marker für das Überleben bei häufig behandelten Patienten mit idiopathischer PAH war, was unsere Ergebnisse stützt
19
. Kürzlich haben Valentin et al. (2021) zeigten, dass eine Sauerstoffentsättigung (SaO 2 ) ≥ 3 % zum Zeitpunkt der ersten Nachuntersuchung nach einem Jahr in Kombination mit niedrigem DLCO signifikant mit einer schlechteren Prognose von PAH assoziiert war
20
, was mit unseren Ergebnissen übereinstimmt, die niedriges OxyHem und niedriges DLCO verknüpfen mit früher PVD. In dieser Kohorte korrelierte das männliche Geschlecht nicht mit dem Überleben in Übereinstimmung mit den Ergebnissen aus der Literatur
6
,
21
,
22
.Stärken und Grenzen der StudieDiese Studie liefert wichtige Einblicke in prognostische Prädiktoren und Stratifizierungsmodelle bei SSc-Patienten, die auf PH gescreent wurden. Das Screening auf PH wurde in einem Expertenzentrum durchgeführt, einschließlich einer gründlichen diagnostischen Aufarbeitung, was zu einer gut charakterisierten Studienkohorte führte. OxyHem bietet einen Parameter, der bei verschiedenen Organbeteiligungen bei SSc wie ILD, PH und Herzerkrankungen pathophysiologisch wichtig ist. Während es in der univariablen Analyse ein signifikanter Prädiktor war, wurde es im multivariablen Modell übertroffen. Dies könnte auf die begrenzte Stichprobengröße oder den starken Einfluss der ILD auf die Prognose zurückzuführen sein. Da wir nur ausgedehnte ILD in unsere Bewertung einbezogen haben, könnte dies die Ergebnisse ebenfalls verzerrt haben. Eine der Haupteinschränkungen dieser Studie ist ihr retrospektiver Charakter, der aufgrund fehlender Parameter zu einem kleineren Datensatz führt. Frühe prognostische Marker müssen in zukünftigen, prospektiven Studien untersucht werden. Wir hatten auch keine Kontrollkohorte gesunder Personen oder anderer gut charakterisierter Patienten, mit denen wir unsere Ergebnisse vergleichen konnten. Der prognostische Wert von OxyHem wurde jedoch bereits bei COPD-Patienten beschrieben
7
. Darüber hinaus konnten andere Organmanifestationen von SSc, wie gastrointestinale Manifestationen und Nierenkrise, aufgrund fehlender Daten nicht berücksichtigt werden. Obwohl die Kohortengröße unserer Studie für eine so seltene Krankheit groß ist, war die Stichprobengröße der Untergruppen zu klein, um die Auswirkungen von OxyHem auf das Überleben bei ILD und PH getrennt zu differenzieren. Eine weitere Einschränkung besteht darin, dass in unserer Kohorte die Blutgasanalyse mit arterialisiertem Kapillarblut aus dem Ohrläppchen durchgeführt wurde, das möglicherweise nicht in Standard-Screening-Verfahren von Rheumatologen einbezogen wird. Allerdings hat diese Methode bereits eine gute Korrelation mit der arteriellen Punktion gezeigt
23
. Die Bedeutung von OxyHem im Krankheitsverlauf inklusive Follow-up-Daten sollte in zukünftigen Studien thematisiert werden. Schließlich umfasste unsere Kohorte nur SSc-Patienten, die zum Screening auf PH überwiesen wurden, was zu verzerrten Daten hätte führen können.SchlussfolgerungenDie Ergebnisse dieser Studie zeigten, dass OxyHem ein neuer Biomarker sein könnte, der für die Risikostratifizierung bei SSc und die Identifizierung von Patienten mit früher PVD bzw. PH verwendet werden könnte. OxyHem ist in der täglichen Routine leicht zu berechnen und Werte ≤ 12,5 g/dl waren signifikant mit einem schlechteren Überleben assoziiert. Darüber hinaus könnte die Kombination von DLCO ≤ 65 % vorhergesagt und niedrigem OxyHem die Entwicklung einer frühen PVD in dieser Kohorte vorhersagen. Weitere prospektive Studien sind erforderlich, um die Ergebnisse zu bestätigen.MethodenStudienpopulationSSc-Patienten mit dcSSc oder lcSSc
24
, die zwischen 2008 und 2020 von ihren Rheumatologen an unser Zentrum für PH an der Thoraxklinik Heidelberg gGmbH am Universitätsklinikum Heidelberg, Deutschland, überwiesen wurden, wurden in dieser monozentrischen Querschnitts-Kohortenstudie retrospektiv analysiert. Alle Patienten erfüllten die SSc-Klassifikationskriterien des American College of Rheumatology/European League against Rheumatism
25
und wurden gemäß den aktuellen Empfehlungen jährlich nachuntersucht
9
. Personen wurden ausgeschlossen, wenn sie minderjährig waren, andere rheumatische Erkrankungen als SSc hatten, fehlende Daten für die Berechnung von OxyHem hatten oder nicht in der Lage waren, ihre Einverständniserklärung abzugeben. Daten eines Teils dieser Kohorte wurden bereits vor
26 analysiert und veröffentlicht
. Die Ethikkommission der Medizinischen Fakultät der Universität Heidelberg (interne Nummer S-126/2021) hatte keine Einwände gegen die Durchführung dieser Studie. Alle Patienten gaben ein schriftliches Einverständnis zur Analyse der Daten. Die Studie entspricht der Deklaration von Helsinki in ihrer aktuellen Fassung.StudiendesignDaten aus routinemäßig durchgeführten Untersuchungen wurden bei der ersten Vorstellung im PH-Zentrum aus den Patientenakten extrahiert. Die Patienten wurden von ihren Rheumatologen wegen ungeklärter Atemnot und/oder Verdacht auf PH zum Screening auf PH überwiesen. Bei allen Patienten wurde eine ausführliche klinische Aufarbeitung durchgeführt. Das routinemäßig durchgeführte Screening umfasste die Anamnese, die Erfassung von Begleiterkrankungen wie arterieller Hypertonie, koronarer Herzkrankheit oder Adipositas (BMI > 30 kg/m 2 ).), körperliche Untersuchung, Elektrokardiogramm, PFT mit DLCO, Blutgasanalyse aus arterialisiertem Kapillarblut aus dem Ohrläppchen, Echokardiographie in Ruhe und unter Belastung, hochauflösende Computertomographie der Lunge (HRCT), um das Vorhandensein von Lungenmanifestationen oder -erkrankungen zu untersuchen , WHO-FC, 6MWD-Test unter standardisierten Bedingungen
27
, Laboruntersuchungen inkl. Blutbild, NTproBNP, CRP, Analyse auf Eisenmangel, Nierenfunktion inkl. glomerulärer Filtrationsrate und Rechtsherzkatheter in Ruhe und/oder unter Belastung.Das Vorliegen von Herzerkrankungen wie koronarer Herzkrankheit und pulmonalen Manifestationen wie PH oder ILD wurde dokumentiert und im Falle einer Pathologie weiter untersucht. Eine ILD wurde nur im Falle einer ausgedehnten ILD in Betracht gezogen, definiert als das Vorhandensein einer signifikanten interstitiellen Fibrose im HRCT der Lunge (> 20 % des Parenchyms) oder eines restriktiven Musters im PFT (VCmax < 70 % vorhergesagt mit einem normalen Verhältnis von FEV1 zu VC ) bei fehlender Quantifizierung der interstitiellen Fibrose im HRCT
28
. Manifeste PAH wurde nach gültigen Leitlinien zum Zeitpunkt der Studie diagnostiziert (mPAP ≥ 25 mmHg, PAWP ≤ 15 mmHg und PVR > 3 WU), gemessen durch RHC
9
. Anzeichen einer frühen PVD wurden als mPAP ≥ 21 mmHg definiert. PH aufgrund einer Linksherzerkrankung wurde durch einen mPAP ≥ 21 mmHg mit einem PAWP > 15 mmHg definiert
29
. PH aufgrund einer Lungenerkrankung basierte auf Lungenfunktionsparametern und im Falle einer ILD-HRCT-Bildgebung
30
.statistische MethodenStatistische Analysen wurden von einem medizinischen Statistiker (NB) durchgeführt. Die Daten werden als Mittelwert ± Standardabweichung (SD) mit einem Konfidenzintervall von 95 % des Mittelwerts dargestellt. Häufigkeitsdaten werden als n und % dargestellt. Die Konzentration von OxyHem (g/dl) wurde zu Studienbeginn durch Multiplikation der Hb-Konzentration im Blut mit der während der Blutgasanalyse gemessenen SaO 2 berechnet, wie zuvor beschrieben
7
.Die Überlebensanalyse wurde unter Verwendung der Kaplan-Meier- und Cox-Regressionsanalyse durchgeführt. Das Datum des ersten Screening-Besuchs wurde als Ausgangswert für die Überlebensanalyse festgelegt. Tod wurde als Tod aus jedweder Ursache definiert. Schwellenwerte für die Dichotomisierung von Parametern wurden entweder aus der Literatur bekannter prognostischer Prädiktoren oder durch ROC erhalten, falls der Schwellenwert unbekannt war oder eine Schwellenwertanpassung erforderlich war. Klinische Parameter wurden mit dem zweiseitigen Student's t-Test für unabhängige Stichproben für Patienten über und unter der OxyHem-Schwelle verglichen. Qualitative Daten wurden jeweils mit dem Chi-Quadrat-Test analysiert. Diese Studie hat explorativen Charakter. P-Werte < 0,05 wurden als statistisch signifikant angesehen und nicht für multiples Testen angepasst.Variablen wurden durch univariable Analyse ausgewertet, um ihre Auswirkungen auf das Überleben zu identifizieren. Die Parameter wurden dann mit multivariabler Cox-Regressionsanalyse analysiert. OxyHem wurde mit bekannten prognostischen Faktoren bei SSc verglichen, die durch Literaturrecherche identifiziert wurden. Dazu gehörten Geschlecht, Art der SSc, Alter ≥ 60 Jahre bei Studienbeginn
31
, Vorliegen einer ILD
1
,
15
, PVR ≥ 2 WU
26
, DLCO ≤ 65 % des Sollwerts
13
. Darüber hinaus wurde die Leukozytenzahl aufgenommen, da sie neben OxyHem in der OxyHem-Entdeckungskohorte
7
eine signifikante Vorhersagekraft zeigte . Für die multivariable Cox-Regression wurden alle oben aufgeführten Parameter berücksichtigt.Eine Überlebensanalyse wurde bei Untergruppen von Patienten mit Anzeichen einer kardiovaskulären Erkrankung mit entweder erhöhtem PVR ≥ 2 WU oder mit mPAP ≥ 25 mmHg durchgeführt. Alle Analysen wurden mit IBM SPSS Version 27 (SPSS Statistics V27, IBM Corporation, Somers, New York) durchgeführt.Ethik-Zustimmung und Zustimmung zur TeilnahmeAlle Daten wurden pseudonymisiert und die Studie von der Ethikkommission der Medizinischen Fakultät des Universitätsklinikums Heidelberg genehmigt (interne Nummer S-126/2021). Die Studie entspricht der Deklaration von Helsinki in ihrer aktuellen Fassung. Die an dieser Studie teilnehmenden Patienten gaben eine schriftliche Einverständniserklärung ab.
Kaplan-Meier-Analyse des multivariablen Risikosatzes. Zur Risikostratifizierung wurde ein multivariables Risikoset verwendet, das DLCO ≤ 65 % des Sollwerts, ILD und Alter ≥ 60 Jahre umfasste.
OxyHem bei LungengefäßerkrankungenZu Studienbeginn hatten Patienten mit PH (mPAP ≥ 21 mmHg) die höchste Rate an niedrigem OxyHem (41,8 %) im Vergleich zu Patienten mit normaler Hämodynamik (27,8 % niedriges OxyHem; Chi-Quadrat P = 0,016). Niedriges OxyHem bei der Nachuntersuchung war jedoch nicht mit dem hämodynamischen Status assoziiert ( p = 0,562) (Tabelle
4
). PH zu Studienbeginn konnte mit 41,8 % Sensitivität und 72,7 % Spezifität durch niedriges OxyHem vorhergesagt werden. Bei Kombination von niedrigem DLCO und niedrigem OxyHem hatte die Vorhersage des PH zu Studienbeginn eine Sensitivität von 76,1 % und eine Spezifität von 50,6 %. Im Vergleich dazu erreichte Schritt 1 des DETECT-Algorithmus
10
eine Sensitivität von 85,3 % und eine Spezifität von 37,0 %. In Schritt 2 des DETECT-Algorithmus
10
konnten zu Studienbeginn 79,4 % Sensitivität und 73,6 % Spezifität für PH erreicht werden.Tabelle 4 Häufigkeit von niedrigem OxyHem bei Patienten mit PH oder PAH.
Bei Verwendung der drei unabhängigen Risikofaktoren DLCO ≤ 65 % vorhergesagt, Alter ≥ 60 Jahre und Vorliegen einer ILD konnte das Auftreten einer PH mit mPAP ≥ 21 mmHg während der Nachsorge mit einer Sensitivität von 91,1 % und einer Spezifität von 34,6 % vorhergesagt werden mindestens einer der drei Risikofaktoren war erfüllt. Die Kombination von DLCO ≤ 65 % vorhergesagt und OxyHem ≤ 12,5 g/dl hatte eine Sensitivität von 58,7 % und eine Spezifität von 72,9 % für die Vorhersage von PH während der Nachbeobachtung, wenn mindestens einer der beiden Risikofaktoren erfüllt war (Vorhersage von 44 von 44 von 57; richtig negativ 35 von 66).DiskussionIn dieser Studie wurde erstmals nachgewiesen, dass SSc-Patienten mit einem OxyHem-Spiegel ≤ 12,5 g/dl ein signifikant schlechteres Überleben haben als Patienten mit einem OxyHem-Spiegel > 12,5 g/dl ( P = 0,046). ILD, niedriger DLCO, höheres Alter waren robuste prognostische Faktoren im Zusammenhang mit dem Überleben in der multivariablen Analyse. Darüber hinaus waren niedriges OxyHem in Kombination mit niedrigem DLCO zu Studienbeginn Prädiktoren für PH zu Studienbeginn und während der Nachbeobachtung (Sensitivität 76,1 % bzw. 58,7 %, Spezifität 50,6 % bzw. 72,9 %). Unseres Wissens ist dies die erste Studie, die den Einfluss von OxyHem als Prädiktor für das Überleben bei SSc-Patienten aufzeigt.OxyHem- und SSc-PrognoseLower OxyHem wurde bei Patienten mit kürzerer Überlebenszeit identifiziert, was den Einfluss der Oxygenierung und die Bedeutung des Sauerstofftransports bei Patienten mit ausgedehnter Fibrose und Vaskulopathie hervorhebt, die typischerweise SSc charakterisieren
11
. Patienten mit niedrigem OxyHem zeigten häufiger klinische Merkmale mit schlechterem Überleben in zuvor beschriebenen Risikostratifizierungsmodellen, wie z. B. größere WHO-FC
12
, erhöhtes CRP
1
, Vorhandensein von ILD
1
, niedrigere VCmax und DLCO
13
sowie niedrigeres Hb und kürzere 6MGT
12
,
13
. Patienten mit lcSSc und Patientinnen hatten in unserer Kohorte signifikant häufiger einen niedrigen OxyHem-Spiegel. Da bei diesen Patienten kein Risiko für ein beeinträchtigtes Ergebnis vermutet wird, unterstreicht dies die Wichtigkeit, auch Patienten mit niedrigem Risiko zu untersuchen
1
,
12
,
13
,
14
,
15
,
16
.SSc und OxygenierungDie Bedeutung der Sauerstoffsättigung nach dem Training als Prädiktor für die Sterblichkeit bei SSc-ILD-Patienten wurde zuvor evaluiert
5
. Die belastungsinduzierte Entsättigung erwies sich im PHAROS-Register auch als Prädiktor für die Mortalität bei Patienten mit PH-Risiko, obwohl sich die SaO 2 in Ruhe zwischen den Gruppen nicht unterschied
17
und in der DIBOSA-Studie ein Zusammenhang mit dem 3-Jahres-Überleben festgestellt wurde
18
. Wu et al. berichteten, dass eine Entsättigung < 94 % bei 6MGT in Kombination mit dem Vorhandensein von Arthritis mit einer Krankheitsprogression bei SSc-ILD
4 assoziiert war
. Im Gegensatz dazu kann für die Berechnung von OxyHem die Ruhesauerstoffsättigung herangezogen werden, was den Parameter im Vergleich zur Messung der Sauerstoffsättigung unter Belastung einfacher zu bestimmen und für den Patienten weniger anstrengend macht.PVDIn unserer Kohorte war OxyHem nur zu Studienbeginn, aber nicht bei der Nachbeobachtung mit pulmonaler Vaskulopathie assoziiert. Dies könnte durch den Beginn einer zielgerichteten PAH-Therapie nach der Diagnose verursacht werden. Höper et al. berichteten, dass die Oxygenierung kein prognostischer Marker für das Überleben bei häufig behandelten Patienten mit idiopathischer PAH war, was unsere Ergebnisse stützt
19
. Kürzlich haben Valentin et al. (2021) zeigten, dass eine Sauerstoffentsättigung (SaO 2 ) ≥ 3 % zum Zeitpunkt der ersten Nachuntersuchung nach einem Jahr in Kombination mit niedrigem DLCO signifikant mit einer schlechteren Prognose von PAH assoziiert war
20
, was mit unseren Ergebnissen übereinstimmt, die niedriges OxyHem und niedriges DLCO verknüpfen mit früher PVD. In dieser Kohorte korrelierte das männliche Geschlecht nicht mit dem Überleben in Übereinstimmung mit den Ergebnissen aus der Literatur
6
,
21
,
22
.Stärken und Grenzen der StudieDiese Studie liefert wichtige Einblicke in prognostische Prädiktoren und Stratifizierungsmodelle bei SSc-Patienten, die auf PH gescreent wurden. Das Screening auf PH wurde in einem Expertenzentrum durchgeführt, einschließlich einer gründlichen diagnostischen Aufarbeitung, was zu einer gut charakterisierten Studienkohorte führte. OxyHem bietet einen Parameter, der bei verschiedenen Organbeteiligungen bei SSc wie ILD, PH und Herzerkrankungen pathophysiologisch wichtig ist. Während es in der univariablen Analyse ein signifikanter Prädiktor war, wurde es im multivariablen Modell übertroffen. Dies könnte auf die begrenzte Stichprobengröße oder den starken Einfluss der ILD auf die Prognose zurückzuführen sein. Da wir nur ausgedehnte ILD in unsere Bewertung einbezogen haben, könnte dies die Ergebnisse ebenfalls verzerrt haben. Eine der Haupteinschränkungen dieser Studie ist ihr retrospektiver Charakter, der aufgrund fehlender Parameter zu einem kleineren Datensatz führt. Frühe prognostische Marker müssen in zukünftigen, prospektiven Studien untersucht werden. Wir hatten auch keine Kontrollkohorte gesunder Personen oder anderer gut charakterisierter Patienten, mit denen wir unsere Ergebnisse vergleichen konnten. Der prognostische Wert von OxyHem wurde jedoch bereits bei COPD-Patienten beschrieben
7
. Darüber hinaus konnten andere Organmanifestationen von SSc, wie gastrointestinale Manifestationen und Nierenkrise, aufgrund fehlender Daten nicht berücksichtigt werden. Obwohl die Kohortengröße unserer Studie für eine so seltene Krankheit groß ist, war die Stichprobengröße der Untergruppen zu klein, um die Auswirkungen von OxyHem auf das Überleben bei ILD und PH getrennt zu differenzieren. Eine weitere Einschränkung besteht darin, dass in unserer Kohorte die Blutgasanalyse mit arterialisiertem Kapillarblut aus dem Ohrläppchen durchgeführt wurde, das möglicherweise nicht in Standard-Screening-Verfahren von Rheumatologen einbezogen wird. Allerdings hat diese Methode bereits eine gute Korrelation mit der arteriellen Punktion gezeigt
23
. Die Bedeutung von OxyHem im Krankheitsverlauf inklusive Follow-up-Daten sollte in zukünftigen Studien thematisiert werden. Schließlich umfasste unsere Kohorte nur SSc-Patienten, die zum Screening auf PH überwiesen wurden, was zu verzerrten Daten hätte führen können.SchlussfolgerungenDie Ergebnisse dieser Studie zeigten, dass OxyHem ein neuer Biomarker sein könnte, der für die Risikostratifizierung bei SSc und die Identifizierung von Patienten mit früher PVD bzw. PH verwendet werden könnte. OxyHem ist in der täglichen Routine leicht zu berechnen und Werte ≤ 12,5 g/dl waren signifikant mit einem schlechteren Überleben assoziiert. Darüber hinaus könnte die Kombination von DLCO ≤ 65 % vorhergesagt und niedrigem OxyHem die Entwicklung einer frühen PVD in dieser Kohorte vorhersagen. Weitere prospektive Studien sind erforderlich, um die Ergebnisse zu bestätigen.MethodenStudienpopulationSSc-Patienten mit dcSSc oder lcSSc
24
, die zwischen 2008 und 2020 von ihren Rheumatologen an unser Zentrum für PH an der Thoraxklinik Heidelberg gGmbH am Universitätsklinikum Heidelberg, Deutschland, überwiesen wurden, wurden in dieser monozentrischen Querschnitts-Kohortenstudie retrospektiv analysiert. Alle Patienten erfüllten die SSc-Klassifikationskriterien des American College of Rheumatology/European League against Rheumatism
25
und wurden gemäß den aktuellen Empfehlungen jährlich nachuntersucht
9
. Personen wurden ausgeschlossen, wenn sie minderjährig waren, andere rheumatische Erkrankungen als SSc hatten, fehlende Daten für die Berechnung von OxyHem hatten oder nicht in der Lage waren, ihre Einverständniserklärung abzugeben. Daten eines Teils dieser Kohorte wurden bereits vor
26 analysiert und veröffentlicht
. Die Ethikkommission der Medizinischen Fakultät der Universität Heidelberg (interne Nummer S-126/2021) hatte keine Einwände gegen die Durchführung dieser Studie. Alle Patienten gaben ein schriftliches Einverständnis zur Analyse der Daten. Die Studie entspricht der Deklaration von Helsinki in ihrer aktuellen Fassung.StudiendesignDaten aus routinemäßig durchgeführten Untersuchungen wurden bei der ersten Vorstellung im PH-Zentrum aus den Patientenakten extrahiert. Die Patienten wurden von ihren Rheumatologen wegen ungeklärter Atemnot und/oder Verdacht auf PH zum Screening auf PH überwiesen. Bei allen Patienten wurde eine ausführliche klinische Aufarbeitung durchgeführt. Das routinemäßig durchgeführte Screening umfasste die Anamnese, die Erfassung von Begleiterkrankungen wie arterieller Hypertonie, koronarer Herzkrankheit oder Adipositas (BMI > 30 kg/m 2 ).), körperliche Untersuchung, Elektrokardiogramm, PFT mit DLCO, Blutgasanalyse aus arterialisiertem Kapillarblut aus dem Ohrläppchen, Echokardiographie in Ruhe und unter Belastung, hochauflösende Computertomographie der Lunge (HRCT), um das Vorhandensein von Lungenmanifestationen oder -erkrankungen zu untersuchen , WHO-FC, 6MWD-Test unter standardisierten Bedingungen
27
, Laboruntersuchungen inkl. Blutbild, NTproBNP, CRP, Analyse auf Eisenmangel, Nierenfunktion inkl. glomerulärer Filtrationsrate und Rechtsherzkatheter in Ruhe und/oder unter Belastung.Das Vorliegen von Herzerkrankungen wie koronarer Herzkrankheit und pulmonalen Manifestationen wie PH oder ILD wurde dokumentiert und im Falle einer Pathologie weiter untersucht. Eine ILD wurde nur im Falle einer ausgedehnten ILD in Betracht gezogen, definiert als das Vorhandensein einer signifikanten interstitiellen Fibrose im HRCT der Lunge (> 20 % des Parenchyms) oder eines restriktiven Musters im PFT (VCmax < 70 % vorhergesagt mit einem normalen Verhältnis von FEV1 zu VC ) bei fehlender Quantifizierung der interstitiellen Fibrose im HRCT
28
. Manifeste PAH wurde nach gültigen Leitlinien zum Zeitpunkt der Studie diagnostiziert (mPAP ≥ 25 mmHg, PAWP ≤ 15 mmHg und PVR > 3 WU), gemessen durch RHC
9
. Anzeichen einer frühen PVD wurden als mPAP ≥ 21 mmHg definiert. PH aufgrund einer Linksherzerkrankung wurde durch einen mPAP ≥ 21 mmHg mit einem PAWP > 15 mmHg definiert
29
. PH aufgrund einer Lungenerkrankung basierte auf Lungenfunktionsparametern und im Falle einer ILD-HRCT-Bildgebung
30
.statistische MethodenStatistische Analysen wurden von einem medizinischen Statistiker (NB) durchgeführt. Die Daten werden als Mittelwert ± Standardabweichung (SD) mit einem Konfidenzintervall von 95 % des Mittelwerts dargestellt. Häufigkeitsdaten werden als n und % dargestellt. Die Konzentration von OxyHem (g/dl) wurde zu Studienbeginn durch Multiplikation der Hb-Konzentration im Blut mit der während der Blutgasanalyse gemessenen SaO 2 berechnet, wie zuvor beschrieben
7
.Die Überlebensanalyse wurde unter Verwendung der Kaplan-Meier- und Cox-Regressionsanalyse durchgeführt. Das Datum des ersten Screening-Besuchs wurde als Ausgangswert für die Überlebensanalyse festgelegt. Tod wurde als Tod aus jedweder Ursache definiert. Schwellenwerte für die Dichotomisierung von Parametern wurden entweder aus der Literatur bekannter prognostischer Prädiktoren oder durch ROC erhalten, falls der Schwellenwert unbekannt war oder eine Schwellenwertanpassung erforderlich war. Klinische Parameter wurden mit dem zweiseitigen Student's t-Test für unabhängige Stichproben für Patienten über und unter der OxyHem-Schwelle verglichen. Qualitative Daten wurden jeweils mit dem Chi-Quadrat-Test analysiert. Diese Studie hat explorativen Charakter. P-Werte < 0,05 wurden als statistisch signifikant angesehen und nicht für multiples Testen angepasst.Variablen wurden durch univariable Analyse ausgewertet, um ihre Auswirkungen auf das Überleben zu identifizieren. Die Parameter wurden dann mit multivariabler Cox-Regressionsanalyse analysiert. OxyHem wurde mit bekannten prognostischen Faktoren bei SSc verglichen, die durch Literaturrecherche identifiziert wurden. Dazu gehörten Geschlecht, Art der SSc, Alter ≥ 60 Jahre bei Studienbeginn
31
, Vorliegen einer ILD
1
,
15
, PVR ≥ 2 WU
26
, DLCO ≤ 65 % des Sollwerts
13
. Darüber hinaus wurde die Leukozytenzahl aufgenommen, da sie neben OxyHem in der OxyHem-Entdeckungskohorte
7
eine signifikante Vorhersagekraft zeigte . Für die multivariable Cox-Regression wurden alle oben aufgeführten Parameter berücksichtigt.Eine Überlebensanalyse wurde bei Untergruppen von Patienten mit Anzeichen einer kardiovaskulären Erkrankung mit entweder erhöhtem PVR ≥ 2 WU oder mit mPAP ≥ 25 mmHg durchgeführt. Alle Analysen wurden mit IBM SPSS Version 27 (SPSS Statistics V27, IBM Corporation, Somers, New York) durchgeführt.Ethik-Zustimmung und Zustimmung zur TeilnahmeAlle Daten wurden pseudonymisiert und die Studie von der Ethikkommission der Medizinischen Fakultät des Universitätsklinikums Heidelberg genehmigt (interne Nummer S-126/2021). Die Studie entspricht der Deklaration von Helsinki in ihrer aktuellen Fassung. Die an dieser Studie teilnehmenden Patienten gaben eine schriftliche Einverständniserklärung ab.



OMNIA TEMPUS HABENT
Diagnose IPAH im Februar 2013, in Behandlung bei OA Dr. Ulrich Krüger, jetzt Dr. Fischer Herzzentrum Duisburg, Medikamente: Sildenafil, Bosentan jetzt Macitentan, Subkutane Treprostinilpumpe, seit Januar 2024 getunnelter ZVK mit externer Pumpe (Groshongkatheter), 24/7 Sauerstoff, Marcumar, Diuretika
Bitte Anmelden oder Registrieren um der Konversation beizutreten.
